您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2018-01-18 16:42
熔点的测定
了解熔点测定的意义,掌握测定熔点的方法。
通常当结晶物质加热到一定的温度时,即从固态转变为液态。此时的温度为该化合物的熔点,或者说,熔点应为固液两态在大气压力下成平衡时的温度。纯粹的固体有机化合物一般都有它固定的熔点。常用熔点测定法来鉴定纯粹固体有机化合物。纯化合物开始熔化至完全熔化(初熔至全熔)的温度范围叫熔程。温度一般不超过0.5℃~1℃。如该化合物含有杂质,其熔点往往偏低,且熔程也较长。所以根据熔程长短可判别固体化合物的纯度。
⑴仪器
提勒管或双浴式熔点管 温度计(150℃) 橡皮塞 熔点毛细管 长玻璃管(70-80cm)玻璃棒 表面皿 小胶圈 酒精灯铁架台 显微熔点测定仪。
⑵药品
萘 乙酰苯胺 苯甲酸 尿素 浓硫酸。
四、实验操作(毛细管法测定熔点)
由于熔点的测定对有机化合物的研究具有很大的价值,因此如何测出准确的熔点是一个重要问题。目前测定熔点的方法以毛细管法最为简便。现介绍如下:
①样品的装入
放少许待测熔点的干燥样品(约0.1克)于干净的表面皿上,用玻棒或不锈钢刮刀将它研成粉末并集成一堆。将熔点管开口端向下插入粉末中,然后把熔点管开口端向上,轻轻地在桌面上敲击,以使粉末落入和填紧管底。或者取一支长约30~40厘米的玻管,垂直于一干净的表面皿上,将熔点管从玻管上端自由落下,可更好地达到上述目的,为了要使管内装入高约2~3毫米紧密结实的样品,一般需如此重复数次。沾于管外的粉末须拭去,以免沾污加热浴液。要测得准确的熔点,样品一定要研得极细,装得密实,使热量的传导迅速均匀。对于蜡状的样品,为了解决研细及装管的困难,只得选用较大口径(2毫米左右)的熔点管。
②熔点浴
熔点浴的设计最重要的一点是要使受热均匀。下面介绍两种在实验室中最常用的熔点浴。
a.提勒管(Thiele):又称b形管,如图[2-27左]。管口装有开口软木塞,温度计插入其中,刻度应面向木塞开口,其水银球位于b形管上下两叉管口之间,装好样品的熔点管,借少许浴液沾附于温度计下端,使样品的部分置于水银球侧面中部[见图2-27中]。b形管中装入加热液体(浴液),高度达上叉管处即可。在图示的部位加热,受热的浴液作沿管上升运动。从而促成了整个b形管内浴液呈对流循环,使得温度较均匀。

图2-27 毛细管法测定熔点的装置
b.双浴式:如图[2-27右],将试管经开口软木塞插入250毫升平底(或圆底)烧瓶内,直至离瓶底约1厘米处,试管口也配一个开口软木塞,插入温度计,其水银球应距试管底0.5厘米。瓶内装入约占烧瓶2/3体积的加热体,试管内也放入一些加热液体,使在插入温度计后,其液面高度与瓶内相同。熔点管粘附于温度计和在b形管中相同。
在测定熔点时凡是样品熔点在220℃以下的,可采用浓硫酸作为浴液。但高温时,浓硫酸将分解放出三氧化硫及水。长期不用的熔点浴应先渐渐加热去掉吸入的水分,如加热过快,就有冲出的危险。
当有机物和其他杂质触及硫酸时,会使硫酸变黑。有碍熔点的观察。此时可加入少许硝酸钾晶体共热后使之脱色。
除浓硫酸之外,亦可采用磷酸(可用于300℃以下)、石蜡油或有机硅油等。如将7份浓硫酸和3份硫酸钾或5.5份浓硫酸和4.5份硫酸钾在通风橱中一起加热,直至固体溶解,这样的溶液可应用在220~320℃的范围。若以6份浓硫酸和4份硫酸钾混合,则可使用至365℃。但此类加热液体不适用于测定低熔点的化合物,因为它们在室温下呈半固态或固态。
③熔点的测定
将提勒管垂直夹于铁架上,按前述方法装配完毕,以浓硫酸作为加热液体,用温度计水银球蘸取少许硫酸滴于熔点管上端外壁上,即可使之粘着,图[2-27]。将粘附有熔点管的温度计小心地伸入浴中,以小火缓缓加热。开始时升温速度可以较快,到距离熔点10~15℃时,调整火焰使每分钟上升约1~2℃。愈接近熔点,升温速度应愈慢(掌握升温速度是准确测定熔点的关键)。这一方面是为了保证有充分的时间让热量由管外传至管内,以使固体熔化;另一方面因观察者不能同时观察温度计所示度数和样品的变化情况。只有缓慢加热,才能使此项误差减小。记下样品开始塌落并有液相产生时(初熔)和固体完全消失时(全熔)的温度计读数,即为该化合物的熔程。要注意在初熔前是否有萎缩或软化、放出气体以及其他分解现象。例如一物质在120℃时开始萎缩,在121℃时有液滴出现,在122℃时全部液化,应记录如下:熔点121~122℃,120℃时萎缩。
熔点测定,至少要有两次重复的数据。每一次测定都必须用新的熔点管另装样品,不能将已测过熔点的熔点管冷却,使其中的样品固化后再作第二次测定。因为有时某些物质会产生部分分解,有些会转变成具有不同熔点的其他结晶形式。测定易升华物质的熔点时,应将熔点管的开口端烧熔封闭,以免升华。
如果要测定未知物的熔点,应先对样品粗测一次。加热可以稍快,知道大致的熔点范围后,待浴温冷至熔点以下约30℃左右,再取另一根装样的熔点管作精密的测定。
熔点测好后,温度计的读数须对照温度计校正图进行校正。
一定要待熔点浴冷却后,方可将浓硫酸倒回瓶中。温度计冷却后,用废纸擦去硫酸,否则温度计极易炸裂。
用以上方法测定熔点时,温度计上的熔点读数与真实熔点之间常有一定的偏差。这可能是由于温度计的质量所引起。例如一般温度计中的毛细孔径不一定是很均匀的,有时刻度也不很准确。其次,温度计有全浸式和半浸式两种。全浸式温度计的刻度是在温度计的汞线全部均匀受热的情况下刻出来的,而在测熔点时仅有部分汞线受热,因而露出的汞线温度当然较全部受热者为低。另外经长期使用的温度计,玻璃也可能发生体积变形而使刻度不准。为了校正温度计,可选用一标准温度计与之比较。通常也可采用纯粹有机化合物的熔点作为校正的标准。通过此法校正的温度计,上述误差可一并除去。校正时只要选择数种已知熔点的纯粹化合物作为标准,测定它们的熔点,以观察到的熔点作纵坐标,测得熔点与应有熔点的差数作横坐标,画成曲线,在任一温度时的读数即可直接从曲线中读出。
用熔点方法校正温度计的标准样品如下,校正时可以具体选择。
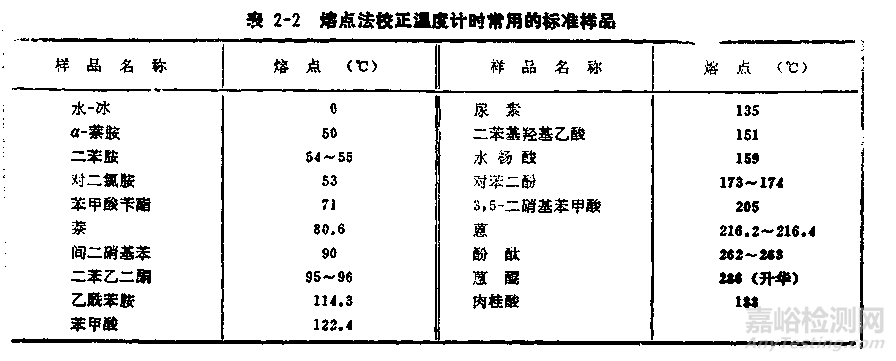
* 零点的测定最好用蒸馏水和纯冰的混合物。在一个15×2.5的试管中放置蒸馏水20毫升,将试管浸在冰盐浴中至蒸馏水部分结冰。用玻棒搅动使之成冰-水混合物。将试管自冰盐浴中移出,然后将温度计插入冰-水中,轻轻搅动混合物,到温度恒定后(2~3min)读数。
1、熔点管本身要干净,管壁不能太厚,封口要均匀。容易出现的问题是,封口一端发生弯曲和封口端壁太厚,所以在毛细管封口时,一端在火焰上加热时要尽量让毛细管接近垂直方向,火焰温度不宜太高,最好用酒精灯,断断续续地加热,封口要圆滑,以不漏气为原则。
2、样品一定要干燥,并要研成细粉末,往毛细管内装样品时,一定要反复冲撞夯实,管外样品要用卫生纸擦干净。
3、用橡皮圈将毛细管缚在温度计旁,并使装样部分和温度计水银球处在同一水平位置,同时要使温度计水银球处于b形管两侧管中心部位。
4、升温速度不宜太快,特别是当温度将要接近该样品的熔点时,升温速度更不能快。一般情况是,开始升温时速度可稍快些(5℃/min)但接近该样品熔点时,升温速度要慢(1~2℃/min),对未知物熔点的测定,第一次可快速升温,测定化合物的大概熔点
5、熔点温度范围(熔程、熔点、熔距)的观察和记录,注意观察时,样品开始萎缩(蹋落)并非熔化开始的指示信号,实际的熔化开始于能看到第一滴液体时,记下此时的温度,到所有晶体完全消失呈透明液体时再记下这时的温度,这两个温度即为该样品的熔点范围。
6、熔点的测定至少要有两次重复的数据,每一次测定都必须用新的熔点管,装新样品。进行第二次测定时,要等浴温冷至其熔点以下约30℃左右再进行
7、使用硫酸作加热浴液(加热介质)要特别小心,不能让有机物碰到浓硫酸,否则使溶液颜色变深,有碍熔点的观察。若出现这种情况,可加人少许硝酸钾晶体共热后使之脱色。采用浓硫酸作热浴,适用于测熔点在220℃以下的样品。若要测熔点在220℃以上的样品可用其它热浴液。
8、测定工作结束,一定要等浴液冷却后方可将浓硫酸倒回瓶中。温度计也要等冷却后,用废纸擦去硫酸方可用水冲洗,否则温度计极易炸裂。
9、除了要校正温度计刻度之外,还要将温度计外露段所引起的误差进行读数的校正,才能够得到正确的熔点。
例: 浴液面在温度的30℃处测定熔点为190℃(t1)则外露段为190℃-30℃=160℃,这样辅助温度计水银球应放在160℃×1/2+30=110℃处。测得t2=65℃,熔点为190℃,则K=0.000159。按照上式则可求出:
Δt=O.000159×160×(l90-65)=3.18≈3.2
所以,校正后的熔点应为190+3.2=193.2℃
1、熔点管必须洁净。如含有灰尘等,能产生4~10℃的误差。
2、熔点管底未封好会产生漏管。
3、样品粉碎要细,填装要实,否则产生空隙,不易传热,造成熔程变大。
4、样品不干燥或含有杂质,会使熔点偏低,熔程变大。
5、样品量太少不便观察,而且熔点偏低;太多会造成熔程变大,熔点偏高。
6、升温速度应慢,让热传导有充分的时间。升温速度过快,熔点偏高。
7、熔点管壁太厚,热传导时间长,会产生熔点偏高。
8、使用硫酸作加热浴液要特别小心,不能让有机物碰到浓硫酸,否则使浴液颜色变深,有碍熔点的观察。若出现这种情况,可加人少许硝酸钾晶体共热后使之脱色。采用浓硫酸作热浴,适用于测熔点在220℃以下的样品。若要测熔点在220℃以上的样品可用其它热浴液。

来源:AnyTesting


