您当前的位置:检测资讯 > 监管召回
嘉峪检测网 2018-06-06 12:20
导读
近日,国家药品监督管理局通报对重庆欣汶医疗器械有限公司、长沙精通医疗器械有限公司、海南泰合医疗科技有限公司这3家医疗器械生产企业的飞行检查结果。
国家药品监督管理局关于重庆欣汶医疗器械有限公司停产整改的通告
(2018年第36号)
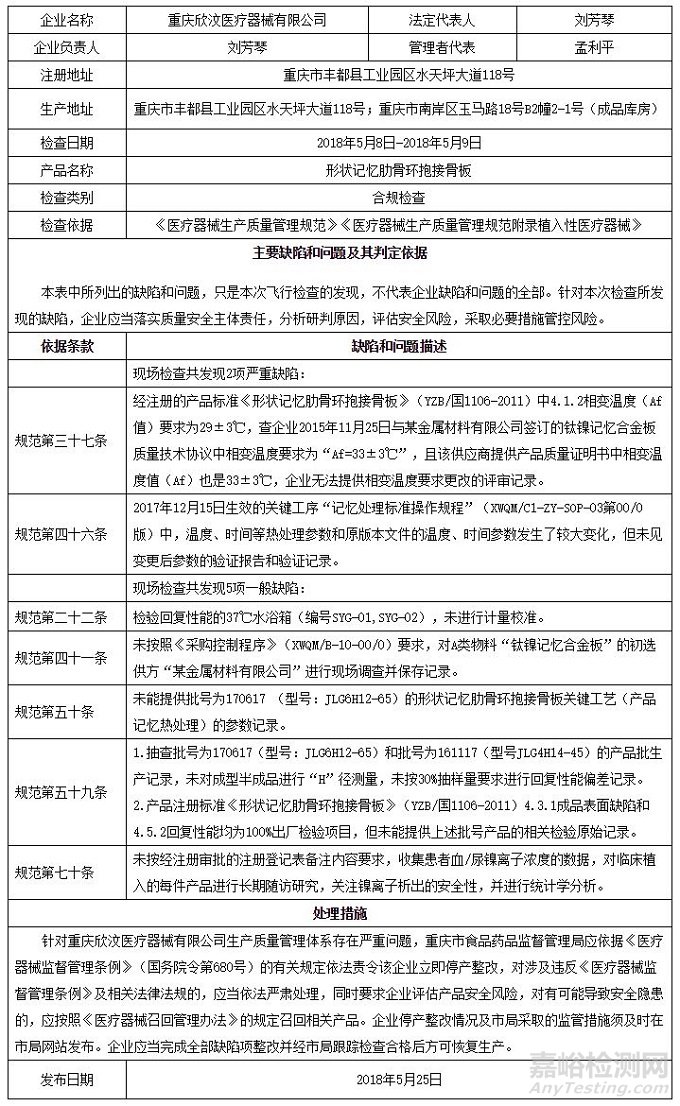
近期,国家药品监督管理局组织对重庆欣汶医疗器械有限公司进行了飞行检查。检查中,发现该企业质量管理体系主要存在以下缺陷:
一、厂房与设施方面
企业检验回复性能的37℃水浴箱(编号SYG-01,SYG-02),未进行计量校准,不符合《医疗器械生产质量管理规范》(以下简称《规范》)中企业应当建立检验仪器和设备的使用记录,记录内容包括使用、校准、维护和维修等情况的要求。
二、设计开发方面
企业经注册的产品标准《形状记忆肋骨环抱接骨板》(YZB/国1106-2011)中4.1.2相变温度(Af值)要求为29±3℃,查企业与某金属材料有限公司签订的钛镍记忆合金板质量技术协议中相变温度要求为“Af=33±3℃”,且该供应商提供产品质量证明书中相变温度值(Af)也是33±3℃,企业无法提供相变温度要求更改的评审记录,不符合《规范》中企业应当对设计和开发的更改进行识别并保持记录。必要时,应当对设计和开发更改进行评审、验证和确认,并在实施前得到批准的要求。
三、采购方面
企业未按照《采购控制程序》(XWQM/B-10-00/0)要求,对A类物料“钛镍记忆合金板”的初选供方“某材料有限公司”进行现场调查并保存记录,不符合《规范》中企业应当建立供应商审核制度,并应当对供应商进行审核评价。必要时,应当进行现场审核的要求。
四、生产管理方面
(一)现场查看企业2017年12月15日生效的关键工序“记忆处理标准操作规程”(XWQM/C1-ZY-SOP-03第00/0版)中,温度、时间等热处理参数和原版本文件的温度、时间参数发生了较大变化,但未见变更后参数的验证报告和验证记录,不符合《规范》中企业应当编制生产工艺规程、作业指导书等,明确关键工序和特殊过程的要求。
(二)企业未能提供批号为170617(型号JLG6H12-65)的形状记忆肋骨环抱接骨板关键工艺(产品记忆热处理)的参数记录,不符合《规范》中每批(台)产品均应当有生产记录,并满足可追溯要求的要求。
五、质量控制方面
抽查产品批号为170617(型号JLG6H12-65)和产品批号为161117(型号JLG4H14-45)的批生产记录,企业未对成型半成品进行“H”径测量,未按30%抽样量要求进行回复性能偏差记录;产品注册标准《形状记忆肋骨环抱接骨板》(YZB/国1106-2011)4.3.1成品表面缺陷和4.5.2回复性能均为100%出厂检验项目,但未能提供上述批号产品的相关检验原始记录,不符合《规范》中每批(台)产品均应当有检验记录,并满足可追溯要求的要求。
六、不良事件监测、分析和改进方面
企业未按经注册审批的注册登记表备注内容要求,收集患者血/尿镍离子浓度的数据,对临床植入的每件产品进行长期随访研究,关注镍离子析出的安全性,并进行统计学分析,不符合《规范》中企业应当建立数据分析程序,收集分析与产品质量、不良事件、顾客反馈和质量管理体系运行有关的数据,验证产品安全性和有效性,并保持相关记录的要求。
企业已对上述其质量管理体系存在的缺陷予以确认。该企业上述行为不符合医疗器械生产质量管理规范相关规定,生产质量管理体系存在严重缺陷,国家药品监督管理局责成重庆市食品药品监督管理局依法责令该企业立即停产整改,对涉及违反《医疗器械监督管理条例》(国务院令第680号)及相关法律法规的,依法严肃处理。同时责成重庆市食品药品监督管理局要求该企业评估产品安全风险,对有可能导致安全隐患的,应按照《医疗器械召回管理办法》(国家食品药品监督管理总局令第29号)的规定,召回相关产品。
待企业完成全部项目整改并经所在地省级食品药品监督管理局跟踪复查合格后方可恢复生产。
附件
国家药品监督管理局关于长沙市精通医疗器械有限公司停产整改的通告
(2018年第37号)
近期,国家药品监督管理局组织对长沙市精通医疗器械有限公司进行了飞行检查。检查中,发现该企业质量管理体系主要存在以下缺陷:
一、厂房与设施方面
(一)企业《定制式固定义齿》产品技术要求规定表面粗糙度Ra小于等于0.025μm,但企业未配置粗糙度分析仪,不符合《医疗器械生产质量管理规范》及相关《附录》(以下简称《规范》)中企业应当配备与产品生产规模、品种、检验要求相适应的检验场所和设施的要求。
(二)企业铸造用氧气瓶、液化气瓶置于氧气室,无排风设施,且与铸造室、纯钛铸造室仅用玻璃隔离,不符合《规范》中易燃、易爆、有毒、有害的物料应当专区存放、标识明显,专人保管和发放的要求。
二、设备方面
企业《包埋作业指导书》(编号CSJT/SOP-04)中规定蜡型包埋时应放在振荡器上,防止内冠气泡,但企业未配备振荡器,不符合《规范》中企业应当配备与所生产产品和规模相匹配的生产设备、工艺装备等,并确保有效运行的要求。
三、设计开发方面
企业胶托钢托组生产区内进行的钢托电解抛光处理,电压设置为16.2V,但《电解机操作和保养规范》(编号CSJT/SB-15)规定电压设置为12V,《铸造作业指导书》(文件编号CSJT/SOP-05)规定,铸圈放入930—950℃的烤箱中进行烧焙,烧焙时间40—45分钟,但《支架(钴铬)包埋料使用说明书》中规定升温至950℃,保温45—60分钟,不符合《规范》中企业应当对设计和开发的更改进行识别并保持记录,必要时,应当对设计和开发更改进行评审、验证和确认,并在实施前得到批准的要求。
四、采购方面
(一)企业主体材料记录中2018年5月5日使用的支架合金注册证号为苏食药监械(准)字2013第2631287号,但现场查见实际使用的钴铬合金注册证号为国械注进20172631496,主体材料记录中未记录2018年5月5日使用的支架合金的批号和有效期信息,不符合《规范》中采购记录应当满足可追溯的要求。
(二)抽查批号分别为4962、4436,收验日期分别为2018年3月30日、2018年3月19日的钴铬合金 SPARTALLOY ALLOY物料检验原始记录,企业未留存金属原材料生产企业出厂检验报告,不符合《规范》中企业应当对采购物品进行检验或者验证,确保满足生产的要求。
五、生产管理方面
企业原材料库中树脂牙产品脱包装后,多批次混放在一个抽屉中,难以区分不同批次树脂牙生产批号,不符合《规范》中企业应当建立产品的可追溯程序,规定产品追溯范围、程度、标识和必要的记录的要求。
六、销售和售后服务方面
企业未提供牙模单号2018P0583、牙模单号2018D05134、牙模单号2018A05165的医疗机构资质证明文件,不符合《规范》中应当选择具有合法资质的医疗机构,保存医疗机构执业资质证明文件,并建立档案的要求。
七、不良事件监测、分析和改进方面
企业未提供上一年度《医疗器械不良事件年度汇总报告表》,不符合《规范》中企业应当按照有关法规的要求建立医疗器械不良事件监测制度,开展不良事件监测和再评价工作,并保持相关记录的要求。
企业已对上述其质量管理体系存在的缺陷予以确认。该企业上述行为不符合医疗器械生产质量管理规范相关规定,生产质量管理体系存在严重缺陷,国家药品监督管理局责成长沙市精通医疗器械有限公司依法责令该企业立即停产整改,对涉及违反《医疗器械监督管理条例》(国务院令第680号)及相关法律法规的,依法严肃处理。同时责成湖南省食品药品监督管理局要求该企业评估产品安全风险,对有可能导致安全隐患的,应按照《医疗器械召回管理办法》(国家食品药品监督管理总局令第29号)的规定,召回相关产品。
待企业完成全部项目整改并经所在地省级食品药品监督管理局跟踪复查合格后方可恢复生产。
附件

国家药品监督管理局关于海南泰合医疗科技有限公司停产整改的通告
(2018年第38号)
近期,国家药品监督管理局组织对海南泰合医疗科技有限公司进行了飞行检查。检查中,发现该企业质量管理体系主要存在以下缺陷:
一、机构与人员方面
企业管理者代表为产品检验报告的复核人,未经过与其岗位要求相适应的培训,不符合《医疗器械生产质量管理规范》及相关《附录》(以下简称《规范》)中从事影响产品质量工作的人员,应当经过与其岗位要求相适应的培训,具有相关理论知识和实际操作技能的要求。
二、厂房与设施方面
企业医疗器械生产区内与另一食品生产区共用人流物流走廊,不符合《规范》中厂房与设施应当符合生产要求,生产、行政和辅助区的总体布局应当合理,不得互相妨碍的要求。
三、采购方面
现场发现企业产品的主机面壳无购进记录,探头线、遥控器线等供应商档案中缺少资质证明文件,不符合《规范》中应当建立采购记录,包括采购合同、原材料清单、供应商资质证明文件、质量标准、检验报告及验收标准等,采购记录应当满足可追溯的要求。
四、生产管理方面
(一)企业生产工序二的某工作人员工作量记录(2018年4月至5月)中反映的生产行为,无对应的批生产记录,不符合《规范》中每批(台)产品均应当有生产记录,并满足可追溯的要求。
(二)企业产品出厂检验报告(批号170329编号170329-001)中的检验项目与产品出厂检验规程不一致,缺少检验规程中“工作情况检验”5.1的检验项目,不符合《规范》中企业应当根据强制性标准以及经注册或者备案的产品技术要求制定产品的检验规程,并出具相应的检验报告或者证书的要求。
五、不合格品控制方面
企业未能提供对WSJ-B型旋磁式糖尿病治疗仪不合格产品(批号150330)采取相应处置措施的记录,不符合《规范》中企业应当对不合格品进行标识、记录、隔离、评审,根据评审结果,对不合格品采取相应的处置措施的要求。
企业已对上述其质量管理体系存在的缺陷予以确认。该企业上述行为不符合医疗器械生产质量管理规范相关规定,生产质量管理体系存在严重缺陷,国家药品监督管理局责成海南泰合医疗科技有限公司依法责令该企业立即停产整改,对涉及违反《医疗器械监督管理条例》(国务院令第680号)及相关法律法规的,依法严肃处理。同时责成海南省食品药品监督管理局要求该企业评估产品安全风险,对有可能导致安全隐患的,应按照《医疗器械召回管理办法》(国家食品药品监督管理总局令第29号)的规定,召回相关产品。
待企业完成全部项目整改并经所在地省级食品药品监督管理局跟踪复查合格后方可恢复生产。
附件


来源:AnyTesting