您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2018-07-11 10:37
介绍
在2009年,据Tamilvanan学者的统计,有接近50%的新型药物在水中溶解度较低,导致药物生物利用度差和控制释放难题。为了解决这些困难,研发人员将脂质分散体系作为载体系统使用,如脂质乳剂、脂质体。在2008年的一篇研究中,学者Porter将流感活疫苗亲脂性药物分散在乳剂中,发现乳液药物产生了更高的生物利用度,吸引了大量学者的特别关注。
亚微乳剂是一种特别有趣的药物输送系统,由于其生物相容性,生物降解性、易于大规模制备,大的表面积,和经证实的稳定能力,能够在一定时间内避免上浮和沉淀现象(Tamilvanan,2004)。
传统上,磷脂被用作亚微乳剂的表面活性剂,用于药物运输。然而,口服的磷脂基稳定的乳液会很快的被十二指肠中的胆汁盐所替代(Torcello-Gómez et al., 2011),造成破乳。另外,如果这些乳剂由静脉注射进入体内,根据胶体异物特性的不同,乳液将很快被单核吞噬细胞系统(MPS)消除。在这两种情况下,使用磷脂作为唯一的表面活性剂我们无法控制药物的代谢和降解过程。所以,空间的聚合物非离子表面活性剂(PEO和PEG)被用于解决乳剂在口服和注射应用的问题。然而,对于这些表面活性剂是如何影响脂质载体系统的代谢过程的,依然缺乏了解。
静态多重光散射技术(S-MLS)不仅可以测定乳剂的不稳定现象,也可以测试药物制剂的降解过程。在本文中,使用Turbiscan多重光散射仪研究了乳液在模拟体内条件下的稳定性。
方法
材料
四种聚合物非离子表面活性剂
Sigma–Aldrich试剂公司的葵花籽油
葵花籽油浓度25%,表面活性剂加量1%
两种测试条件
胃条件
十二指肠条件
测试方法
将配置好的乳液分别与胃液体和十二指肠液体混合,模拟体内条件。
将配置好的样品装入Turbiscan多重光散射仪进行测试。
结果与讨论
在胃条件下
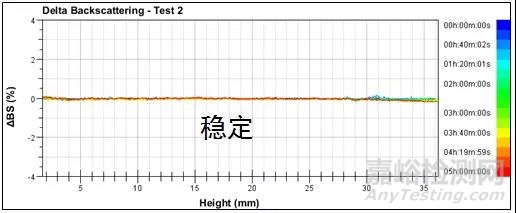
图1 乳液在胃条件下的背散射光图谱
Turbiscan多重光散射仪数据显示,乳液在胃条件下,2h之内背散射光强度基本没有变化(ΔBS<0.3%),说明乳液在胃条件下可以保持稳定,没有絮凝和聚并现象,四种表面活性剂配制的乳液稳定性类似。这一结果与DLS测试的结果相对应,说明2h之内液滴粒径没有变化。因此,可以确定油滴可以保护这些药物在严酷的胃条件下不被溶解,从而直达十二指肠被有效地吸收。
在十二指肠条件下
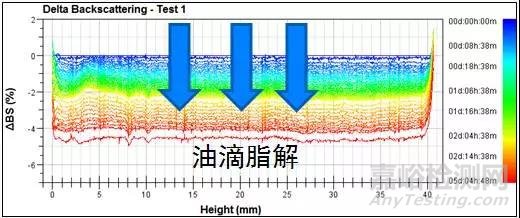
图2 乳液在十二指肠条件下的背散射光图谱
不同于胃条件,十二指肠中含有的脂肪酶可以将脂肪分解,在此条件下,乳液液滴会被逐渐分解。从图中可见,随着时间增加背散射光曲线出现整体的下降,说明乳液在十二指肠条件下乳液液滴开始出现脂解,药物开始从液滴中被释放出来。
脂解过程研究
为了对比4种不同表面活性剂形成乳剂的脂解速度和过程,绘制样品的散射光强度随时间的变化曲线:
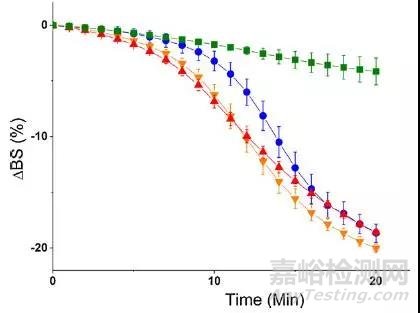
图3 不同表面活性剂乳液在十二指肠条件下的背散射光变化曲线
四种表面活性剂由于分子结构中PEO链段长度的不同,脂解得速度也不尽相同。F127含有100个PEO链段,分解速度最为缓慢。M52仅具有40个PEO链段,分解速度最快,而F68具有75个PEO链段,分解速度居中。但是M52表面活性剂的结果就比较复杂了,M52同样具有100个PEO链段,但是分解速度却依然很快。这个现象不禁让我们想到:聚合物非离子表面活性剂的分解机理,不仅仅只受到链段长短的影响,同样与表面活性剂在界面上构筑的方式有关。
据前人研究,一个M52分子在界面上形成的覆盖面积在0.4 至 1.2 nm2/molecule之间,而F68在3 and 3.4 nm2/molecule之间,而F127的覆盖面积在 6.5–7.21nm2/molecule之间,暂无人报道M59在界面上的覆盖面积。
为了研究活性剂的主导作用,将不同比例的F68和F127复配,发现仅仅1/4的F127与F68复配就可以达到与全部F127一样的脂解速度。这说明长链的F127在脂解过程中对界面的分解起着重要的主导作用。
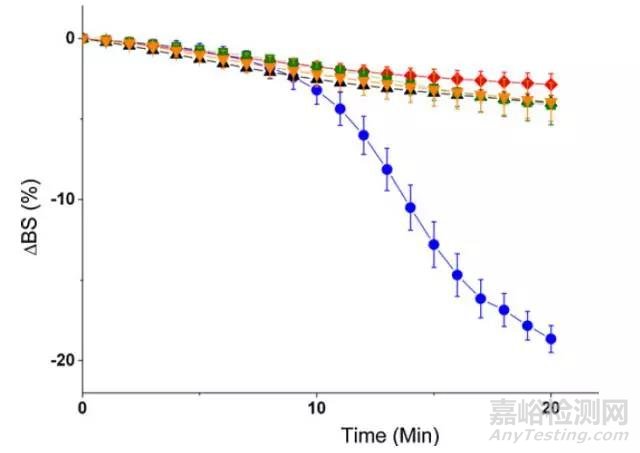
图4 表面活性剂复配乳液在十二指肠条件下的背散射光变化曲线
结论
在本文中,我们研究了聚合物非离子表面活性剂对体内脂解过程的作用。通过模拟胃环境和十二指肠环境的测试,得知只要乳液稳定,药物运输过程就不会出现大的问题。
通过Turbiscan多重光散射仪研究药物制剂的脂解过程,我们得知乳液液滴脂解的速度不仅与活性剂链段长度有关,也与活性剂的构筑方式相关。由此我们可以控制药物在十二指肠中的释放过程,例如,添加长分子链段的表面活性剂。另外,我们发现复配表面活性剂比例可以改变乳液在体内环境的脂解速度。这些研究结果给我们对于亚微米乳液的控制-释放的合理设计具有重要意义。

来源: 朗迪森科技


