您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2018-09-28 14:50
三磷酸腺苷(adenosine triphosphate,ATP)是一种以次黄嘌呤核苷酸为底物,经生物发酵技术制得的一种高能化合物,是生物体内组织细胞一切生命活动所需能量的直接来源,被誉为细胞内能量的“分子通货”,能够储存和传递化学能,参与体内蛋白质、脂肪、糖和核酸的代谢[1-2].ATP作为最重要的能量分子在细胞的各种生理、病理过程中起着重要作用,可以作为细胞活性的一个重要标志物.ATP也常作为检测微生物污染的一个指标[3-4],通过检测ATP含量,可以检测食品、水、药品、化妆品等的微生物污染情况,通过监测活细胞线粒体内ATP含量的变化,可以预测各种药物、生物制剂或生物活性物质引起的细胞杀伤、细胞抑制和细胞增殖作用.
目前文献报导检测ATP的方法主要有纸层析法[5-6],电化学传感器法[7-8],离子交换色谱[9],高效液相色谱[10-11],分光光度法[12-15],生物发光法[16-17]和基于核酸适体的方法[18-21]等.这些方法中有的操作比较繁琐,耗时较长,制备过程复杂,如纸层析法和电化学传感器法;有的对仪器设备要求高,且需要特定的酶,如高效液相色谱法和生物发光法;有的精度低,如离子交换色谱法.因此,探索新的、灵敏度高的、快速便捷的检测方法对于检测ATP在食品、药品、环境水样中的微生物污染情况等具有十分重要的意义.
二级散射(second-order scattering,SOS)作为一种新发展起来的分析技术,因其灵敏度高,简单便捷的优点引起人们的关注[22-23],并在金属离子[24]、表面活性剂[25]、蛋白质[26]、核酸[27]、药物[28]及环境样品[29]的检测中得到广泛应用.本课题组在研究中发现,在中性条件下,双核铀酰配合物(binuclear uranyl-isophthalaldehyde-tetrapyrrole,BUIPTP)与ATP能形成一种配合物体系,对体系进行光谱性能测试,发现在体系激发波长的二倍处出现一个强峰,激发波长位于566 nm处,在最大激发波长处,体系的SOS强度随着ATP的浓度的增加存在这线性关系,可用于痕量分析,且该方法具有较高的灵敏度,检出限为0.75 nmol/L,其灵敏度较常见的检测ATP的方法要大大的提高.研究双核铀酰配合物(BUIPTP)与ATP的配位反应对二级散射强度的影响,并对反应条件进行一系列的优化,得出的结果让人满意.
仪器:UV-3900紫外-可见分光光度计(日本日立),IR Prestige-21傅立叶变换红外光谱仪(日本岛津公司),Hitachi-F7000荧光分光光度计(日本日立公司),IKA-MAGHS7恒温加热磁力搅拌器(广州仪科实验室技术有限公司),DZF-6020真空干燥箱(上海三发科学仪器有限公司),pHs-10C数字酸度计(上海雷磁科学仪器厂),电子分析天平(瑞士梅特勒-托利多仪器有限公司).
试剂:IPTP是实验室自制,六水合硝酸铀酰是购买于湖北楚盛威化工有限公司,三磷酸腺苷(ATP)购买于上海Aladdin化学试剂有限公司.
利用铀酰与双极双齿配体(isophthala ldehyde-tetrapyrrole,IPTP)反应合成了双核铀酰配合物(见图1).合成步骤如下:IPTP参照文献[30] 的方法合成;将IPTP(0.366 0 g,1.0 mmol)和六水合硝酸铀酰(0.502 0 g,1.0 mmol)溶解在100 mL体积比为3∶1的无水乙醇与水溶液中,将混合物室温下用磁子搅拌10 h使其发生螯合反应.将溶剂减压除去,得到的固体用无水乙醇洗涤数次,然后用柱层析进行提纯,所得产物即为纯的BUIPTP.
用分析天平准确称量BUIPTP固体0.740 0 g,经二次蒸馏水溶解,转移至100 mL容量瓶,加水定容至刻度线,摇匀,即得10 μmol/L的BUIPTP溶液.
在10 mL比色管中加入500 μL的ATP标准溶液或样品溶液与200 μL 的Tris-Hcl缓冲液(pH 7).在搅拌下将100 μL 10 μmol/L 的BUIPTP溶液滴加到上述溶液中,总滴加时间为10 min,将该溶液孵育30 min.在激发波长283 nm,发射波长566 nm处用荧光分光光度计测定该体系的二级散射光谱.在566 nm波长处绘制二级散射光强度对ATP浓度的标准曲线.在相同的实验条件下,进行腺苷和其它三种磷酸核苷酸的平行实验.ATP与BUIPTP反应以及检测ATP的过程示意图见图1.
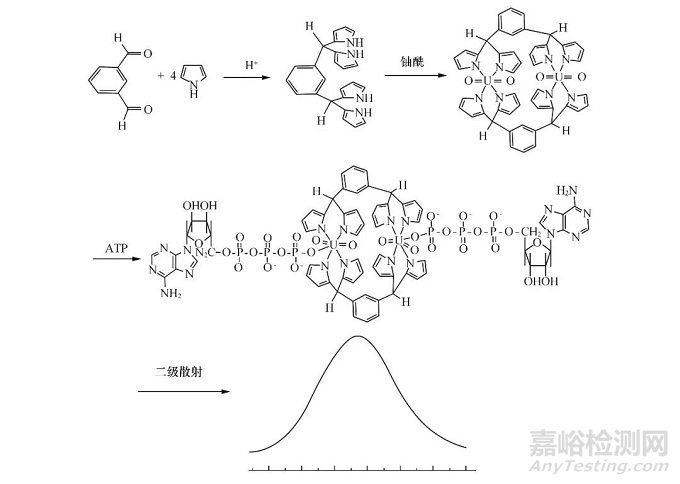
图1 ATP与BUIPTP反应和检测ATP的过程示意图
Fig.1 The reaction of ATP with BUIPTP and the illustrated procedure of ATP detection
图2为BUIPTP与不同浓度的ATP溶液的二级散射光谱图.当体系中不存在ATP时,溶液的二级散射强度较弱.当加入ATP溶液后,体系的二级散射强度增强.因为ATP与BUIPTP形成大的空间体积,使得二级散射强度增强.在最佳条件下,BUIPTP-ATP体系二级散射增加的强度与一定范围的ATP浓度呈现线性关系.因此,可以利用由ATP和BUIPTP引起的反应来建立二级散射光谱法检测ATP.选定在566 nm处检测ATP的二级散射光强度.
我们首先研究了溶液的酸度对体系二级散射强度的影响.由图3可看出,随着pH值增大,二级散射强度出现先增强而后降低现象.pH为7时,体系的二级散射强度最大.结果显示,在中性介质中该反应的效果是最好的.究其原因可能是在强酸性介质中ATP的氨基质子化,导致ATP与BUIPTP结合的亲和力减弱.当pH值高于7.0时,溶液中的氢氧根离子会与ATP竞争结合BUIPTP.因此,采用pH 7的Tris-HCl缓冲溶液.
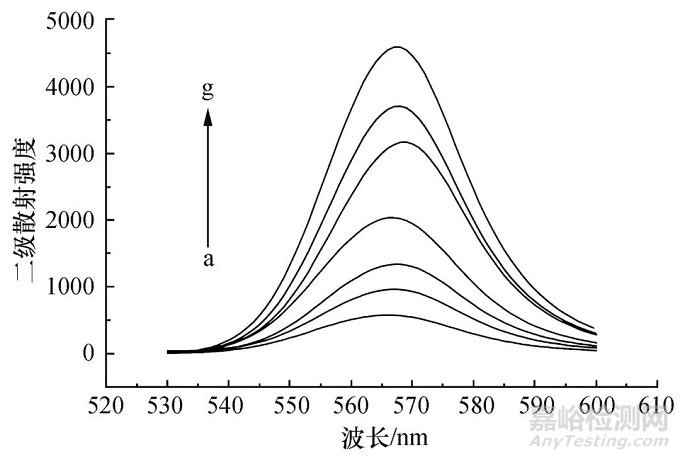
ATP的浓度为:a-g:0,50,100,200,300,400,500 nmol/L
图2 溶液的二级散射光谱图
Fig.2 The second-order scattering of ATP and BUIPTP system
按照实验方法测定了体系在 0~50 min内,考察反应时间对体系二级散射强度的影响,结果显示:反应在达到30 min后二级散射强度即达到最大,并在30~50 min内几乎保持不变(如图4).本实验选择反应30 min后测定.
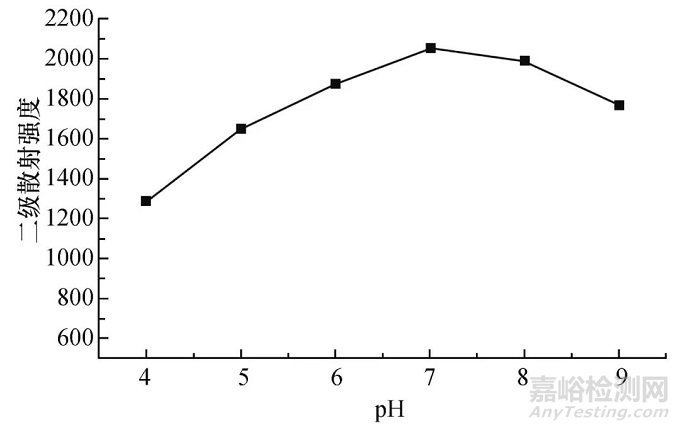
图3 pH对二级散射强度的影响
Fig.3 Effect of pH on the second-order scattering
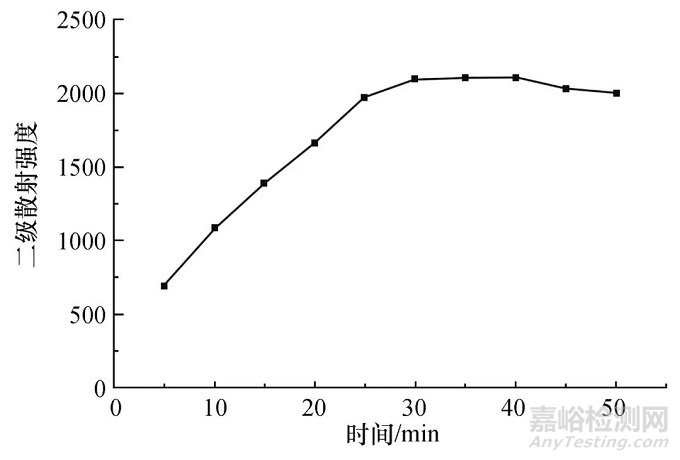
图4 反应时间对二级散射强度的影响
Fig.4 Effect of reaction time on the second-
order scattering
测试了ATP和BUIPTP加入顺序的影响.结果表明,将BUIPTP滴加到ATP溶液时的二级散射信号比ATP滴加到BUIPTP溶液时的更强.可能是因为BUIPTP滴加到ATP溶液中时,BUIPTP与ATP的反应物质的量之比为1∶2.但是将ATP滴加到BUIPTP溶液时,BUIPTP与ATP以物质的量之比为1∶2和1∶1同时进行反应,这使得二级散射信号稍微较弱.所以本研究选择将BUIPTP滴加到ATP溶液.
在最优实验条件下,对不同浓度ATP的二级散射强度进行了测定,并作出了校正曲线.如图5,该标准曲线表明,ATP浓度在2.5~500 nmol/L范围内,二级散射强度(ISOS)与ATP浓度(c)之间具有良好的线性关系.线性回归方程为:ΔISOS=548+7.98c (nmol/L),相关系数r= 0.999 1.平行测定11份空白溶液,根据检出限公式FLOD=3Sb/m(Sb为空白标准偏差,m为工作曲线的斜率),检出限为0.75 nmol/L.分别对ATP浓度为100 nmol/L和300 nmol/L两组待测液进行六次平行测定,相对标准偏差分别为2.56%和2.03%.
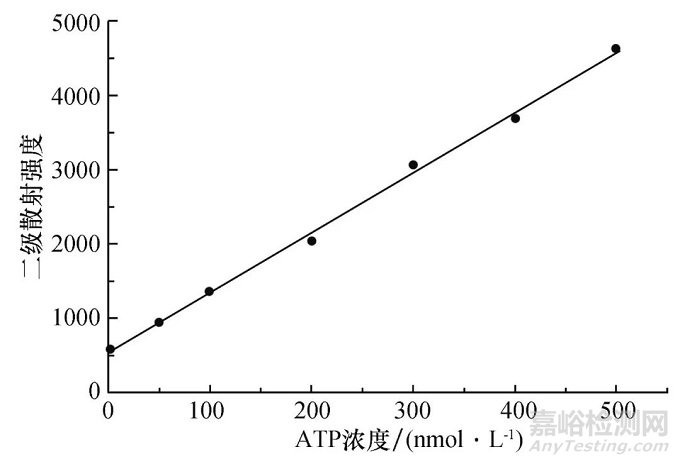
图5 测定ATP的校准曲线
Fig.5 Calibration curve for the determination of ATP
为了研究实验的选择性,我们使用单独的三磷酸腺苷(ATP)和单独的磷酸根进行比较(见图6).
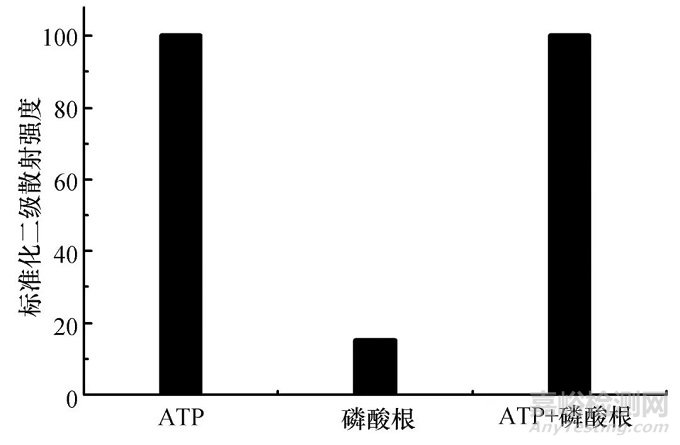
图6 含有相同的浓度的ATP、磷酸根、ATP和
磷酸根共存的BUIPTP溶液的
标准化二级散射强度
Fig.6 Normalized second-order scattering intensity of BUIPTP solution containing the same concentration of ATP, phosphate, and ATP and phosphate coexistence
结果表明,当浓度相同时,单独存在ATP时的IRLS值比单独的磷酸根存在时的IRLS值高,并且当ATP与磷酸根共存时与单独存在ATP时的IRLS值大致相同.说明该方法对ATP具有很好的选择性,进一步证明BUIPTP中的铀酰能特异性地结合ATP中的磷酸基团和腺苷.
在选定条件下,我们对体系进行了共存物质影响的干扰情况研究.结果见表1,表中所列的相对误差在±5%的范围内,基本对ATP的测定无干扰.
表1 共存物质的影响
Table 1 The impact of coexisting substances

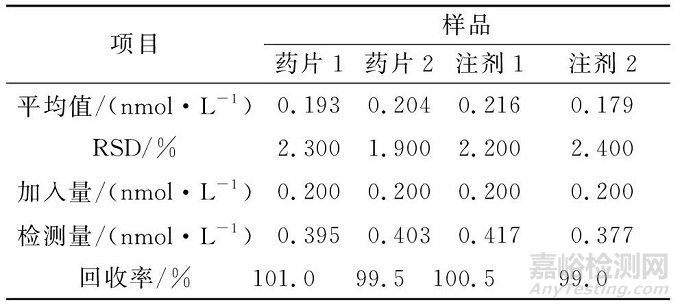
使用该法对实际注射药剂样品中的ATP和药片中的ATP含量进行了测定.使用二次蒸馏水稀释ATP注射液到合适的浓度.将ATP药片研磨成粉末,用分析天平精确称取一定量的粉末后用二次蒸馏水稀释至所需浓度.按照以上实验步骤对稀释后的样品中的ATP进行测定.为了评估该方法的实用性和可靠性,本研究进行了标准浓度的ATP回收实验.由表2可知,样品平行测定的RSD都低于2.5%,回收率在99.0%~101.0%范围内(n=6).结果表明,该研究方法可以成功应用于实际样品中ATP的检测,并且具有较好的回收率.
表2 实际样品分析(n=6)
Table 2 Analysis of real samples(n=6)
在本实验研究中,建立了一种新的二级散射法不经分离直接检测ATP.该方法是基于ATP和BUIPTP反应生成的配合物而引起二级散射增强这一原理建立的.该分析方法具有简单方便、灵敏度高、亲和力高、对ATP的特异性以及不经过分离操作过程等优点.该方法可为其他类似目标分析物如CTP、GTP等的检测提供一种新的思路,并且在生物化学、医学、环境学等领域具有重要的潜在应用价值.

来源:南华大学学报自然科学版


