您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2019-02-11 10:56
欧洲
欧盟消费者安全科学委员会(SCCS)发布关于化妆品中水杨酸的意见 (2019.01.03)
0SCCS已采纳关于化妆品中水杨酸的最终意见,总结认为:水杨酸在化妆品中用作防腐剂且浓度不超过0.5%的情况下是安全的,但不适用于喷雾类和口腔类产品,唇膏除外。还认为,水杨酸在冲洗类和其他类别化妆品中用作其他用途且浓度分别不超过3%和2%的情况下是安全的。在部分产品中,如身体乳、眼霜、睫毛膏、眼线笔、口红等,水杨酸仅用作防腐剂且满足一定浓度限值是安全的。
欧盟化妆品法规附录III第98款规定:

欧盟化妆品法规附录V第3款规定:

欧盟向WTO通报化妆品标签决议草案 (2019.01.02)
欧洲委员会已向WTO通报了一项决定草案,该草案旨在建立用于化妆品标签的常用成分名称词汇表。
该词汇表将成为化妆品产品法规的一部分,旨在:确保统一标签; 和便于识别化妆品成分。
拟议的通过日期是2019年第一季度。它将在欧盟官方公报发布20天后生效。
评论截止日期为通知后60天。
去年10月,欧盟执行委员向世界贸易组织通报了化妆品法规修正草案,以限制使用氯苯咪唑作为防腐剂。
SCCS征求两种化妆品成分安全性的公众意见 (2019.01.02)
欧盟委员会消费者安全科学委员会(SCCS)已就两种化妆品成分发表了初步意见,征求公众意见,意见征询截止日期为3月5日。。两种物质分别是:
关于羟乙氧基苯基丁酮(HEPB) - 认为该物质因对眼部有刺激性,在冲洗类、口腔护理和停留类化妆品中用作化妆品防腐剂,其最大安全浓度为0.7%;
关于2-甲氧基 - 甲基 - 对苯二胺及其硫酸盐(A160) - 认为,该物质在氧化睫毛产品中使用,最大使用浓度为1.8%的情况下是安全的。
与此同时,委员会的DG Grow已要求委员会就过敏警报测试(AAT)的适用性提出意见,以便在外行人使用时提供指示染发剂过敏反应的信号 - 如果按照所列条件应用 - 如果它对测试有任何进一步的科学关注。
决定的截止日期是2019年6月。
消费者组织呼吁欧盟关于电子标签香精过敏原的建议“不公平” (2019.01.03)
欧洲消费者组织Beuc对使用电子标签提高消费者对化妆品中香味过敏原的认识的想法表示担忧。该组织认为这一想法是有缺陷的,这种方法对寻找化妆品的忙碌购物者提出了“不公平和不切实际”的期望。
然而,业界团体表示支持使用电子标签。这是委员会一直在考虑的一个选择,因为其一个科学委员会建议采取措施提高透明度。其他是:没有欧盟行动;更大的包装标签。
例外
化妆品法规要求公司在产品标签上全成分标示。然而,香料化合物被列为使用术语“香精”或“香料”。然而,已知引起过敏反应的26种香料化合物除外,必须将其过敏原成分单独列出。
监管挑战
化妆品中的香精过敏原对监管机构来说是一个不寻常的挑战,因为它们与两种不良事件相关:致敏和过敏反应。
致敏是过敏反应的先决条件,意味着后者仅发生在致敏的个体中。此外,过敏反应所需的暴露水平通常远低于致敏所需的暴露水平。
委员会正在准备5月进行公众咨询的影响评估。
6种高度关注物质被列入REACH候选物质清单 (2019.01.17)
目前高度关注物质(SVHC)候选清单中含有197种物质。
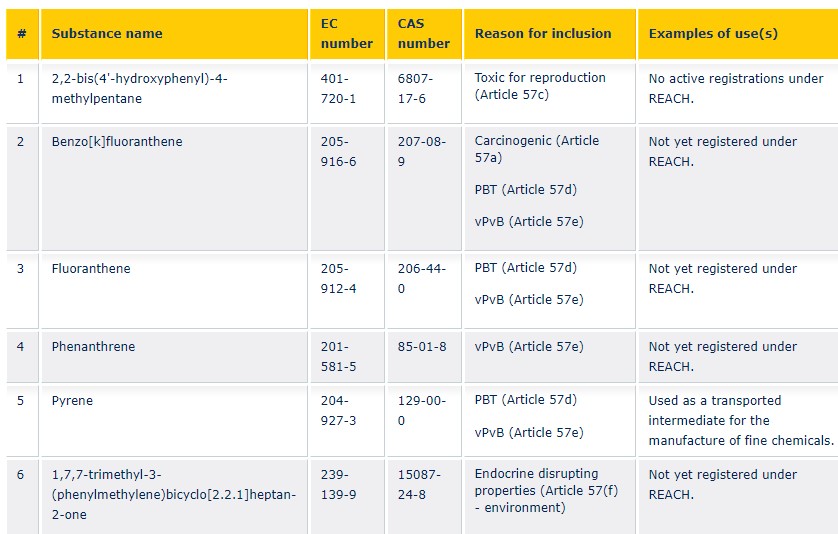
2019年1月15日, 由于这些物质具有致癌性、生殖毒性、持久性、生物累积性和毒性(PBT)以及非常持久且具有生物累积性(vPvB)的特性, ECHA已在候选清单中添加了5种新物质。
在成员国委员会(MSC)的参与下,决定包括四种多环芳烃(PAHs)。四个PAH病例被转介到MSC,以便处理在公众咨询期间提交的新的危害信息。
该名单中还增加了一种物质,由于其内分泌干扰特性,欧盟委员会已将其确定为SVHC。委员会的决定是在2016年提交MSC对此SVHC提案的意见之后做出的。
2019年1月15日授权候选清单中包含的物质及其SVHC特性请见下表:
美洲
美国参议员要求强生公司提供有关滑石粉的信息(2019.01.31)
参议员Patty Murray(D-Washington)已致函强生公司首席执行官Alex Gorsky,要求提供有关该公司关于其含滑石粉产品的安全记录的信息。
她还要求公司与美国食品和药物管理局(FDA)通信。
该请求发布之际,跨国公司面临着多个州正在进行的诉讼,指控其滑石粉婴儿爽身粉产品含有致癌物质石棉,或者导致原告发展卵巢癌。
强生继续坚持认为其产品是安全的。
加拿大提议修订化妆品禁限用物质清单(2019.01.29)
加拿大卫生部已就其化妆品禁限用物质清单中的物质现状提出了一些改变。
在1月23日向利益相关者发出的通知中,政府部门表示正在考虑的提案包括对名单上几个现有条目的条件的变化。这些物质会将一些物质从禁止物种重新分类为限制物种,而其他物质则会被禁止使用。
正在审查的物质是:
加拿大化妆品禁限用物质清单已于2018年9月进行更新,该物质清单并不是一成不变的,会根据实际需要进行更新。
该公告还指出,关于滑石粉的化妆品热点清单审查和咨询将与CMP对该物质的评估一起进行。
非洲
卢旺达90%以上的化妆品中都含有有害物质 (2019.01.29)
卢旺达已查获4,501种化妆品产品,作为其执行禁止销售含有危险亮肤剂的禁令的一部分。
去年11月至12月期间进行检查的卢旺达标准委员会发现,在51个品牌中,只有4个符合汞和对苯二酚的法律要求。
亮肤产品会破坏皮肤细胞中色素黑色素的产生。它们通常包含汞,可能会损害皮肤、眼睛、肺部、肾脏以及消化系统、免疫系统和神经系统。
对苯二酚是另一种常用添加成分,根据化妆品法规在欧盟禁用。检查还发现了产品中的砷和铅。在卢旺达,化妆品中下列物质的法定限制是:
卢旺达标准委员会发言人Simeon Kwizera告诉Chemical Watch,检查员不仅针对标有“皮肤美白”的产品,而且还提供含有可以减轻皮肤光泽的化妆品的“各种各样”产品。
检查员检查了产品标签上的成分,然后在实验室检测了那些带有“误导性成分”或“混淆信息”的成分。
他补充说,检查的对象是“所有品牌和所有进口产品”。这些包括身体油、霜、乳液等以及美容香皂和其他。。
卢旺达标准委员会,卫生部和卢旺达食品和药品管理局共同进行了检查。
这些检查是三个机构为打击美白化妆品而开展的更广泛活动的一部分,该活动于2013年开始,2015年向贸易商和公众传达了部长命令。
去年12月,卢旺达标准委员会发布了关于氢醌影响的警告,并告知人们该物质可能的替代名称。
一个月前,卢旺达总统保罗卡加梅通过他的推特账号呼吁采取行动对抗皮肤增白剂。
卢旺达是最新禁止使用亮肤霜或使用汞和氢醌的非洲国家。
2015年,象牙海岸禁止所有皮肤增白剂,其次是肯尼亚。2016年,肯尼亚设定了对苯二酚的限量。加纳一年后禁止某些皮肤美白产品,包括对苯二酚。
根据世界卫生组织(WHO)的统计数据,在2011年尼日利亚的一项调查中,77%的女性表示他们经常使用美白产品。世界卫生组织发现,在马里,塞内加尔,南非和多哥,至少有四分之一的受访女性表示他们定期使用它们。
根据非政府组织联盟最近的一项研究,在非洲之外,这些产品的使用在中东和亚洲也很“普遍”,而且它们的需求也在急剧上升。
去年8月,英国的贸易标准官员在全国范围的调查中发现了一种含有10.8%的对苯二酚的亮肤产品。
亚洲
化妆品监督管理常见问题解答(一)(2019.01.10)
为进一步规范化妆品监督管理工作,引导消费者科学理性消费,国家药监局化妆品监管司整理了化妆品监督管理中常见问题,并依据我国现行化妆品法规规定和有关技术规范,逐一进行了解答。具体如下:
问:为何经常听说国外有所谓的“药妆品”,而我国化妆品法规中并没有“药妆品”的概念?
答:需要明确指出的是,不但是我国,世界大多数的国家在法规层面均不存在“药妆品”的概念。避免化妆品和药品概念的混淆,是世界各国(地区)化妆品监管部门的普遍共识。部分国家的药品或医药部外品类别中,有些产品同时具有化妆品的使用目的,但这类产品应符合药品或医药部外品的监管法规要求,不存在单纯依照化妆品管理的“药妆品”。
我国现行《化妆品卫生监督条例》中第十二条、第十四条规定,化妆品标签、小包装或者说明书上不得注有适应症,不得宣传疗效,不得使用医疗术语,广告宣传中不得宣传医疗作用。对于以化妆品名义注册或备案的产品,宣称“药妆”“医学护肤品”等“药妆品”概念的,属于违法行为。
问:寡肽-1和表皮生长因子(EGF)有何区别?EGF可否作为化妆品原料使用?
答:寡肽-1和人寡肽1(表皮生长因子,EGF)非同一种物质。寡肽-1为甘氨酸、组氨酸和赖氨酸等3种氨基酸组成的合成肽。而人寡肽-1又名表皮生长因子(Epidermal Growth Factor, EGF),是由53个氨基酸组成的 “53肽”,分子量为6200道尔顿单位。
寡肽-1收录于我国《已使用化妆品原料名称目录》(2015年版),一般作为皮肤调理剂使用。而人寡肽-1未被收录于该目录,一般在医学领域使用较多,临床适应症为外用治疗烧伤、创伤及外科伤口愈合,加速移植的表皮生长。由于分子量较大,EGF在正常皮肤屏障条件下较难被吸收,一旦皮肤屏障功能不全,可能会引发其它潜在安全性问题。基于有效性及安全性方面的考虑,EGF不得作为化妆品原料使用。
综上,不同于寡肽-1,人寡肽-1(EGF)不得作为化妆品原料使用。在配方中添加或者产品宣称含有人寡肽-1或EGF的,均属于违法产品。
问:化妆品原料中添加的如稳定剂等保护原料的成分,是否应当在产品标签上进行标注?
答:根据国家标准《消费品使用说明 化妆品通用标签》(GB5296.3-2008),化妆品销售包装的可视面上应真实地标注化妆品全部成分的名称。
化妆品成分是指生产过程中有目的地添加到产品配方中,并在最终产品中起到一定作用的成分。为了保证化妆品原料质量而在原料中添加的微量稳定剂、防腐剂、抗氧剂等成分,虽然在产品配方中应当进行填报,但不属于化妆品成分的范畴,可以不在产品标签上进行标注。
问:进口非特殊用途化妆品备案境内责任人与原行政许可在华申报责任单位有何区别?
答:进口非特殊用途化妆品备案境内责任人与原行政许可在华申报责任单位主要有以下两点区别:
问:进口非特殊用途化妆品备案境内责任人如何变更?
答:境外化妆品企业根据需要,可以变更境内责任人及其授权产品范围。变更境内责任人的,新的境内责任人应当按要求进行网上备案系统的用户名称注册;仅变更授权产品范围的,境内责任人应当通过网上备案平台重新上传授权书。
变更境内责任人涉及已备案产品的,变更前后的境内责任人应就前期已经进口和销售的产品责任归属问题协商一致后,由拟变更后的境内责任人通过网上备案系统平台提出变更,同时提交原境内责任人签署的知情同意书,变更经原境内责任人通过网上备案系统平台进行确认后完成。
问:全面实施备案管理之前申报行政许可未获批准的进口非特殊用途化妆品,后续可否进行备案?
答:2018年11月10日前已受理进口非特殊用途化妆品行政许可未获批准的产品,不批准理由涉及产品安全性原因的,后续不得办理备案;不涉及安全性原因的,后续可以由境内责任人办理备案。备案时应当同时提交《不批准决定书》并说明重新申报的理由。原行政许可申报资料中的产品检验报告、安全性评估资料以及相关证明性文件等可作为备案资料提交,相关资料原件已随原行政许可申请提交无法获取的,可提供复印件并加盖境内责任人的公章,同时提交相关情况说明。
关于72批次化妆品不合格及1批次假冒产品的通告(2019.01.31)
经湖北省药品监督检验研究院等检验,标示为中山佳丽日用化妆品有限公司等38家企业生产的72批次化妆品不合格(不合格清单详情请见链接附件)。
上述不合格产品及相关企业违反了《化妆品卫生监督条例》《化妆品标识管理规定》等相关法规的规定。国家药品监督管理局要求广东、上海、福建、北京、江苏、浙江省(市)药品监管部门核实后依法督促相关生产企业对已上市销售相关产品及时采取召回等措施,立案调查,依法严肃处理;要求安徽、北京、福建、甘肃、广东、西藏、海南、河北、河南、湖北、湖南、江苏、江西、宁夏、青海、山东、山西、天津、新疆、云南、浙江省(区、市)药品监管部门责令相关经营单位立即采取下架等措施控制风险,对涉嫌假冒的产品,要深查深究其进货渠道,对违法违规行为,依法予以查处,涉嫌犯罪的依法移交公安机关。上述省级药品监管部门自通告发布之日起3个月内公开对相关企业或单位的处理结果,相关情况及时在国家化妆品抽检信息系统中填报并报告国家药品监督管理局。
《关于26批次化妆品不合格的通告》(2018年第88号)中所列的不合格产品“怡思丁多维光护清透无感防晒喷雾SPF50+”(见附件2),经核实,为假冒产品。各地药品监管部门在检查中发现,产品标识进口代理商为广东美协文化发展有限公司,进口国为韩国的“怡思丁多维光护清透无感防晒喷雾SPF50+”,直接按照假冒产品进行查处,不予抽样。各地化妆品经营使用单位、经销商、网络销售平台提供者等经营主体,发现该产品的,应立即停止销售,并主动报告当地药品监管部门。
关于71批次化妆品不合格的通告(2019.01.30)
经青海省药品检验检测院等检验,标示为广州市白云区伊贝诗精细化妆品厂等35家企业生产的71批次化妆品不合格(不合格清单详情请见链接附件)。
上述不合格产品及相关企业违反了《化妆品卫生监督条例》《化妆品标识管理规定》等相关法规的规定。国家药品监督管理局要求广东、浙江省药品监管部门核实后依法督促相关生产企业对已上市销售相关产品及时采取召回等措施,立案调查,依法严肃处理;要求安徽、北京、福建、甘肃、广东、广西、贵州、海南、河北、湖北、湖南、江苏、江西、辽宁、宁夏、青海、山西、天津、新疆、西藏、云南、浙江省(区、市)药品监管部门责令相关经营单位立即采取下架等措施控制风险,对涉嫌假冒的产品,要深查深究其进货渠道,对违法违规行为,依法予以查处,涉嫌犯罪的依法移交公安机关。上述省级药品监管部门自通告发布之日起3个月内公开对相关企业或单位的处理结果,相关情况及时在国家化妆品抽检信息系统中填报并报告国家药品监督管理局。
关于92批次化妆品不合格的通告(2019.01.28)
经广东省药品检验所等检验,标示为广州市汉邦化妆品有限公司等30家企业生产(代理)的92批次化妆品不合格(不合格清单详情请见链接附件)。
上述不合格产品及相关企业违反了《化妆品卫生监督条例》《化妆品标识管理规定》等相关法规的规定。国家药品监督管理局要求广东、浙江、上海、北京、辽宁、山东省(市)药品监管部门核实后依法督促相关生产企业对已上市销售相关产品及时采取召回等措施,立案调查,依法严肃处理;要求安徽、北京、甘肃、广东、贵州、海南、河北、河南、湖北、湖南、江苏、江西、内蒙古、宁夏、山东、山西、陕西、天津、新疆、西藏、云南、浙江省(区、市)药品监管部门责令相关经营单位立即采取下架等措施控制风险,对涉嫌假冒的产品,要深查深究其进货渠道,对违法违规行为,依法予以查处,涉嫌犯罪的依法移交公安机关。上述省级药品监管部门自通告发布之日起3个月内公开对相关企业或单位的处理结果,相关情况及时在国家化妆品抽检信息系统中填报并报告国家药品监督管理局。
关于79批次化妆品不合格的通告 (2019.01.03)
经北京市药品检验所等检验,标示为浙江章华保健美发实业有限公司等23家企业生产的79批次化妆品不合格(不合格清单详情请见链接附件)。
上述不合格产品及相关企业违反了《化妆品卫生监督条例》《化妆品标识管理规定》等相关法规的规定。国家药品监督管理局要求广东、浙江、北京、辽宁省(市)药品监管部门核实后依法督促相关生产企业对已上市销售相关产品及时采取召回等措施,立案调查,依法严肃处理;要求安徽、北京、福建、甘肃、广东、贵州、海南、河南、湖北、湖南、江苏、江西、青海、山东、山西、陕西、天津、新疆、云南、浙江省(市)药品监管部门责令相关经营单位立即采取下架等措施控制风险,对涉嫌假冒的产品,要深查深究其进货渠道,对违法违规行为,依法予以查处,涉嫌犯罪的依法移交公安机关。上述省级药品监管部门自通告发布之日起3个月内公开对相关企业或单位的处理结果,相关情况及时在国家化妆品抽检信息系统中填报并报告国家药品监督管理局。
2018年12月未准入境的化妆品信息 (2019.01.30)
2018年12月,全国海关在入境口岸监管环节检出安全项目不合格并未准入境的化妆品1批。未准入境的化妆品来自日本,未准入境的原因为未按要求提供证书。
以上未准入境的化妆品已在口岸退运或销毁。
广东省药品监督管理局关于明确机构改革过渡期药品化妆品医疗器械案件查处工作有关职责的通知 (2019.01.31)
根据《国务院关于国务院机构改革涉及行政法规规定的行政机关职责调整问题的决定》(国发〔2018〕17号)和《广东省人民代表大会常务委员会关于省人民政府机构改革涉及省的地方性法规规定的行政机关职责调整问题的决定》(2019年第24号公告)的精神,为做好机构改革过渡期药品、化妆品和医疗器械(以下简称“两品一械”)案件查处工作,确保工作不断不乱,现提出如下工作要求:
一、各地要高度重视“两品一械”案件查办工作。药品安全事关人民群众健康福祉、事关社会稳定、事关经济发展大局。在机构改革过渡期,各地要提高政治站位,深刻认识到做好这一时期药品安全监管工作的重要性,切实把思想和行动统一到中央和省的决策部署上来,坚守工作岗位,严守安全底线,进一步加强“两品一械”案件查办工作,坚持“最严厉的处罚”,保持严厉打击“两品一械”生产经营违法犯罪高压态势,确保案件查办工作不断、力度不减。
二、机构改革过渡期原案件查办职责保持不变。根据国务院和省人大常委会有关决定,相关职责尚未调整到位之前,由原承担该职责和工作的行政机关继续承担。机构改革过渡期,新明确的“两品一械”案件省级查处事权(含药品、化妆品和医疗器械生产环节,以及药品批发、零售连锁总部和互联网第三方平台违法行为的查处,下同)的原执法主体保持不变,仍由原各市县食品药品监管部门承担;已挂牌设立市场监管部门的市县,由食品药品监管部门并入的市场监督管理部门承担。
按照中央综合执法改革工作部署,2019年3月底,各地市场监管综合执法职能和队伍应整合到位。届时省级部门将正式承接“两品一械”案件省级查处事权,各市县市场监督管理部门(食品药品监督管理部门)不再承担属于省级事权的“两品一械”案件查办工作职责,但之前已立案的案件应由原办案部门或者其并入的部门继续完成至办结为止。
三、切实加大对“两品一械”案件查处力度。各地要针对群众反映强烈的突出问题,重拳出击、重典治乱,围绕重点品种、重点主体和重点领域机构,严厉查处“两品一械”违法违规行为。机构改革过渡期,原各市县食品药品监督管理部门仍应继续承担辖区内省级事权案件查办工作及相关举报投诉处理、违法线索协查任务,并按照省药品监管局的统一部署,做好跨区域或重大的“两品一械”违法案件查办工作。
四、严格落实“两品一械”监督抽检工作。鉴于2019年抽检工作经费已经按照原工作模式下达到各市,“两品一械”抽样工作仍由各市承担,省药品监管局将另行专门下发2019年广东省“两品一械”抽样检验工作计划,对具体工作安排进行部署。省药检所、省器械所和各地药检所承担相关检验工作。机构改革过渡期,属于省级事权的不合格报告送达、问题产品召回、不合格原因调查和落实整改等不合格产品核查处置工作的职责,仍由原负责食品药品监管的部门负责。各地要突出重点,坚持问题导向,加强对消费量大、风险高和容易出现不合格“两品一械”品种的监督抽检力度,及时处置不合格产品,消除质量安全隐患。
春节期间化妆品安全消费温馨提示(2019.01.21)
春节将至,广东省药品监督管理局温馨提示广大消费者:掌握了必要的化妆品安全常识,才能正确选择和科学使用化妆品,规避消费误区,远离安全风险。
一、确认产品合法
化妆品经由注册或备案后方可上市销售。消费者如购买育发、染发、烫发、脱毛、美乳、健美、除臭、祛斑(含美白)、防晒9类特殊用途化妆品(简称特化),请核对产品销售包装上标注的批准文号,国产特化批准文号为国妆特字G××××××××,进口特化批准文号为国妆特进字J××××××××,必要时可登陆国家药品监督管理局网站查询产品注册信息。(网址:http://www.nmpa.gov.cn/WS04/CL2042/ )。
一般清洁类(如洗发水、洗面奶等)、护肤类(如护肤膏霜、乳液等)、美容/修饰类(如香水、唇膏、指甲油等)等化妆品属于非特殊用途化妆品(简称非特)。国产非特可登陆国家药品监督管理局网站查询备案信息(网址:http://125.35.6.80:8181/ftban/fw.jsp),国产非特备案号为省份简称+G妆网备字××××××××××。进口非特可核对产品销售包装批准文号或备案号,进口非特批准文号为国妆备进字J××××××××,批准文号可登陆国家药品监督管理局网站查询(网址:http://www.nmpa.gov.cn/WS04/CL2042/);进口非特备案号为国妆网备进字(省份简称)××××××××××,备案号可登陆国家药品监督管理局网站查询(网址:http://ft.zybh.gov.cn/province/webquery/list.jsp )。
二、选择正规渠道
建议消费者选择规范企业购买。规范的化妆品经营企业(包含批发市场、专营店、美容院、电商等)应当能够提供所售产品注册或备案的相关证明文件。消费者购买产品时,应要求商家提供发票或电脑小票,并在上面注明购买化妆品的名称、生产厂家和生产批号,以利于依法维权。不能提供上述信息的企业,请消费者谨慎选择。
三、敬请理性消费
化妆品不是药品,一般用于人体表面(牙膏可用于牙齿及口腔黏膜),主要发挥清洁、护理等功能,其作用较为缓和,一般不可能速效显效,建议消费者警惕产品虚假夸大宣传,如宣称快速美白、快速祛痘、快速祛斑等;生活美容院不是医院,建议消费者不要在此类场所进行医学美容,如注射肉毒素等。
四、消费维权建议
消费者如果不慎购买了未注册或未备案产品,应及时向当地食品药品监督管理部门投诉举报,举报电话:12331。
消费者正常使用化妆品出现不良反应,应立即停用并视情就诊,并可通过关注“广东省药品不良反应监测中心”微信公众号进行不良反应上报。
上海市药品监督管理局关于进口非特殊用途化妆品备案管理工作有关事项的公告 (2019.01.07)
为贯彻《国务院关于在全国推开“证照分离”改革的通知》(国发〔2018〕35号)精神,按照国家药品监督管理局《关于在全国范围实施进口非特殊用途化妆品备案管理有关事宜的公告》(2018年第88号)做好本市进口非特殊用途化妆品备案工作,现就有关事项公告如下:
一、备案管理通过国家药品监督管理局“进口非特殊用途化妆品备案管理系统”实施,具体事项办理参照原国家食品药品监督管理总局《关于发布上海市浦东新区进口非特殊用途化妆品备案管理工作程序(暂行)的公告》(2017年第10号)等相关文件执行。详细内容参见上海市药品监督管理局政务网站(http://www.shfda.gov.cn/ ):首页>信息公开>食药监局专题专栏>进口非特殊用途化妆品备案管理工作>进口非特殊用途化妆品备案管理工作指引。
二、为方便企业递交纸质备案资料,上海市药品监督管理局会有关区市场监督管理局设立受理点,承担境内责任人用户名发放及备案纸质资料接收等相关事宜。(具体受理点请见链接)
三、产品备案后,境内责任人持备案管理系统生成的备案凭证,至上海海关按照有关规定办理进口相关手续。后续拟从其他省、自治区、直辖市口岸进口的,应在备案管理系统上补充填报进口口岸和收货人等相关信息。
四、境内责任人应履行承诺,建立进口非特殊用途化妆品质量安全管理制度,加强产品追溯和质量管理,承担产品的质量安全责任,确保化妆品的进口和经营符合法规和标准的要求。发生产品质量安全问题时,应主动公开相关信息并及时召回。
韩国修订《化妆品法案实施细则》(2019.01.10)
2018年12月31日,韩国食药部发布《化妆品法案实施细则》修正案(第1516号总理令),修正该细则第8条(生产销售经理资质标准)、第13条(化妆品生产报告)、第15条(关闭或终止营业)、第19条(化妆品包装的说明和标记),其中第19条新增(8),规定了包装需标记防腐剂含量的产品类型。该修订案于发布之日起生效。
产品召回
|
欧盟
|
|||
| 通报国家 | 产品 | 原因 | 措施 |
| 德国 |
产品类别:化妆品 产品名称:亮肤霜 产品描述: 亮肤霜的容器为 白色瓶子,外包装为同颜色 的盒子,产品已在网 上销售 (特别是亚马逊)。 原产地:法国 |
化学危害 该产品含有检测值为3.7%的 对苯二酚(hydroquinone)。 皮该物质可引起皮肤刺激和炎症。 该产品不符合欧盟化妆品法规的 规定。 |
经济运营商 (零售商) 采取措施: 从亚马逊平台 下架。 |
| 爱沙尼亚 |
产品类别:化妆品 产品名称:婴儿湿巾 产品描述:绿色包装中有72 片儿童湿巾。 原产地:波兰 |
微生物危害 该产品含有金黄色葡萄球菌 (Staphylococcus aureus)。 这些都有感染的风险,尤其是受 损的皮肤。 该产品不符合欧盟化妆品法规的 规定。 |
经济运营商 (经销商) 采取措施: 向消费者警告 其风险; 从市场上撤回 相关 产品。 |
| 德国 |
产品类别:化妆品 产品名称:直发产品 产品描述: 直发产品的容器 为带蓝色 印刷的白色塑料瓶, 与洗发香波和发膜 作为一个套装进行销售。 该产品已在网上销售。 原产地:巴西 |
化学危害 该产品含有过量的甲醛 (检测值为5%); 甲醛可引起眼部、皮肤和上呼吸道 刺激; 长期接触可能会导致癌症。 该产品不符合欧盟化妆品法规的 规定。 |
经济运营商 (零售商) 采取措施: 通过网购 平台发布 撤回申请。 |
| 捷克 |
产品名称:香水 产品描述:产品容器为带塑料 盖的玻璃瓶,净含量100ml。 原产地:阿拉伯联合酋长国 |
化学危害 该产品含有戊基肉桂、香叶醇、 苯甲醇、 肉桂醇和肉桂酸苄酯 (测定值分别为0.1%, 0.014%, 0.0069%,0.0037%,0.0031%)。 这些物质可引起过敏反应和过敏。 消费者不知道其存在,因未在成分 列表中指出。该产品不符合欧盟化 妆品法规的规定。 |
经济运营商 (零售商) 采取措施: 从市场上 撤回 相关产品。 |
|
根据欧盟化妆品法规的规定, 欧盟消费者安全科学委员会SCCS在其第10次修订关于化妆品成分测试和其安全性评估指南 (SCCS guidance for the testing of cosmetic ingredients and their safety evaluation)中指出,3岁以下儿童用、眼部或黏膜部位用化妆品的需氧菌、霉菌和酵母菌总数≤100cfu/g , 其他产品≤1000cfu/g。根据欧盟化妆品法规的规定,其中指定的26个香精过敏原如超过一定浓度,应在标签上标示。 |
|||
| 捷克 |
产品名称:香水 产品描述:产品容器为带塑 料盖的玻璃瓶,净含量100ml。 原产地:中国 |
化学危害 该产品含有己基肉桂、芳樟醇、 苯甲酸苄酯、 香豆素、香茅醇、 丁香酚、环己烯甲醛和香叶醇 (测定值分别为:0.41%,0.038%, 0.019%,0.013%,0.012%, 0.0097%,0.0077%和0.024%)。 这些物质可引起过敏反应和过敏。 消费者不知道其存在,因未在成分 列表中指出。 该产品不符合欧盟化妆品法规的规定。 |
经济运营商 (零售商) 采取措施: 从市场上 撤回 相关产品。 |

来源:ITS


