您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2019-04-22 11:28
欧美国家口服固体制剂生物等效性试验指导原则的要点和启示
作者:张逸凡 钟大放
中国科学院上海药物研究所
摘要
制剂生物等效性试验是评价仿制药口服固体制剂内在质量的关键。
欧美国家药品管理部门颁布了相应的指导原则,并且在使用和实验的基础上不断修订完善。
其要点包括试验设计、参比制剂选择、高变异药物和窄治疗指数药物的特殊要求等,反映了国际上的新进展。
在《中华人民共和国药典》相关指导原则中,吸收了国际先进标准。
我国正在开展的仿制药质量一致性评价,对保障口服固体制剂生物等效有重要作用。
正文
制剂生物等效的基本原则是20 世纪90 年代初确定的,即受试制剂和参比制剂主要药动学参数( AUC 和Cmax) 几何均值比的90% 置信区间应落在80% ~125%之间。
美国、日本、欧盟、加拿大和南非等国相继制定了各自的指导原则。《中华人民共和国药典》2000 年版首次制订了《药物制剂人体生物利用度和生物等效性试验指导原则》,国家食品药品监督管理总局药品审评中心也在2005 年3 月推出了《化学制剂人体生物利用度和生物等效性研究技术指导原则》。
欧盟于1992 年6 月颁布了首个生物利用度( BA) 和生物等效性( BE) 研究指导原则,2001 年7月颁布了《对生物利用度和生物等效性研究的说明》。
2010 年1 月欧洲药品管理局( EMA) 颁布了《生物利用度和生物等效性研究指导原则》,对既往指导原则做了修订。
该指导原则仅适用于仿制化学药品的普通制剂,不包括调释制剂、透皮制剂、经口吸入制剂以及无法用药物浓度证明生物等效性,需要药效动力学或临床终点试验证明等效的药物制剂。
美国食品药品监督管理局( FDA) 于2003 年颁布了《口服制剂生物利用度/生物等效性BA/BE)研究的总体考虑》,并且针对具体药物,FDA 均给出了具体的指导意见。
2007 年FDA 又颁布了《食物对生物利用度的影响以及餐后生物等效性研究技术指导原则》,作为对上一个指导原则的补充。
2013 年12 月FDA 颁布了《以药动学为终点评价指标的仿制药生物等效性研究指导原则( 草案) 》,该指导原则修订并拟替代前两个指导原则中有关仿制药BE 研究的内容。该指导原则也适用于缓控释制剂的BE 试验。
相对于EMA 的指导原则,FDA 的指导原则更加细致、具体和严格。
本文通过对EMA 和FDA 指导原则的要点进行比较,介绍国外对口服制剂生物等效性研究的新规定和观点,以及对我国相应领域的启示。
EMA 和FDA 生物等效性试验
指导原则要点
1、生物等效性试验设计
EMA 和FDA 指导原则中,标准的设计都是2 ×2 的双周期交叉试验设计。对于长半衰期药物,也可以接受平行设计,但不同治疗组别的人口学基线值应该相当,如年龄、体重、性别、种族、吸烟情况和代谢能力等。
因此在平行试验设计中,有必要筛查受试者特定药物代谢酶的基因型或表型,对受试者合理分组。对于高变异药物,推荐使用重复交叉试验设计,以准确评价制剂的个体内变异情况。
一般认为单次给药能更敏感地比较药物释放进入系统循环的制剂间差异,所以指导原则建议采用单次给药试验。
在EMA 指导原则中,有2 种情况可接受多次给药的BE 试验,
一是由于安全性/耐受性原因,只能对患者进行研究,而患者无法停止用药;
二是由于分析方法检测灵敏度不够,需要多次给药达到较高的浓度。
在后一种情况下,如果没有溶解度和安全性的限制,也可单次给予高于临床的剂量进行BE 试验。
而FDA 指导原则规定,只有在第1种情况时可接受多次给药的BE 试验。
2、选择受试者
EMA 和FDA 均建议优先选择健康志愿者为受试者,但由于安全性原因,也可选择患者进行生物等效性研究。EMA 和FDA 均要求有足够的受试者例数,以保证试验的把握度。
EMA 对受试者例数的要求是不少于12 例,并认为在大多数情况下,健康志愿者体内模型足以检测制剂的差别,并允许将结果外推到参比药品被批准治疗的群体( 如老年、儿童、肾或肝功能受损患者等) 。
FDA 新的指导原则要求生物等效性试验的受试人群具有代表性,要考虑年龄、性别和种族等因素,如果试验药物的适用人群包括不同性别,则受试人群应有相似的男女比例; 如果试验药物主要用于老年患者,则建议尽可能多的入选60 岁以上的老年志愿者。
对于高变异药物采用比例标化的平均生物等效性试验时,FDA 要求例数不少于24 例。
3、选择参比药品
按照EMA 要求,参比制剂应该是在欧盟已经获得上市授权的药品,并具有全面的药效和安全性资料。因此原研产品的最初批准剂型应该是首选。
FDA 对于参比制剂的选择很明确,在处方药及非处方药的目录中,FDA 规定了参比药品目录,以此来避免由于参比制剂使用的不同而可能导致的各仿制品之间发生显著的差异。每个品种的参比药品都非常明确,并给出了特定药厂和特定规格。
EMA 和FDA 都要求受试制剂药物含量与参比制剂药物含量差值小于5%,对于BE 试验中的药品,FDA 要求要保存足量的留存样品。
4、选择空腹或餐后服药
EMA 认为空腹条件在评价制剂差别时最敏感,一般只要求空腹给药下的试验。但如果参比制剂注明餐后给药,则一般在餐后条件下进行BE 试验。
如果餐后给药仅仅是为了避免患者长期用药出现耐受性问题,则也可以接受空腹条件的BE 试验; 如果是基于药动学原因导致药物暴露量显著不同而采用餐后给药方式时,则只能进行餐后给药的BE 试验。
对于特殊剂型特征的药品( 如微乳和固体分散体) ,生物等效性试验需要既在空腹也在餐后条件进行,除非药品必须仅在空腹或仅在餐后服用。
FDA 新的指导原则整合了餐后BE 研究的相关内容。要求除空腹给药外,还要进行餐后给药的BE试验,除非参比药品说明书明确规定空腹给药。
对于只能餐后给药的立即释放制剂,除餐后给药外,只要没有严重不良事件的风险,也要做空腹给药BE试验。
因此,按照FDA 的要求,大部分药物均需要进行空腹和餐后2 种条件下的BE 试验。而对于缓释制剂,均要求在空腹和餐后2 种条件下进行单次给药的BE 试验。
在FDA 新的指导原则中,对于食物组成与EMA 要求相似,只规定食物的热量和脂肪含量,以及试验用餐中,蛋白、糖类和脂肪的热量比例。
不再推荐相应的食谱,因此可以根据试验地点的饮食习惯选择食物组成。
5、选择检测物质
5.1 原形或代谢物
原则上,评价生物等效性应该基于母体化合物的测得浓度,即便是非活性前药,这已得到共识。
按照EMA 的要求,如果已经测了母体药物,则不需要检测活性代谢物。但FDA 要求,当主要代谢物由系统前代谢形成( 如首过效应、肠壁或肠腔代谢) 且对药物安全性或疗效有显著影响时,需要检测该代谢物,但仅对原形药物进行生物等效性评价,代谢物只作为支持数据。
特殊情况下,如非活性前药血浆浓度很低,并且快速清除,导致难于证明母体化合物的生物等效性时,或者试验研究药物母体化合物的分析方法不能改进时( 即使在高剂量下) ,可考虑用活性代谢物或主要代谢物进行BE 评价。
5.2 对映体或外消旋体
通常推荐用非手性的方法进行生物等效性研究。按照FDA 的要求,同时满足以下4 种情况时才需要对映体选择性分析:
① 两对映异构体药效不同。
② 两对映异构体药动学不同。
③ 两对映异构体中占少数的异构体发挥主要疗效。
④ 至少有一个对映异构体吸收过程呈现非线性( 随着药物吸收速率的变化,两对映异构体浓度比例发生改变) 。
6、内源性物质的生物等效性试验
如果试验药物和内源性物质结构相同,则应该用基线校正来计算药动学参数,以使药动学参数计算反映给药后增加的浓度。
而对于基线校正的方法,用的最多的校正方法是给药后测得浓度减去基线浓度,而基线浓度一般为给药前3 个以上浓度的均值。
EMA 推荐标准缩减基线校正法,即减去个体的内源性物质给药前浓度的均值,或者减去个体给药前内源性AUC。
也有人用内源性物质基线水平的对数值进行校正。
比较成熟的方法是在给药前检测不同时间点内源性物质水平,以获得有昼夜节律的基线值,给药后浓度用相应时间点的校正值。
这个方法与FDA 推荐的方法相似,即对于由机体产生的内源性物质,建议给药前根据药动学特征多点测定基线值,从给药后的血药浓度中减去相应的基_线值。
若经过基线校正后血药浓度出现负值,则以零计。
校正前和校正后的数据应分别进行药动学参数计算和统计分析。
采用校正后的数据进行生物等效性评价。
FDA 强调对来源于食物的内源性物质,试验中控制饮食的必要性。EMA 建议考虑超治疗剂量给药,只要该剂量能被很好耐受,使给药后增加的超过基线的浓度能被可靠测定。不管何种校正方法,都应该在试验前规定。
7、关于高变异药物
高变异药物和高变异药物制剂分别指生物等效性试验中AUC 和Cmax的个体内变异系数≥30% 的药物和药物制剂。
个体内变异的来源包括影响生物利用度的生理学因素、药物的内在性质、物理化学性质、制剂因素及其他。
据统计,2003 -2005 年在FDA 做上市评价的仿制药制剂中,有约20% 为高变异药物制剂。进行高变异药物BE 试验时,需要更多的受试者才能达到足够的把握度。
但是,扩大受试者例数既会带来伦理学问题,也会增加申办者的经济负担。
因此,对于高变异药物的生物等效性评价问题,一直以来是各国研究人员和药政管理部门所关心的问题。
关于高变异药物的BE 研究,一些专家和机构提出的解决办法有:
① 增加样本量。
② 重复交叉设计或多剂量试验设计。
③ 放宽等效性判断的限值,这种方式又包括静态放宽、固定样本量放宽和比例标化的平均生物等效性。
比例标化的平均生物等效性方法是目前FDA 推荐的方法,即根据参比制剂的个体内变异程度放宽生物等效性判断的标准。
为了判断是否为高变异药物,需要采用重复交叉试验设计以评估药物的个体内变异程度。
可采用部分重复的交叉试验设计( 3 周期) 或完全重复的交叉试验设计( 4 周期) ,其核心均强调参比制剂要重复给药1 次。
目前FDA 推荐比例标化的平均生物等效性方法,对于高变异药物,AUC 和Cmax的等效性判断标准为: 上限/下限= exp [± ln( 1.25)·(SWR/SWO) ]。
SWR表示参比制剂的个体内变异,SWO是预先设定好的常数0. 25 ( 对应的个体内变异系数CV =25. 4%) 。
参比制剂个体内变异SWR的界值定为0. 294( 对应的个体内变异系数CV = 30%) ,当SWR≥0. 294 时,FDA 允许根据参比制剂的个体内变异程度放宽等效性判断接受的标准。
但是这种方法对受试制剂和参比制剂几何均值比( GMR) 的差别缺乏敏感性,有时会出现结果显示两个制剂是等效的,但两制剂GMR 的点估计值却落在80% ~125% 之外的情况。
而BE 试验模拟结果也表明,当个体内变异超过50% ~ 60%时,对GMR 的点估计值的限制则成为主导标准。
因此,FDA 还要求两制剂GMR的点估计值应在80% ~125%范围内。FDA 推荐的高变异药物的生物等效性评价具体算法见孕酮胶囊生物等效性的指导意见。
2010 年版EMA 指导原则采用的方法与FDA 相似,但也有一些不同。
EMA 只接受对Cmax放宽接受标准,同时设定了最大的限度至69.84% ~ 143.19%( CV = 50%) ,对AUC 仍然采用80% ~125% 的标准。
对于高变异药物,EMA 的接受范围按下式计算: 上限/下限= exp(±k·SWR) 。k 是一个为0.760 的常数,与比例标化的起点变异度( CV = 30%) 相对应,这样比例标化和非比例标化之间可平滑过度,以避免在个体变异略高于30%时,过度放宽标准。
而FDA 采用的比例标化常数有更大的自由度( 更宽的标准) 。FDA 和EMA 对置信区间的放宽标准如图1 所示。
图1 FDA( a) 和EMA( b) 生物等效性标准比较。
无论何种算法,采用比例标化的平均生物等效性方法,均可大大减少试验受试者的例数,并增加试验的把握度。
以阿仑膦酸钠为例,它属于高变异药物,AUC 和Cmax的个体内变异约50%,1 项24 例受试者的双周期交叉试验把握度只有50%,尽管受试制剂和参比制剂参数的几何均值比为95%,其90%置信区间仍未落在80% ~125% 之间,要获得80%的把握度,至少需要106 例受试者。
如果采用3 周期重复交叉设计、比例标化的方法进行评价,31 例受试者可得到90% 的把握度。该方法已成功用于一项阿仑膦酸钠制剂的生物等效性研究。
8、关于窄治疗指数药物
EMA 对治疗指数窄的药物比较严格,AUC 的等效性标准缩窄至90% ~ 111. 11%,在Cmax对安全性、药效或药物浓度监测特别重要的情况下,同样适用于上述范围。
FDA 在2012 年前对窄治疗指数药物的接受标准仍然是80% ~125%。而目前FDA 推荐的是比例标化的方法,在等效性限值90% ~111%基础上根据参比制剂的变异度放宽标准。
当参比制剂的个体内变异CV≤10% 时,等效性限值为90% ~111%; CV 在10% ~ 21%之间时,等效性限值比80% ~ 125% 窄; CV > 21% 时,等效性限值为80% ~125%。
另外要求受试制剂和参比制剂的个体内变异比值SWT /SWR≤2. 5。基于这一要求,只能采用完全重复的交叉试验设计( 4 周期) 。
FDA 推荐的窄治疗指数药物的生物等效性评价具体算法见华法林片生物等效性的指导意见。
9、其他
EMA 的指导原则可以接受2 阶段试验设计,但要求必须在试验方案中预先规定,为减少I 类错误的发生,要规定调整后显著性水平。
在分析第1 阶段以及第1 和第2 阶段合并的数据时,使用94. 12%置信区间是可以接受的。EMA 和FDA 都对数据的剔除做了说明,如呕吐和腹泻、非零基线浓度大于Cmax的5% 以及AUC0 ~ t 覆盖 AUC0 ~ ∞少于80%的数据处理。
新版的FDA 指导原则指出: 对于半衰期较长的( 24 h 以上) 药物,如果药物分布和清除个体内变异较大,则不能截取部分AUC 来评价药物暴露量。
因为在给药后短时间内( 5 ~ 15 min) 未采集早期的样本,导致首个样本即为Cmax,则一般不应将该受试者的数据纳入统计分析。
另外,特殊问题点则考虑到了酒精对非常释制剂可能的影响。
对我国生物等效性试验的启示
经过近20 年的发展,我国的生物等效性试验水平有了较大的提高,并且日趋与国际接轨。
1、指导原则的修订
在2000 年版《中华人民共和国药典》中,对制剂生物等效性的接受限度规定为AUC 几何均值比在80% ~125%,Cmax几何均值比在70% ~143%。
显然,此处明显放宽了Cmax的接受范围。
在2010 年版《中华人民共和国药典》中,Cmax几何均值比的接受范围缩窄为75% ~135%。在即将发布的2015 年版《中华人民共和国药典》中,该范围进一步缩窄为80% ~125%。
上述变化反映了我国制剂工业的技术进步,以及与国际先进标准逐步接轨的过程。
在《中华人民共和国药典》2015 年版修订的指导原则中,还明确了对参比药品、受试药品以及试验药品包装的规定; 对受试者和试验标准化也有新的规定; 对代谢物、对映异构体、内源性物质BE试验也有具体规定。
此外,规定生物等效性试验每周期采样一般不超过72 h。此次修订还引入了对窄治疗指数药物生物等效性试验的规定、对高变异药物生物等效性试验的规定、生物等效性试验相关的体外溶出度检查以及基于药剂学分类系统的生物豁免概念。
2、固体制剂质量一致性评价与生物等效性评价
在制剂生物等效性评价中,发现的问题有:
① 药物制剂体外一致性评价不充分,很多药厂在开展体内BE 试验前未进行系统的溶出度试验考察,BE 试验失败后,再进行体外溶出度的比较试验寻找原因。
② 由于受试者例数不够导致无法判断制剂是否等效,有些药厂无法接受由于受试者例数增加所带来的支出。
③ 参比制剂选择的困难,有些原研药品虽然获得了进口许可,但无法在市场买到。
对于问题①,建议采用多条溶出曲线进行受试制剂和参比制剂一致性评价,体外溶出度试验比较得越充分,就越能发现问题,及早改进。
对于问题②,可以参考本文前面叙述的比例标化试验设计,降低受试者例数。
对于问题③,建议研发人员和申办方应及时了解国内外研究动态,尽可能多与相关管理部门和药物审评部门的专家沟通,改进国内生物等效性试验的质量,进而提高国内仿制药的研发水平。
展望
随着我国经济的发展和制药工业的技术进步,人们期待着更高质量的药品。目前,我国生物等效性试验指导原则正在全面接轨国际先进水平。
随着固体制剂质量一致性评价等项目的广泛开展,实现上市药品生物等效的技术保障将日趋完备。
我们要继续关注国际上制剂生物等效性研究和法规的新进展,借鉴发达国家的经验,为确保仿制药品的安全、有效和质量可控而不断努力。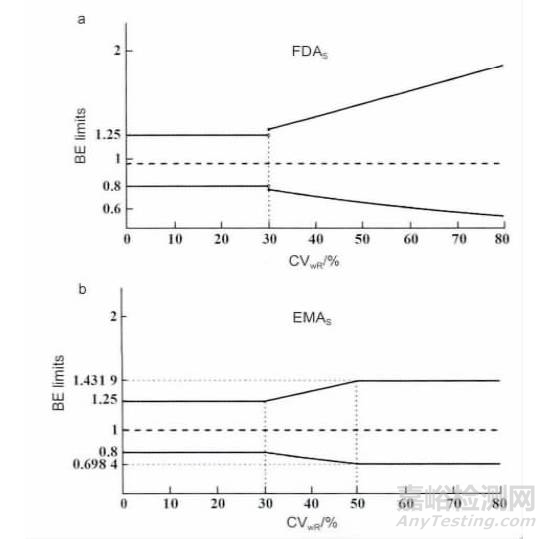

来源:AnyTesting


