您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2019-07-05 15:17
20 世纪 70 年代,某静脉输液剂型发生过一次严重的事故:盛放药物的玻璃瓶密封失误,受到污染,造成约 8,000 起血行性感染,并导致最终 10% 的患者死伤。这次严重的包装故障事件引发了全生命科学行业对包装完整性的高度重视!
药品的质量和有效性在很大程度上取决于恰当的包装:无菌产品和对水分 / 氧气敏感药物在长达数年的保质期内需要极好的屏障,以保护药物免受微生物污染、水分和氧气的侵入。
容器密封性(CCIT –Container Closure Integrity Test),顾名思义就是检查容器(内包材)的密封性(完整性,泄漏情况)。
容器密封性测试主要分为物理的(Physical CCIT)和微生物测试(Microbial CCIT)。测试方法包括常见的亚甲基蓝染色,真空衰减,激光,微生物侵入法等等。方法选择时,则需考虑各种因素,如包装本身、包装内容物、密封组件的匹配、方法本身的特点、检出限等。
一些对湿度高度敏感的药物(例如用于吸入的干粉)则需要具有高灵敏度的完整性测试。
传统的一般检测方法有很大的漏洞空白。制造者需要自己学习并升级/搭配测试方法,完整的密封性测试决定药物产品的最终质量!
CCIT:监管严格,却缺乏详细指南
药品容器封闭完整性测试的高风险导致它受到严格监管。主要机构有FDA(美国)和 EMA(欧洲)。
2008 年,美国 FDA 发布了针对整个生命科学行业(制药公司、兽医药品和制造无菌医疗产品的公司)的新指南,该指南要求该领域进行可靠的物理测量以确保适当的CCI。
然而在实践中,FDA 的新指南、欧洲的生产规范指南、甚至是无菌医药产品制造规定,这三大指南,都没有具体的方法建议。只是给予制药商既定义务:必须确保“容器封闭系统能够保持其微生物屏障的完整性,从而确保药品在整个保质期内的无菌性”。
尽管官方法规通常没有详细描述如何进行 CCI 测试。但美国药典处理了这个问题,并在 2016 年提出了一项新的指南:USP <1207>。该指南重点关注无菌和重要医药产品(例如小瓶和注射器),其分为 3 章:
■ 1207.1:包装完整性和测试方法选择
■ 1207.2:包装完整性泄漏测试方法
■ 1207.3:包装密封质量测试方法
USP <1207> 并未描述出所有的方法,总共只介绍了三种:真空衰减法、高压放电法和激光法。但为评估各种流行的潜在方法提供了良好的概述和指导。
不同药物:不同测试方法和检测限
用于包装完整性测试的各种测试方法的初始列表已在 90 年代末发行。当时的报告范围非常狭窄,建议通过直接将其与微生物入侵测试进行比较来验证化学 - 物理泄漏。
该概率性测试方法依赖于具有随机结果的一系列顺序发生和 / 或同时发生事件。研究结果与需要大样本和精确测试条件控制的不确定性有关。
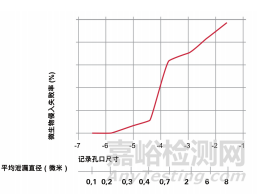
如图 1 所示,临界泄漏尺寸为 0.2 μm,分别为 6•10-6 mbar l/s。该值被广泛地用作所谓的 MALL(最大允许泄漏水平)。此外,该图表显示,2 μm 的泄漏已经导 致药物污染的风险接近 70%。
图1
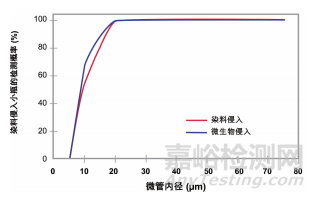
然而,这些研究已经证明,经典的概率性测试方法依然有很多漏洞。比如微生物侵入测试以及蓝染料测试方法。如图 2 所示,染料侵入测试 仅有约 70% 的机会检测到 10μm 的泄漏。任何低于 5μm 的泄漏都或多或少是不可检测的。
图2
因此,相对于传统的测试方法,建议应用确定性完整性测试方法。各种不同方法可以追溯到制药市场中 CCIT 的不同挑战。这些与不同的 工艺步骤、不同的包装类型和不同的药物类型有关。
测试从包装设计阶段就需要开始
在包装的早期开发阶段(“包装设计阶段”),供应商有义务确保包装在设计上能够保证无菌。因此,需要对包装进行 0.2 μm 范围内的缺陷测试,分别为 6•10-6 mbar l/s (MALL)。这些是目前对装满药物的容器的稳定性和质量控制的要求。
完整 性测试主要在 2 至 20μm 的缺陷尺寸范 围内进行。其主要原因是可用方法在合理 的测试时间内检测较小缺陷的可行性。当 处理以 120 至 600 份 / 分钟的速度运行的 生产线的 100% 检查时,允许的缺陷尺寸 有时甚至增加到显著更高的水平。生产单元的检测限 (LOD) 定义为成本、技术和产品之间基于风险的决策。为了补偿这种基于风险的方法,进行额外的离线样品测试, 以达到 1 至 10μm 范围内更严格的规格。这也适用于在实验室测试中进行的稳定性测试。
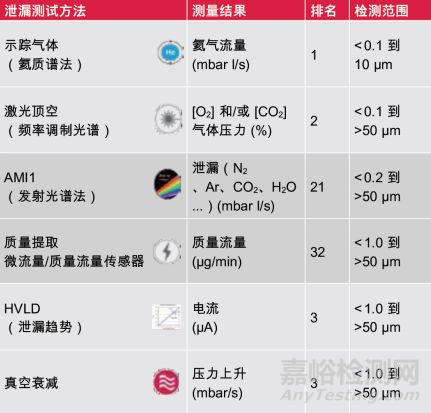
同样,灵敏度比测试时间更重要。图 3给出了制药行业中各种不同包装 和药物类型的粗略区别。并非所有测试方 法都可用于所有类型的包装以及所有类型 的药物。除了下面提到的包装类型的特征 之外,诸如包装的透明性和其导电性之类 的特征在选择正确的完整性测试方法方面 也起着重要作用。
图3
普发真空测试方法
普发真空提供各种不同的泄漏测试方 法,以解决制药行业面临的众多挑战,因为没有一种解决方案适合与特定产品相关 的所有不同挑战。普发真空可在 CCIT 流 程定义和集成的整个期间为客户提供支持, 并在 IQ/OQ(安装认证 / 操作认证)方面 提供 GMP 支持,包括所有测试方法所需 的文档。以下概述可以初步了解普发真空 的泄漏测试方法组合。
氦质谱法
普发真空氦气泄漏检测解决方案非常适合制药行业的 MALL 测试。为了确 保正确的测量,在测量期间管理示踪气 体浓度是非常重要的。处理小瓶或其他 密封包装时,这一点尤其棘手。因此, 普发真空提供完整的解决方案,包括示踪气体处理和充入以及根据不同的包装和 测试室进行调整。
质量提取法
我们 USP <1207> 和 ASTM (F-3287- 17) 认可的 Mass Extraction 技术的工作原理是基于稀薄气流。测试在真空条件下进 行,以获得更高的灵敏度。这种专利技术类型的测试特别适用于药品包装,如输液 袋、密封袋或玻璃瓶。使用该方法可以检测到更大的缺陷和小至 1 μm 的缺陷。因此,该技术适用于实验室应用以及在生产 环境中的使用,允许稳定性控制以及自动 100% 测试(也在内联机器中)。美国的 FDA 实验室和主要的制药公司已经使用质量提取仪器超过 10 年。
发射光谱法
用于 AMI 测试系统的普发真空发射光 谱法使用不需要示踪气体的专利工艺测量 密封性。相反,该方法使用包装内部空腔 中的现有气体混合物在扩展的测量范围内 进行高灵敏度测试。因此,AMI 具有区分 药物产品典型的气体种类的能力。该程序 具有很大的灵活性,可以测试各种不同的 包装类型,如泡罩包装、密封袋、药水瓶 和塑料瓶,也可以同时测试多个样品。
AMI 的广泛测量范围提供比传统测试 更高的灵敏度,从低至 1•10-6 mbar l/s 的 0.5 μm(和更小)的相应泄漏率开始, 但也可以识别粗略泄漏,例如完全打开的 容器。因此,AMI 设备可以在一个设备 中执行粗略和精细的泄漏测试。无论什么 用户,该程序都能提供具有高重复性的确 定性测试结果,并且具有 USP 1207.1 范 围内的可靠性和准确性。它可以在生产测 试期间用于实验室测试以及 IPC(过程控制)。根据包装的不同,同时也可对多个 部件进行同步测试。



来源:荣格医药商情


