您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2019-09-18 10:09
今天,咱们再来聊聊ICCBBA是如何编码UDI的。
01、ICCBBA机构介绍
ICCBBA全称为International Council for Commonality in Blood Banking Automation,即国际血库自动化委员会,成立于1983年,是一家国际非政府机构(NGO),负责管理、开发和许可ISBT 128。
ISBT 128为人源医疗产品术语、编码及标签的国际信息标准。该标准最初在1994年被ISBT(International Society of Blood Transfusion, 国际输血协会)所采纳,目前已得到广泛应用。其使用范围已经超出输血领域,扩展到所有的人源医疗产品。
截至2017年,分布在六大洲87个国家,超过5000家机构已经注册使用ISBT 128。每年有超过4000万份血液、细胞和组织产品被贴上了ISBT 128标签。
总的来说,ISBT 128标准主要具有以下特点:1)拥有捐献编号系统,确保识别的唯一性;2)采用国际认可的参考表格进行信息传输;3)拥有产品参考数据库;4)可承载信息的数据结构;5)用于传输产品标签信息的条形码系统。
02、ICCBBA编码规则
按照ICCBBA编码规则,医疗器械的UDI会由两部分组成,器械识别码(DI)和生产识别码(PI)。器械识别码包含厂商信息、厂商定义的商品信息、和标准化的产品描述信息。而生产识别码会由捐献唯一识别码、序列号、效期、生产日期以及批号中的一种或多种信息组成。
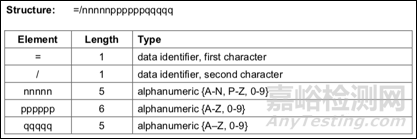
1. 器械识别码(DI)
最后五位字符“qqqqq”为产品描述代码(PDC, Product Description Code),由ICCBBA编制,注册用户可在ISBT 128产品描述代码数据库中进行查询,呈现的信息为代码及具体描述,可参考下表。


代码中的T指代Tissues,相关的产品大类还包括:Blood, Cellular Therapy, Ocular, Human Milk, Topical Products of Human Origin, Fecal Microbiota, Reproductive, Plasma Derivatives, In Vivo Diagnostic MPHO, Organs, and Regenerated Tissue。
另外,描述信息会包含产品分类和属性,例如,T0474代表氧化锡骨,其属性为去除矿物质。结合以上描述,大家可以参考下图示例,进一步巩固对于DI编码结构的理解。

按照ISBT 128编码要求,生产识别码必须包含捐献识别号和产品区分号(即序列号),而效期、生产日期和批号除非出现在产品标签上,则必须包含在内,否则自行选择。每一类信息也会对应不同的数字分隔符,比如序列号用“=,”表示,效期用“=>”表示,生产日期用“=}”表示,等等。详情参考下表。
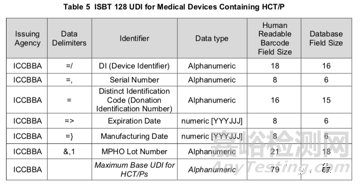
另外,编制批号和产品区分号会相对简单。批号用18位字母数字表示,序列号用6位字母数字表示即可。
3. ICCBBA UDI举例

03、如何向ICCBBA提交申请
向ICCBBA申请厂商识别代码的步骤很简单:第一,下载ISBT 128注册表单;第二,填写ISBT 128注册表,所有申请人都应填写表格的A部分,对于需要分配一个或多个厂商识别号码(FIN)的厂商,应针对每个FIN,填写B部分;第三,邮寄、传真或通过电子邮件发送ISBT 128注册表,并一同提交所需付款。通常而言,ICCBBA需要2-4周时间来处理注册申请。
04、ICCBBA收费情况
所有机构都需要支付一次性注册费和年度许可费,收费金额取决于机构类型。比如对于血液产品厂商,一次性注册且申请一个FIN的费用为200美元,额外的FIN每个收费160美元。
对于年度许可费用,如果你提供的是医院输血服务,而不是采集或汇集血液制品,那么年费为206美元;如果你拥有小于等于1000个产品数量,那么年费为245美元;若每年小于等于20000个,则为375美元;若每年大于20000个,则基础年费为375美元,超出部分按每个产品0.01582美元进行累加(可见下表)。
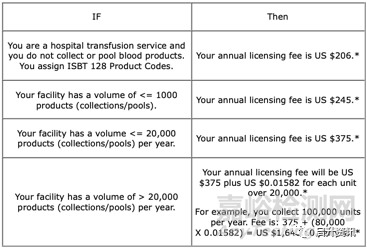
当然,除了血液制品外,还有细胞治疗产品、组织制品、组织及基于细胞和组织的医疗器械、人乳制品等等,其收费标准都会有所差异。小编在此就不做过多介绍,大家可以在ICCBBA官网进行查阅,网址为:https://www.iccbba.org/registration-licensing/isbt-128-fees#BloodCollection。
参考资料:
1. https://www.iccbba.org/home
2. An Introduction to ISBT 128
3. ISBT 128 STANDARD Coding and Labeling of Medical Devices Using ISBT 128
4. ISBT 128 STANDARD Standard Terminology for Medical Products of Human Origin For Use with Product Description Code Database

来源:启升资讯


