您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-04-01 19:47
作者:王鑫春、程志强、周耀昌、程志磊、莫盼盼
作者单位:河南驼人医疗器械集团有限公司
正交试验设计是一种应用普遍的试验工具,在多行业得到了广泛的应用,但在医疗器械行业却较少见到相关的报道。文章介绍正交试验设计在医疗器械产品开发过程中医用导管尖端成型工艺中的应用,通过应用正交试验设计中极差分析和方差分析方法,确定对医用导管尖端黏接力影响的关键因子,并确定温度、推力、时间和材料种类对医用导管尖端黏接力的影响,验证并确定最佳的医用导管尖端成型工艺参数窗口。
医疗器械的产品质量关系到其临床应用的安全性和有效性,一直以来都是社会和国家监管机构关注的重点,同时产品质量的优劣也是影响企业是否可以得到社会认可从而决定其自身能否得到持续稳健发展的重要因素。
1.研究背景
最初人们认为医疗器械的质量是由检验出来,但在长期应用实践后发现,对医疗器械产品各个环节进行100%检验几乎是不可能的,既不能从根本上解决质量问题,还会造成资源的巨大浪费,特别是一些特殊检验项目无法实现100%检验,只能采取抽样检验,但这样就存在着概率的风险,而要想解决这些无法或不便于检验项目的质量保证问题,只有对其进行工艺验证和确认才能使其质量稳定在某一个既定的水平。
20 世纪70 年代,日本质量大师田口玄一博士提出田口质量理论。他认为,产品质量首先是设计出来的,其次才是制造出来的,将质量控制从制造阶段进一步提前到设计阶段[1]。这一套全面质量管理理念已经应用到医疗器械质量管理中,并进行实践应用。
国家食品药品监督管理总局在2014 年发布了《医疗器械生产质量管理规范》,在该规范中强调了验证的重要性,要求将设计和开发的结果转换为适合企业的可执行的生产工艺规范,转换的根本方法就是实施医疗器械工艺的验证和确认,特别是对于特殊工艺或关键工艺更是如此。
随着质量管理实践的深入,质量工程与科学进一步发展,一些质量管理工具也随之应运而生,其中非常著名且广泛应用的就是正交试验设计法,该方法在许多行业都得到了广泛的应用,但在医疗器械行业却很少见到相关报道。
正交试验设计是利用正交表来安排与分析多因素试验的一种设计方法。它是由试验因素的全部水平组合中,挑选部分有代表性的水平组合进行试验,通过对部分试验结果的分析了解全面试验的情况,找出最优的水平组合[2]。该工具特别适用于新产品开发过程,借助该工具可以较快确定影响产品质量的关键因素,减少试验次数,缩短试验周期,从而节约成本加快新产品开发的效率,并可确定最佳工艺参数窗口,为产品质量提供可靠的工艺参数。
本文以医用导管尖端成型工艺的验证过程为案例,介绍了正交试验设计在医疗器械产品开发过程中医用导管尖端成型工艺中的应用,通用正交试验设计中极差分析和方差分析方法,确定了对医用导管尖端黏接力影响的关键因素,并确定了温度、推力、时间和材料种类对医用导管尖端黏接力的影响顺序,验证并确定了最佳的医用导管尖端成型工艺参数窗口。
2.案例分析
在临床应用中,为便于医用导管进入到患者血管中并减轻对患者血管的损伤,其尖端通常设计成锥形,由一段蓝色的软管和主体管焊接而成。如果医用导管尖端和主体管之间的黏接力过小,在产品使用过程中,尖端会因外力作用断裂在血管内,引发医疗事故纠纷。笔者采用正交试验设计方法对尖端成型工艺和材料进行试验设计,确定了最优的试验参数与材料。试验设计及试验过程如2.1~2.9所示[3]。
案例产品名称:一次性使用造影导管规格5F
主体管材料:PEBAX 5533
软管材料:PEBAX 5533+BaSO4(20%);PEBAX 5533+BaSO4(30%)
尖端成型设备:美国Vante model 4200 Saffire and model 4210
测试设备:伺服控制拉力试验机AI-3000
拉伸速度:50mm/min
2.1 试验目的
通过对尖端成型工艺的参数验证,寻找满足产品黏接力的工艺参数范围。
2.2 确定考察目标
考察目标Yi为尖端黏接力,该指标为望大指标,黏接力越大越好。
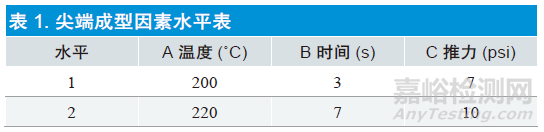
2.3 制定因素表
影响导管尖端成型的工艺参数有:成型温度、设备推力、保压时间。
影响因素的水平是根据材料供应商和设备供应商提供的经验值选定。
软管材料选的是PEBAX 5533+BaSO4(20%)。
见表1。
2.4 设计试验方案
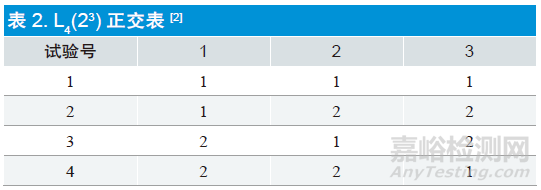
2.4.1 选择正交表,三因素两水平选取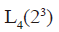
见表2。
2.4.2 表头设计,水平对号入座
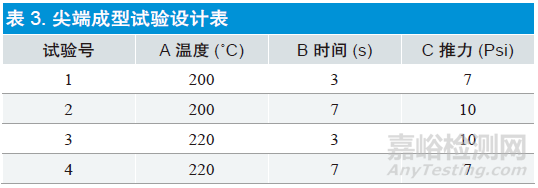
2.5 实施试验方案
依据设计好的试验设计进行方案实施,实施后的试验结果见表4。每组试验条件下样品数为10个,考察指标采用10组样品去掉最大值去掉最小值后的平均值。
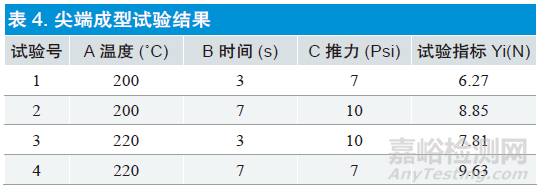
2.6 试验结果分析
对正交试验结果分析主要有两种分析,第一种是数据观察,直接看,可靠又方便。存在问题点是正交试验结果只能控制95%的试验结果,还有5%的结果在未进行试验组中,可以通过第二种方法进行计算验证确认。第二种就是算一算,通过计算,有效还简单。
通过表4的试验结果看到,温度220˚C,时间7s,推力7Psi时,尖端黏接力最大。
2.6.1 极差分析
见表5。
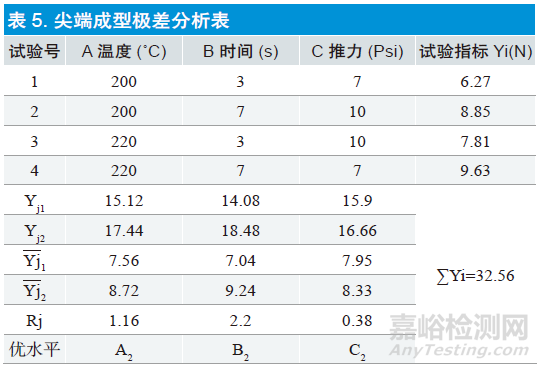
考察指标采用Yi 表示,用Yj1 表示某列因素对应1 水平各试验号试验的试验指标之和,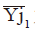 为其平均值。
为其平均值。
通过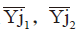 的比较,就可找到该因素最优水平(望大指标越大越好,望小指标越小越好),各因素的最优水平组合起来,就是对试验结果最有利的条件。本试验中各因素的最优水平为A2、B2、C2,所以对试验结果来说最优条件是A2 B1 C2。在
的比较,就可找到该因素最优水平(望大指标越大越好,望小指标越小越好),各因素的最优水平组合起来,就是对试验结果最有利的条件。本试验中各因素的最优水平为A2、B2、C2,所以对试验结果来说最优条件是A2 B1 C2。在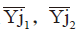 中数值最大者与最小者之差,即因素的极差,Rj表示。它反映了各因素水平变动时,试验指标变动的幅度。极差越大,说明这个因素对指标的影响越大,所以根据极差的大小就可以排出因素主次的顺序。在本组试验中对尖端黏接力影响力顺序为时间>温度>推力。
中数值最大者与最小者之差,即因素的极差,Rj表示。它反映了各因素水平变动时,试验指标变动的幅度。极差越大,说明这个因素对指标的影响越大,所以根据极差的大小就可以排出因素主次的顺序。在本组试验中对尖端黏接力影响力顺序为时间>温度>推力。
发现极差分析的最优组合与观察法看到的最佳工艺组合存在不符合的情况,这是因为正交试验试验组合是以最少的、合理的试验组合数来体现最大化(95%)的试验结果。
还有5%的试验结果是需要继续验证。通常情况下是观察法与计算法的结论是一致统一的。
2.6.2 方差分析
极差分析出各个因素对熔头黏接力的影响程度顺序。极差越小,影响程度越小。小的什么程度,可以忽略此因素,在节约成本的情况下,可以将这些不影响考察指标的因素进行成本最低化设置。这里就可以采用方差分析进行对试验设计分析。方差分析中,假定每一次试验都是独立进行的,试验结果都是服从正态分布的。方差分析中需要有误差项,三因素两水平加误差项选择七因素两水平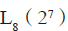 正交试验表。
正交试验表。
见表6。
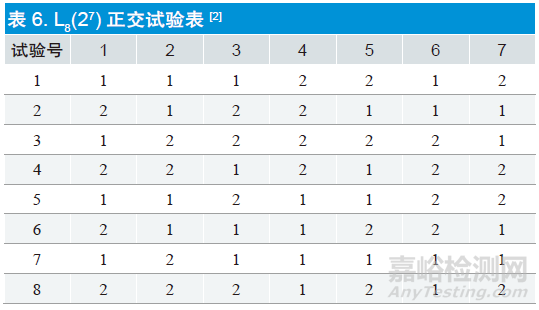
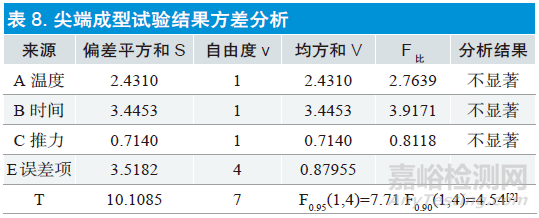
依据选择好的正交试验表,将因素水平填入试验表中,按照设计好的正交试验表进行试验,测试,出具试验结果。并进行方差分析。如表7、8 所示。
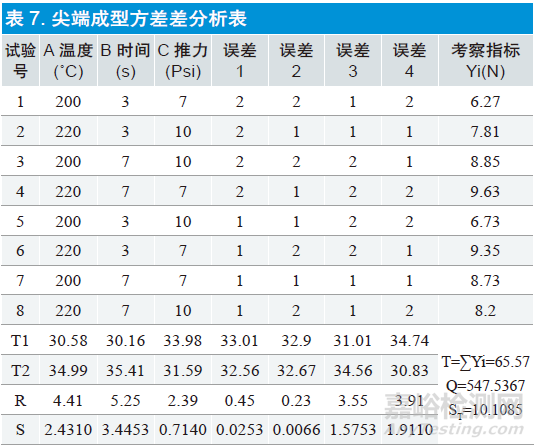
方差分析中每次试验结果不同,产生波动每次试验结果不同,产生波动,这是因为试验条件不同和试验中存在误差,总偏差平方和是用来描述这种波动的,计算公式为公式1:
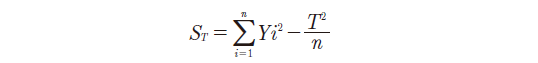
式中n 代表试验次数;T代表试验结果的总和;Yi 代表试验结果。
各影响因素的偏差平方和Sj的计算公式为公式2 :
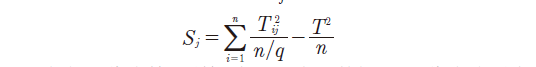
式中Tij 代表第j 列第i 水平对应的数据和;q 代表该列水
平数。
误差的偏差平方和Se的计算公式为公式3 :
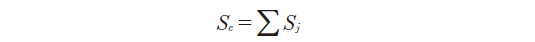
式中Sj代表各误差项的偏差平方和。
在方差分析中总自由度v 等于总的试验数减1,各个影响因素的自由度等于水平数减1,误差项自由度为总的自由度减所有影响因素的自由度和。各项均方和V等于各项偏方和除以各项自由度。F比等于各个影响因素的均方和除以误差项的均方和。
经查文献,F0.95(1,4)=7.71 F0.90(1,4)=4.54,此次试验的三个影响因素的F比小于这两个数值,说明尖端工艺选取的三个参数对尖端拉力这个考察指标都不是强相关影响因素。
通过极差分析得到温度、时间、推力对考察指标的影响因素为时间>温度>推力。最优组合为A2B2C2。通过对试验结果方差分析,时间、温度及推力对考察指标的影响都不是显著因素。还需要重新寻找对连接牢固度有影响的试验条件。经过大量数据推断,尖端熔头的材料选择对熔头的黏接力有直接影响关系。对此次试验进行了优化试验。
2.7 优化试验
通过对尖端熔头设备的参数验证,得知推力对熔头黏接力影响最小,在节省成本的原则下,设定设备的推力为7Psi。
在此基础上对材料的种类进行优化选择,软管材料选择了PEBAX 5533+BaSO4(30%)。再次通过正交试验,验证软管材料对熔头黏接力的影响程度。
2.8 试验分析
选择新材料试验结果如表9 所示。
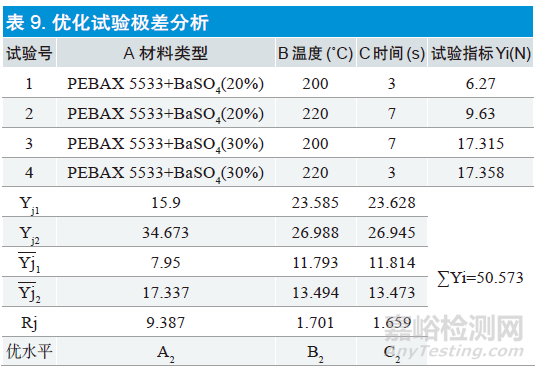
通过表9 极差分析得到材料类型的极差很大,对熔头断裂力影响很大。
2.9 结论
①温度、时间、推力、材料类型对产品尖端断裂力的影响程度顺序为材料类型>时间>温度>推力。
② 最优的尖端成型参数是材料类型为PEBAX5533+BaSO4(30%),温度为220˚C,时间是7s,推力是7Psi。尖端成型设备上参数是工艺结果考察指标的弱相关因素,结合设备参数对资源成本的影响,在制定工艺作业指导书时,将设备参数定为区间段,如加工温度为200~220˚C,时间设置为7~11s,推力设置为7~13Psi。材料类型是尖端黏接力的强相关因素,在工艺流程中需要严格把控材料类型。
2.10 确认验证
对2.9 中结论进行验证确认,选取四因素三水平试验设计表格(误差项不显示),试验数据如表10 所示。
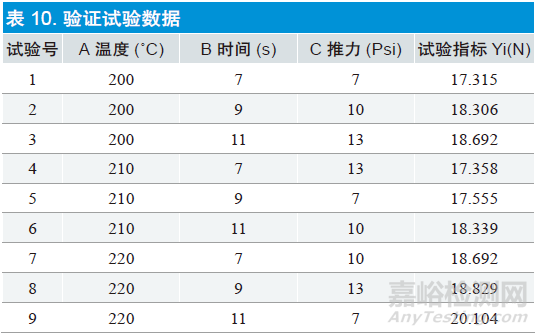
表10 看到,在设置的范围之内,产品尖端黏接力其尖端熔头拉力均在17N以上,满足产品性能需求,验证了正交试验设计分析结果的有效性。
3.小结
应用正交试验设计中极差分析和方差分析方法,确定了对医用导管尖端黏接力影响的关键因素,并确定了温度、推力、时间和材料种类对医用导管尖端黏接力的影响顺序,验证并确定了最佳的医用导管尖端成型工艺参数窗口,并通过实际参数测试验证了正交试验设计分析结果的有效性。本次案例将正交试验设计的思路与分析方法成功应用在医疗器械产品设计和开发过程中,保证设计和开发过程中工艺参数能满足产品质量需求,避免医疗器械不良品现象,节约资源成本,符合《医疗器械生产质量管理规范》(总局公告2014年第64 号)中设计开发阶段要求。
参考文献
[1] 汪仁官. 设计和生产中的质量管理——关于田口玄一博士的管理思想和方法[J]. 数理统计与管理,1982,1(3):17-21.
[2] 梁国明.ISO9000 族标准常用统计技术方法43 种[M]. 北京: 中国标准出版社出版,2011:78-90.
[3] Montgomery DC. Design and analysis of experiments [M].New York: Wiley,1984:1-14.

来源:中国医疗器械信息