您当前的位置:检测资讯 > 生产品管
嘉峪检测网 2020-05-12 10:13
为帮助企业建立合规的产品质量管理体系,本文列出了医疗器械质量管理体系的建立及要点,供大家参考及自查。
1、为什么要建立质量管理体系
质量管理体系是个系统工作,除了我们常说的文件及记录外,还有关键的管理控制子系统,设计控制子系统,生产制造子系统,需要与公司的培训系统,绩效系统,营销系统等相结合。基于此,质量管理体系对企业来说,是企业多年运行的标准化沉淀产物。
另外,实施质量管理体系的终极目的,是为了降低风险。因此,对于企业来说,做好系统管理是最重要的,也容易达到实施体系的目的:预防为主,降低风险。
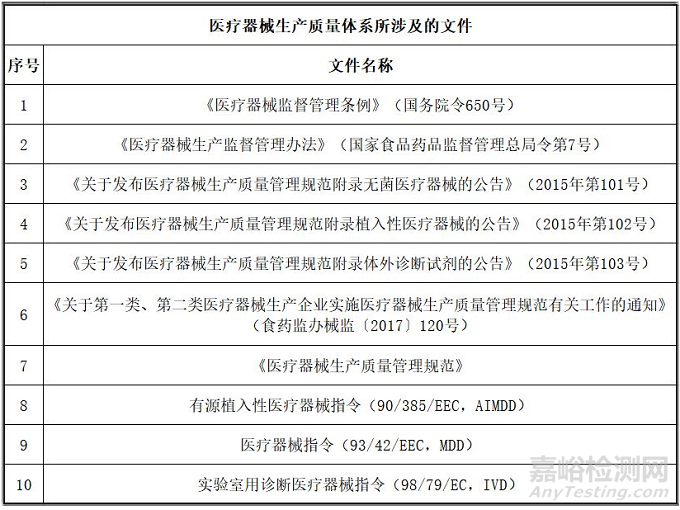
质量管理体系涉及的法规文件
如何建立质量管理体系文件
企业建立质量管理体系,决策层起着关键作用,其应在企业内形成一种重视质量、关注顾客的氛围,并提供充足的资源,为推行ISO13485标准做好领导作用。决策层需要掌握的ISO13485知识至少应包括:ISO13485标准的产生背景、发展形式和趋势,ISO13485质量管理体系的成功组织案例,质量方针和目标的设定,质量意识的强化、管理职责、质量策划、管理评审、质量成本管理、质量管理体系与企业管理其他部分的关系等。企业建立质量管理体系的总体流程如下。
建立质量管理体系的要点
1.企业应按照《医疗器械生产质量管理规范》的要求,结合产品特点,建立健全与所生产医疗器械相适应的质量管理体系。
2.质量体系管理涵盖的范围包括设计开发(GLP)、生产(GMP)、销售和售后服务(GSP)。
3.结合实际的人员配置、机构设置、人员的基础素质等,在不违反《医疗器械生产质量管理规范》内容的前提下,最大限度地发挥主观能动性。
4.质量管理体系要将风险管理贯穿产品全生命周期。

来源:Internet


