您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-06-23 11:01
导读
研究流程图
参考文献作者及单位
美国FDA研究与标准化办公室ORS
建模与模拟方法的用途
案例摘要
有文献报道:华法林结晶包合物中异丙醇的减少和酸性pH条件(比如4.5)下溶出的变慢将对其体内的PK有显著的影响。
FDA仿制药办公室等研究人员通过建模与模拟的方法,探讨华法林结晶包合物的质量控制应采用pH 4.5还是pH 6.8的溶出介质来评价其生物等效性。
本研究通过构建基于生理学的机制性吸收药代动力学模型,并将制剂相关的参数和体外溶出相关数据输入到模型中。模型的参数敏感性分析表明:溶解度、粒径、密度不是影响华法林在体内的PK行为的关键因素,pH 4.5溶出介质中的溶出与体内PK相关性不强,但在pH 6.8的溶出介质中,其溶出速率和溶出能力与体内PK有较强的相关性。
虚拟生物等效性试验表明,经加速降解实验(高温高湿处理)后的华法林钠片在pH 4.5溶出介质中的溶出速率将变慢,但不影响生物等效性结果;只要在pH 6.8溶出介质中的溶出与未经加速降解的制剂的溶出相似,就能确保二者生物等效。
研究亮点
该研究当前已获得哪些信息?
研究表明,在短时间暴露于较高的温度和湿度之后,华法林钠片可能容易发生晶型的变化,但是这种药品质量的变化带来的临床意义(生物利用度)是未知的。
该研究想解决的问题是什么?
本研究采用建模和模拟评估药品质量的变化对其体内行为的影响。
该研究能增加哪些知识?
除了获得关于药品质量对华法林体内PK性能影响的新见解之外,该研究还显示了PBPK机制性吸收建模与模拟在科学研究中的重要作用。
将如何改变药物发现、开发或治疗的决策?
因制剂处方、生物药剂学的变更可能导致药物生物利用度的改变,可通过建模与模拟工具评估该变化给患者带来的潜在风险,当达到的风险水平可能产生新的体内BE或生物利用度数据时,会影响药物开发和药物监管方面的决策。
基于生理学的药代动力学的建模与模拟已经在药物制剂开发和监管审评方面展现出实用性,基于生理的机制性吸收模型连接了药物的理化性质、制剂的体外行为和体内行为。在生物等效性(BE)、建立体内外关系和药品开发中的质量源于设计方面,机制性的吸收模型已被用于研究处方、体外行为对口服给药后药物体内行为的影响。
在本文中,FDA仿制药办公室将以华法林钠片为例,说明建模和模拟在探究仿制药BE问题中的作用。华法林属于弱酸,pKa 5.05,在低pH条件下溶解度较低,高pH条件下溶解度较高。华法林钠是华法林的钠盐,以无定型形式或结晶包合物形式存在。结晶包合物是一种华法林钠异丙醇(IPA)复合物,在高湿度(RH)环境中IPA减少,结晶包合物转变成无定型并且此转变不可逆。对于浴室这种高湿度的环境,是否会引起IPA的减少从而影响药物的体内行为,这是接下来的研究方向。
2. 研究方法
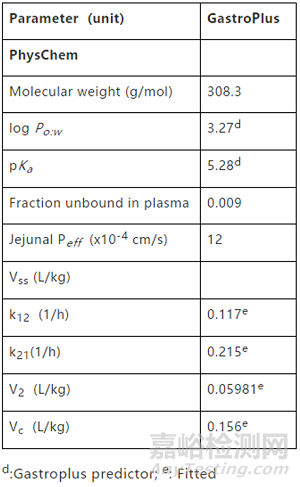
建模参数:
为了研究酸性pH条件下体外溶解速率降低影响药物制剂的体内行为,采用建模与模拟的方法搭建了基于生理的吸收模型。建模工具包括GastroPlus v9.0等软件;GastroPlus采用Johnson溶出模型,双阶段溶出结果使用Z-factor模型进行数据的整合。
对溶解度、粒径、密度、剂量、Z值进行了敏感性分析,并进行三维参数分析以探究pH值4.5和pH 6.8的Z值之间的相互作用及其对Cmax的影响,还对密度、粒径进行了三维参数敏感性分析,以探索两者之间的相互作用及其对Cmax的影响。
通过虚拟BE试验模拟各比较组的BE通过率,采用30名健康受试者双处理、两序列、四周期、完全重复交叉体内虚拟BE试验设计。随机选择1,200名虚拟健康受试者基于Z因子模拟未经加速降解或经加速降解的PK,对于每个BE模拟试验,随机选择30名受试者,并且对每个比较组进行100次虚拟BE模拟试验。
2.3 体内研究
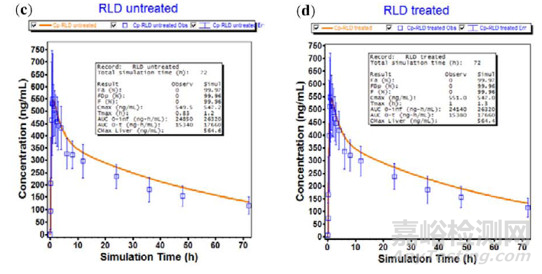
C:5 mg储存在约20-25℃的密闭容器中的香豆定(参比制剂未经加速降解);
D:5 mg储存于40℃、75%湿度的开口瓶中24小时的香豆定(参比制剂经加速降解)。
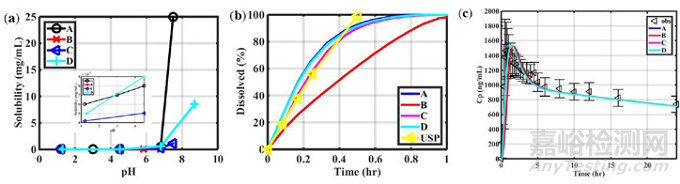
使用PBPK机制性吸收模型预测华法林的PK曲线,并将模型用于分析不同pH对应的溶解度和Z因子对华法林PK曲线的影响。参数敏感性分析表明,华法林的PK曲线对溶解度(如Figure 2c)、粒径和密度的变化不敏感。低溶解度会延迟Tmax,而Cmax和AUC对溶解度的变化不敏感。比较溶解度-pH曲线(Figure 2a)和体内溶出曲线(Figure 2b),可知即使来源B的溶解度很低,但在给药后的1h体内也能达到完全释放。参数敏感性分析还表明华法林的PK参数如AUC、Cmax和剂量成正相关,而且华法林也是窄治疗窗药物,最近美国药典也规定了华法林钠片含量不得少于95.0%且不超过105.0%。
使用图 2中的溶出曲线预测华法林的体内PK,BE模拟结果表明所有比较组都具有高通过率,结果如下图,所有的比较组通过点估计(PE)计算都接近1。
图2.(a)四种不同来源的溶解度数据;(b)四种不同来源的溶解度数据对应于ACAT模型(高级房室吸收与转运模型)中的体内溶出曲线;(c)使用a图中的溶解度数据通过ACAT模型预测到的体内PK曲线。
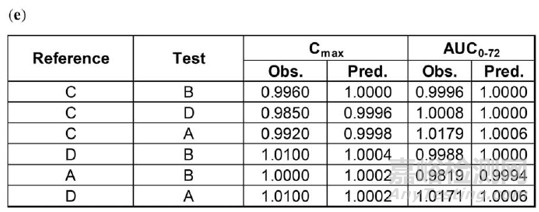
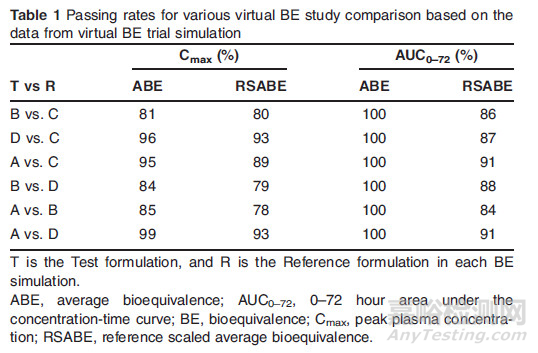
各组比较的统计结果如下Table 1,使用ABE标准(平均生物等效性标准,90%的置信度)每个比较组的Cmax BE通过率均高于80%,AUC通过率均为100%;按照RSABE(reference scaled average bioequivalence)标准,A vs.B比较组通过率最低,Cmax通过率为78%、AUC0-72通过率为84%。
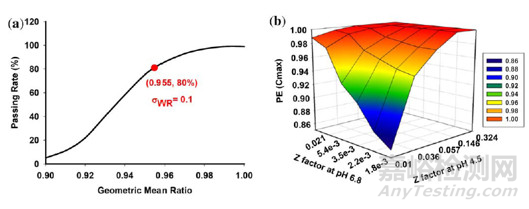
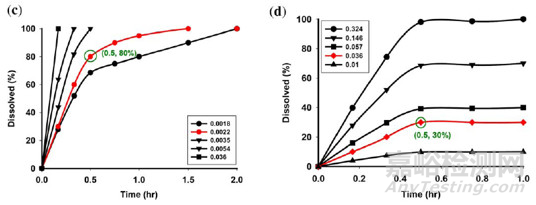
PBPK模型用于制定体内外相关的溶出空间,通过多个参数敏感性分析探索确保BE的溶出空间,测试了pH 4.5和pH 6.8条件下的多个Z因子以产生虚拟溶出曲线,如下图(Figure 4b)展示了在pH 4.5和6.8条件下PE(Cmax)与Z因子之间的关系三维图,该区域的大部分空间PE均在0.95-1.00的范围内。根据RSABE标准,如果Cmax的PE为0.955且合格率为80%(Figure 4a),则在pH4.5条件下30分钟至少释放30%,在pH6.8条件下30分钟至少释放80%(Figure 4c, d)。
图4.对pH 4.5和6.8对应的Z因子进行三维敏感性分析,(a)使用RSABE的方法评估几何平均比(GMR)对假设的窄治疗指数药物(rWR=0.10)的影响,(b)对pH4.5和6.8对应的Z因子进行参数敏感性分析,(c)在pH6.8下各Z因子对应的虚拟溶出曲线,(d)在pH4.5下各Z因子对应的虚拟溶出曲线。
3.3 体内研究结果
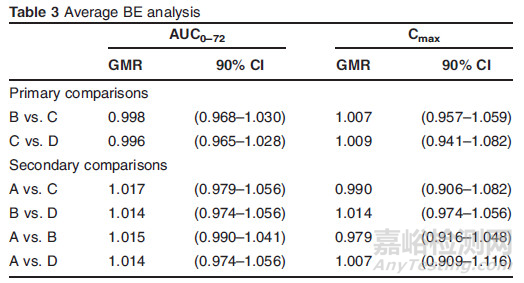
4种制剂的体内PK曲线较为接近,主要的药动学参数如下表,且AUC0-72、Cmax的CV%值均小于30%,按照ABE标准,各比较组都是生物等效的,如Table 3。
4. 结果与讨论
5 应用软件与模块
参考文献
英文原文:
Zhang, X. , Wen, H. , Fan, J. , Vince, B. , Li, T. , Gao, W. , Kinjo, M. , Brown, J. , Sun, W. , Jiang, W. and Lionberger, R. (2017), Integrating In Vitro, Modeling, and In Vivo Approaches to Investigate Warfarin Bioequivalence. CPT Pharmacometrics Syst. Pharmacol., 6: 523-531



来源:Internet


