您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-08-19 09:44
前言
笔者在药品研发从业多年,自己写过很多质量标准,也见过很多其他人写的与合作方提供的质量标准;自己犯过很多错,也见过很多他人犯的错,见的多了对于药典格式质量标准如何撰写也算略有心得,拿出来和读者分享,如有不当或疏漏之处,敬请方家指正。
下文说的药典格式专指中国药典格式,用于申报其他国家的质量标准请按照该国相关要求撰写。
本文内容仅适用化药质量标准撰写过程。
编写药典格式质量标准要点
1、不得使用口语,应使用规范的书面的表述方式
质量标准为书面文件,有其表述方式的规范要求,不应使用日常在实验室交流过程中使用的口语内容,如“定容、容量瓶、胖肚吸管”等。以口头交流常用的“定容”为例,药典格式质量标准的表述方式应为“稀释至刻度”。
2、使用统一的表述方式,避免使用同义但不同于习惯表述的词句
药典格式质量标准的很多内容有其习惯或者统一的表述方式,如果不同于该方式,意义并不会让人产生误解,但是会让人觉得有些怪异。这类似于看习惯了职业装,眼前突然出现一个杀马特一样。举个例子,如在质量标准中列出了色谱柱的品牌型号规格等参数,后面一般可以加一句“或效能相当的色谱柱”,如果写成“等效柱”,意义并无不同,但是让人觉得非常奇怪。
撰写药典格式质量标准时,应当注意某些项目具有特定的表述方式,甚至是某个动词与其后的宾语都是固定的搭配,如“取本品”、“加稀释剂溶解”、“用十八烷基硅烷键合硅胶为填充剂”等。
3、不得出现“/”符号
在表述浓度、流速等信息时,不得表述成“0.5mg/ml”与“1.0ml/min”的形式,应为“每1ml中含0.5mg”与“每分钟1.0ml”。
4、药典格式质量标准不同于SOP
质量标准中很多时候无需对参数进行具体规定,如色谱柱品牌型号规格、流速、柱温等。这些内容可以在内部SOP中规定,但是药典格式质量标准中可能没有相关内容。
编写药典格式质量标准常见错误分析
下文以液相色谱法为例,说明撰写药典格式质量标准常见错误以及正确的表述形式。
1、溶液配制
在撰写药典格式质量标准时,常见的错误与正确表述方式见下表:

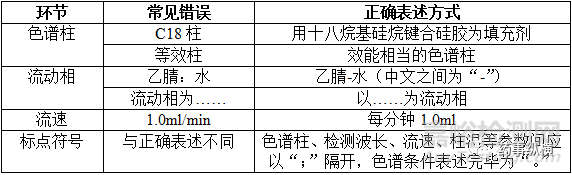
2、色谱条件
在撰写药典格式质量标准时,常见错误与正确表述方式见下表:
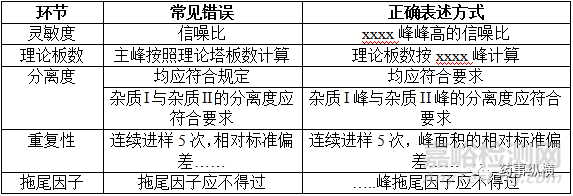
3、系统适用性实验
在撰写药典格式质量标准时,常见错误与正确表述方式见下表:
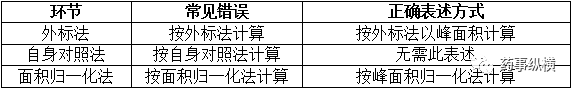
4、计算方法
在撰写药典格式质量标准时,常见错误与正确表述方式见下表:
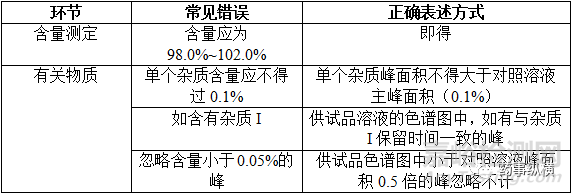
5、可接受标准
在撰写药典格式质量标准时,常见错误与正确表述方式见下表:

来源:药事纵横


