您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-09-30 08:42
分析方法应用在药物研发的不同阶段,其目标与目的各不同,不同药物研发阶段对应着不同特点的分析方法开发。基于质量源于设计的理念,实验设计在分析方法开发中的应用越来越多,它帮助制药分析人员更多的理解和掌握分析方法知识,从而不断提高产品质量控制手段和策略。
分析方法开发的不同阶段
候选药物开发阶段,分析方法用于支持临床前的药物纯度与含量的评价,处方前研究的评估,以及原始早期化合物稳定性研究。这个阶段分析方法以检测为主,基本不需要有过多的设计与开发,试错法完全可以满足当前阶段要求。根据化合物的结构特点,筛选找到合适的检测器和色谱系统,方法有足够的专属性,能满足它的目标。
临床研究阶段,在药物完成初步筛选和安全性评估后,得到官方的批准进入临床试验。这个阶段的分析方法需要有足够的能力完成化合物鉴别、纯度、表征、含量,以及药物效价的评估。该阶段分析方法需要有简单的验证或者确认,以确保方法的专属性、可靠性、准确性和精密度。
药物上市后研究阶段,分析方法常常发生不同实验室的技术转移,因此方法的耐用性在该阶段需要重点考察。经历前面临床研究的稳定性考察,分析方法得到进一步优化,其专属性和准确性将得到进一步的确认,以用于商业化产品的放行和稳定性考察。
分析质量源于设计(AQbD,Analytical Quality of Design)
传统分析方法开发采用的试错法用于单因素单水平的试验,需要不断摸索、不断重复试验,最后幸运地找到一个合适的方法。这种方法开发的模式比较盲目,费时费力费成本,方法开发时不会考虑各参数的空间,耐用性差,不同实验室转移时常出现方法测试不能重现的现象。
现代分析方法开发是基于分析质量源于设计的理念,对方法进行系统性的研究,多因素多水平同时评估。利用方法开发工具和统计学软件进行数据的分析与处理,最后得到一个高性能的方法。这类方法耐用性好,设计空间可靠,准确性高,收集的方法知识多,使用的生命周期长,大大节省人力和时间成本。
新药研发重点关注药物的质量可控性、安全性和有效性。通过质量源于设计和过程分析等工具,帮助制药行业不断提高药品研发的质量。ICH Q8、Q9和Q10紧密联系,为药物的开发研究、质量风险管理,以及制药质量体系提供了很好的理论和实践指南。ICH Q11为原料药的合成工艺开发、设计和质量提供了实施指南。
相对于原料药工艺开发的设计,ICH目前还没有具体的指南用于指导分析方法开发,在不久的将来,ICH Q14将为分析方法开发提供实践指南,内容包含有分析质量源于设计的部分,分析行业人员期待该指南的正式发布。
相对于工艺的质量源于设计过程,分析方法的开发设计流程类似,如图1。首先找到方法中分析目标概况→定义关键质量属性→对方法进行初步的风险评估→方法优化和实验设计→找到方法的可操作和设计区域→得到方法的控制策略,进一步风险评估→基于QbD的方法验证→最后进行持续的方法监测。
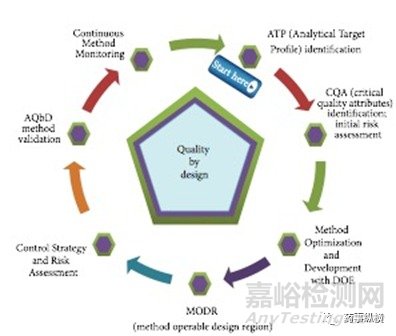
图1:分析QbD工具和生命周期
分析方法的QbD手段有三种方式:实验设计、风险评估和过程分析。实验设计和风险评估是实践中较为常用的手段。
在进行方法开发实验设计时,首先对方法进行初步的风险评估,找到影响方法的关键变量参数,设计关键因素不同水平的实验,得到一系列的数据,使用工具软件导入与处理这些分析数据,进行色谱数据的统计学分析,建立数学模型,最后找到分析方法重要参数的可设计空间。
分析方法开发实验设计(DoE,Design of Experiment)
以有关物质HPLC方法为例,它的分析目标概况大致包括下面内容,如表1:
表1:有关物质HPLC方法通用分析目标概况
| 序号 | 有关物质方法要求 | 序号 | 有关物质方法要求 |
| 1 | 分析物的数量(API和杂质) | 12 | 检测器(紫外/示差折光/蒸发光散射/电雾式) |
| 2 | 所有分析物的分离 | 13 | 建立相对保留时间/相对响应因子 |
| 3 | 流动相(缓冲液和有机溶剂) | 14 | 流速 |
| 4 | 洗脱方式(梯度或等度) | 15 | 进样体积 |
| 5 | 样品浓度 | 16 | 柱温箱温度 |
| 6 | 样品溶剂 | 17 | 运行时间 |
| 7 | 对照品和样品溶液稳定性 | 18 | 系统适用性参数选择与限制 |
| 8 | 样品制备过程(释释和超声过程) | 19 | 检测限和定量限浓度的确定 |
| 9 | 过滤或离心 | 20 | 杂质计算方法 |
| 10 | 杂质标准限度 | 21 | 准确度(回收率) |
| 11 | 色谱柱类型(固定相或尺寸) |
对上述的21个分析目标概况进行分析,用理论知识和实践经验找到关键影响因素,减少变量,简化数学模型。
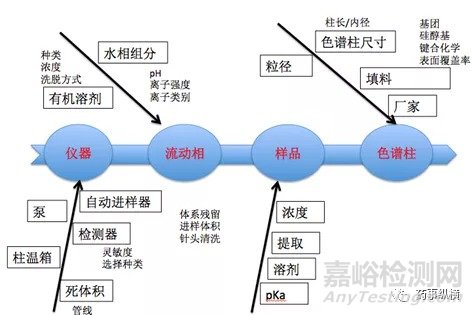
图2:影响有关物质分析方法的因素
对图2中影响方法开发的四个因素,进行初步的风险评估,得到实验设计中具体的关键影响因素,如表2。
表2:有关物质HPLC方法的风险评估分析
| 影响选择性因素 | 严重性 | 发生率 | 检测 | 是否关键(Y/N) | |
| 色谱柱 | 填料(硅胶) | 3 | 1 | 1 | N |
| 键合化学 | 3 | 2 | 1 | N | |
| 厂家 | 1 | 1 | 1 | N | |
| 流动相 | pH | 3 | 2 | 2 | Y |
| 有机溶剂比例 | 2 | 2 | 3 | Y | |
| 流速 | 3 | 2 | 2 | Y | |
| 样品 | 溶解性 | 1 | 1 | 2 | N |
| 仪吕 | 检测波长 | 3 | 1 | 2 | N |
| 柱温 | 3 | 2 | 2 | Y | |
通过风险评估,确认影响分析方法选择性的关键影响因素:流动相的pH,有机溶剂的比例,流速和柱温。根据风险评估确定的影响因素对方法开发进行实验设计(DoE, Design of Experiment)。
实验设计是应用统计学的一个分支,通过计划、执行和分析,以及解释一系列控制性的测试,用于评估对工艺参数的影响因素。实验设计是一个非常有用的数据收集和统计分析工具。
用于筛选的实验设计工具包括全因子设计, 部分因子设计,placket-burmann,混料设计和最优设计等。用于优化的实验设计包括Central composite design, Box Benken和Doehlert等。
分析方法实验设计时,通过不同因素不同水平实验得到的响因值,建立因素与响因值之间的回归模型关系。比如对单因素水平流动相pH值的筛选:不同pH值条件下,可以得到不pH条件下化合物之间的分离度,通过系列的pH值和分离度数据,建立pH值和分离度的数学回归模型,从而找到化合物在某pH值条件下的最佳分离度,同时还可以找到满足分离要求的pH值空间范围。
常用的色谱优化实验设计软件包括,Drylab,ACD ChromManager和ChromSword。
简单的实验计为单因素设计。比如,筛选方法的pH值,分离度为关键属性(Rs),三个水平pH2.9、3.5和4.1。只需要进行三次实验,得到的分离数据建立单因素三水平的模型,通过模型找到最佳分离并预测pH值。
稍微复杂一点的分析方法开发,需要对两个因素两个水平的考察。比如梯度和温度,各两个水平。需要2*2,4次实验,建立模型用于预测不同梯度和温度条件下的分离情况,找到两个因素的最佳范围。
再复杂一点的方法设计,在上面两因素两水平的条件下,引入一个因素pH值,三个水平,这时需要2*2*3,12次实验,建立模型预测三个因素的最佳范围。
现代实验设计的色谱工具软件已经发展的非常强大, 可以建立多因素多水平的实验模型,建立二维、三维、甚至多维的模型图,预测复杂的成分分离,建立实验条件的耐用性范围。
关于有关物质分析方法实验设计实例
选择方法中的四个关键方法参数:梯度程序,柱温,流动相pH,以及有机相组成及比例,每个参数选择不同个水平,具体的流程如下图3:
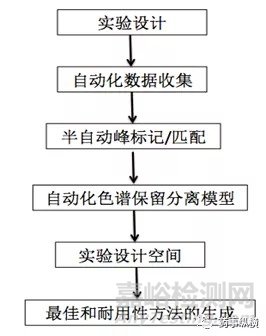
图3:方法开发实验流程
分析的化合物包括扁桃酸、邻苯二甲酸、间羟基苯乙酸、异香兰素、对乙酰氨基酚、对羟基苯乙酸、苯甲醇、香兰素酸、4-羟基-3-甲氧基苯甲醇及其它未知成分。
实验条件为梯度程序两个水平:30min和90min,色谱柱温度水平:30摄氏度和60摄氏度,流动相水相离子浓度100mM三个pH水平:2.4、3.0和3.6。流动相有机相组成三个水平:纯乙腈,纯甲醇,乙腈:甲醇(50:50)。
梯度程序和温度两个水平,pH值和有机相比例各三个水平,共36次实验,得到36组色谱数据,四因素设计如图4。

图4:分析方法开发:四因素优化实验设计
得到36组数据后,使用工具软件对数据中的色谱峰分析、识别与标记。匹配完成,所有产生的色谱数据将自动导入工具软件中,得到分离二维图(图5)。每个图对应固定的pH值和有机相,以及梯度和柱温两因素模型图。在各图中可以找到分离度大于1.5的各因素的空间和范围。
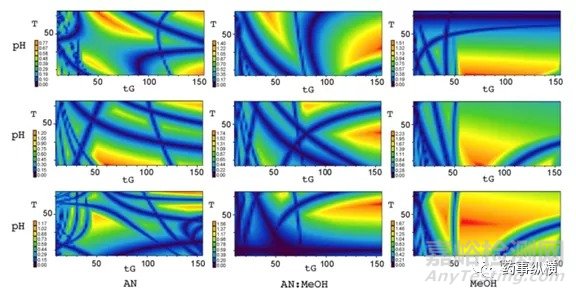
图5:梯度与温度的二维分离回归模型图
不同梯度、温度、pH和有机相比例的模拟结果如下表3:
表3:不同有机相和pH对应的分离度
可以看到,不同pH值,pH3.0分离度最高,pH3.0次之,pH3.6最低;不同有机相,甲醇分离度最高,混合溶剂次之,乙腈最低。
在pH3.0的条件继续优化温度和梯度程序,找到最优的梯度和温度,软件模拟和真实实验色谱分离如下图6,结果非常接近:
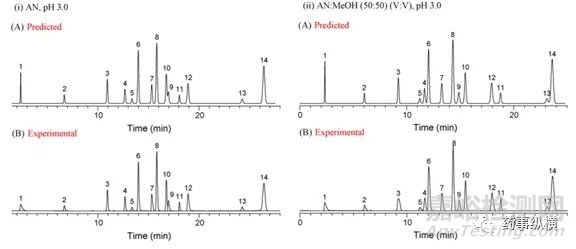
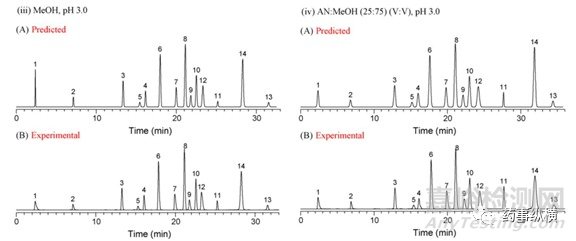
图6:优化温度和梯度条件下的预测和真实色谱图
通过上面的多因素与多水平的优化,能找到多对关键色谱分离对,说明在分析方法开发时,尤其是复杂的有关物质分离,固定一对分离对是很难实现的。通过软件建立分离模型,可以找到多对分离对的设计空间,如图7。

图7:移动的关键色谱分离对
在工具软件中,可以通过多因素多水平的实验,建立三维的模型。上例中在pH3.0条件的三维模型图,如梯度、温度和有机相比例,能够找到温度、梯度和有机相比例三个因素的色谱分离耐用性范围,如图8。
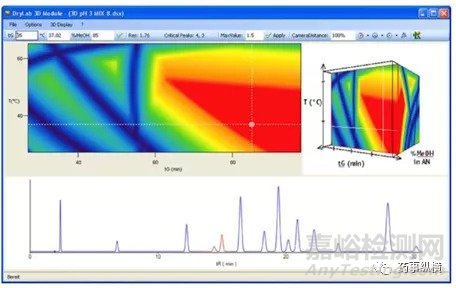
图8:三因素三维模型图
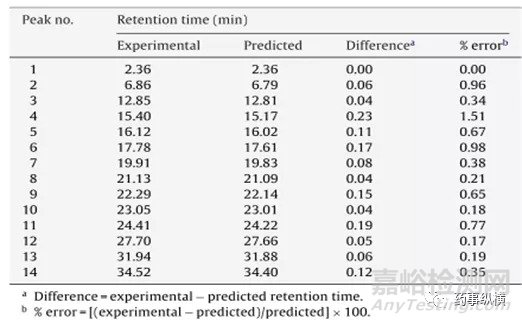
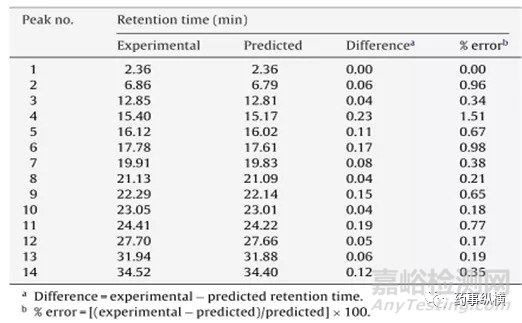
通过建立三维模型图,对实验中实际产生的各峰保留时间与模型中预测的保留时间进行对比,如表4,两者的相关性良好:
表4:在pH3.0,有机相ACN:MeOH(25:75),柱温42摄氏度,梯度120min,条件下各峰保留时间和模型预测的保留时间
运用软件工具,对梯度和流速进一步的优化,最终得到20min内实现14个组分优良分离的条件,如图9。
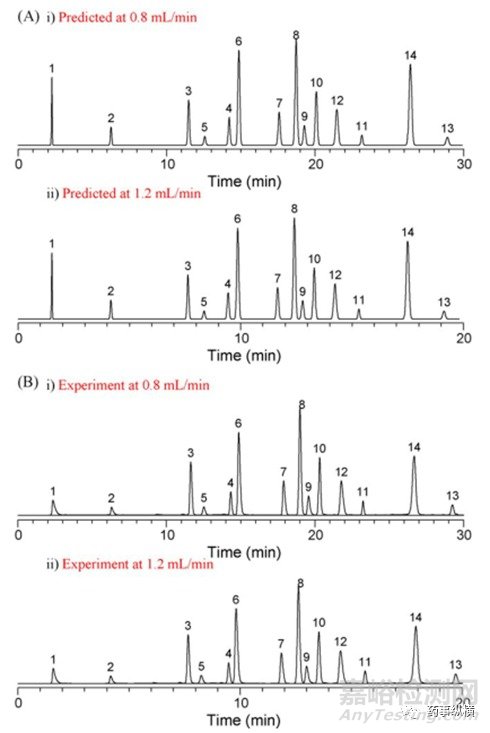
图9:保留时间的最终优化
该实例充分运用分析方法QbD理念,通过实验设计,大幅减少实验的次数,仅用了36次实验,通过多因素多水平建立的分离模型,提高色谱分析工作效率,得到的分析方法具有良好的耐用性范围,最佳分离度,以及适当的保留时间。
结束语
FDA相关专家认为,通过分析质量源于设计,可以帮助制药专业分析人员更多地了解和理解产品工艺参数,收集影响产品风险的知识,确认产品的工艺和质量风险,最终帮助制药人员用于产品工艺和质量持续性改进和生命周期的管理。
参考文献:
1.Analytical Quality by Design Approach to Test Method Development and Validationin Drug Substance Manufacturing. N.V.V.S.S.Raman, et al. Journal of Chemistry,2015.
2.USP: ICH guideline Q14 Analytical Procedure Development, Amanda Guirldelli, 2018
3.QbD Considerations for Analytical Methods – FDA Perspective, IFPAC AnnualMeeting, Baltimore, Sharmista Chatterjee, January 25, 2013.
4.Aspects of the “Design Space” in high pressure liquid chromatography method development.I.Molnar,2010. Journal of Chromatograph A.

来源:药事纵横


