您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-12-27 10:17
本研究首次报道了基于人工合成受体可选择性捕获及释放肿瘤细胞的唾液酸印迹温度响应性水凝胶界面。该智能水凝胶表面不仅可以通过识别肿瘤表面过表达的唾液酸分子实现有效捕获真实血液中的肿瘤细胞,还可以通过降低温度消除识别位点的方式来无损释放捕获的细胞。与传统非生理兼容性的细胞捕获与释放,该材料其具有非侵入性的外部刺激响应性,更高的捕获释放效率、细胞选择性及稳定性,对基于细胞的癌症诊断具有很大的应用前景。
01、研究内容简介
分子识别介导的各种细胞进程是生理学和病理学的中心。然而,天然分子识别系统,如受体-配体或抗原-抗体相互作用,除了物理化学性质不稳定和不易储存外,它们的分离和纯化通常费时且成本较高。分子印迹技术(Molecular imprinting technology, MIT)制备的人工受体可模仿细胞过程中发生的自然分子识别,并能触发选择性细胞识别。唾液酸(Sialic acid, SA)是细胞膜蛋白或脂质聚糖中的关键成分,肿瘤细胞表面过度表达的SA残基提供了通过定制具有特定SA识别的MIP来产生细胞亲和力的方法。本工作提出的具有SA识别能力的印迹水凝胶,将MIT从简单的分子分离提取应用拓展大到选择性细胞分离,并通过引入热响应性poly(N-Isopropylacrylamide) (PNIPAAm) 作为水凝胶骨架,实现选择性捕获及无损释放肿瘤细胞(Fig.1),展现了MIT在医学诊疗的潜力。
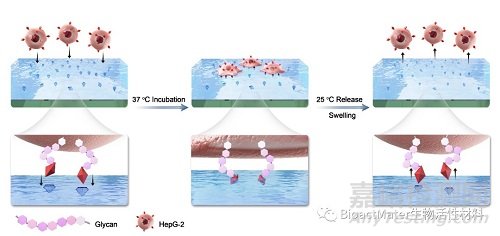
Fig. 1. Thermo-responsive SA-imprinted hydrogel layer enables selective capture and release of cancer cells (e.g., HepG-2, human liver carcinoma cells) through surface molecular specificity towards the overexpressed SA on the glycan terminal of cell membrane proteins.
该工作利用“三明治”结构法,在石英片表面制备了一层微米级别的SA印迹水凝胶(Sialic acid-imprinted hydrogel, SIH),此外还制备了对应的非印迹水凝胶NIH(Non-imprinted hydrogel)。由于SIH表面含有可特异性识别肿瘤细胞表面SA残基的选择性印迹空腔,因此可用于特异性捕获过度表达SA的肿瘤细胞(Fig. 2)。
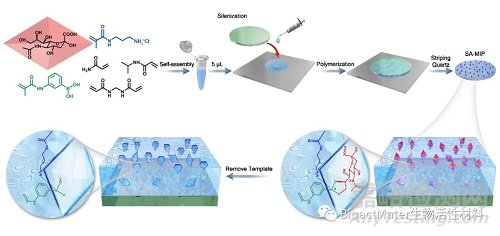
Fig. 2. Strategy to create SA-imprinted sites (i.e., SA-recognition) on thermo-responsive hydrogel layer by means of molecular imprinting on quartz substrate.
文章首先接着通过测试SIH和NIH的SA重新结合特性来确定其印迹机制。在测试浓度范围内,SIH水凝胶可结合的SA比相应的NIH多(Fig. 3A)。进一步的等温吸附实验表明,在一系列的SA浓度范围内,与NIH相比,SIH显示出显着更高的SA结合能力(Fig. 3B,C)。由于这些基于PNIPAAm的水凝胶具有温度敏感的的表面润湿性和内部结构变化特性,文章进一步考察了它的温度响应性SA识别能力。在37 oC下,SIH水凝胶的SA结合能力比NIH水凝胶高2.4倍。当温度降低到25 oC时,SIH和NIH的SA结合力均显着降低,并且SIH的降低幅度远大于NIH。此外,在25 oC时,SIH和NIH之间的结合能力无显著性差异,证明得到的SIH具有温度响应性SA识别能力(Fig. 3D)。
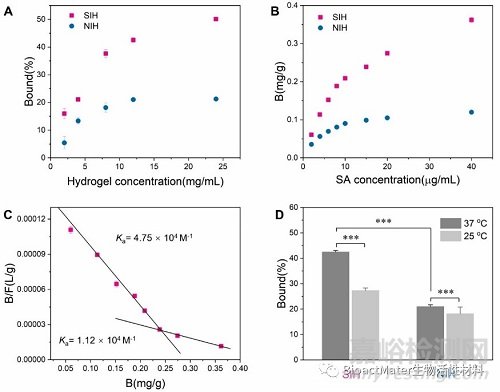
Fig. 3. (A) Equilibrium bindings of SA in PBS (10 μg/mL) on different amount of SIH or NIH. (B) Binding isotherms of SA onto SIH or NIH (24 mg/mL) in PBS over a SA concentration range of 0–40 μg/mL. (C) Scatchard analysis of the binding isotherms. (D) Thermo-responsiveness of the binding capacity.
文章随后研究了SIH和NIH对模型肿瘤细胞HepG-2的捕获和释放特性。HepG-2是膜表面过度表达的一类肝癌细胞。研究发现,SIH和NIH上捕获的HepG-2细胞数量均呈时间依赖性,同时发现具有SA印迹位点的SIH能够捕获大量细胞,与NIH上的细胞数量对比明显更多(Fig. 4 A-B)。由于SIH中的SA识别位点具有温敏性,即SIH表面在低温(例如25 oC)下会失去其SA结合能力,因此在降低体系温度后,30分钟内可以观察到细胞从SIH表面快速脱离(Fig. 4 C-E)。这种现象表明具有温度响应性SA结合能力的SIH水凝胶层可以有效捕获SA过度表达的肿瘤细胞,并能通过生理可接受的温度转变方法快速释放它们。这一高捕获效率和快速释放速率的结果表明,基于MIT的温敏性智能平台在选择性收集肿瘤细胞方面的潜力。
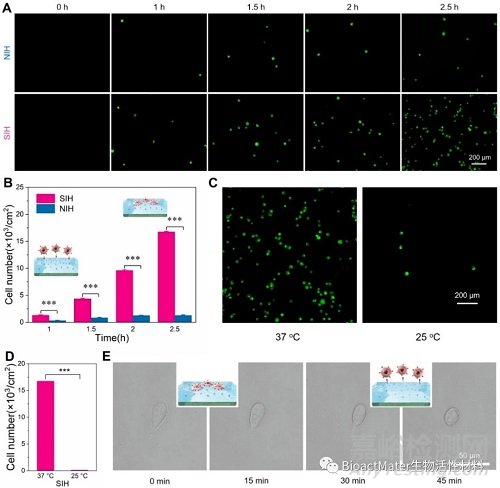
Fig. 4. Cancer cell capture and release. (A) Time-dependent cell capture by the SIH and NIH hydrogel layer (HepG-2 cell, DiO-pre-staining, green). (B) The numbers of captured HepG-2 at different time intervals. (C) Temperature-induced cell release. (D) Cell release efficiency. (E) Details of the captured cells during the capture and release process.
作者还考察了在一个捕获/释放周期后,所收集得到的细胞的活性变化,因为这是后期细胞分析肿瘤精确诊断的关键。作者将回收得到HepG-2细胞重新培养,发现它们可以重新粘附在培养板上,并且发现其细胞生长行为与未经处理的原始细胞相当(Fig. 5A)。活死细胞染色结果也表明,回收的肿瘤细胞不受温度转变过程的负面影响。原始细胞和回收细胞并无显著性活性差异(Fig. 5 B-C)。这进一步证实了用于细胞捕获和分离的热响应水凝胶层的非侵入性以及高度的生物相容性。
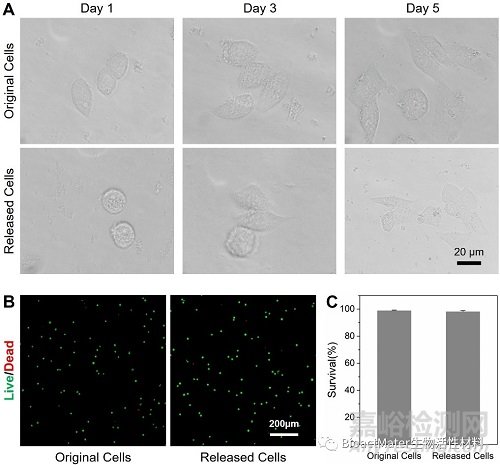
Fig. 5. The biocompatibility of thermo-responsive cell harvesting process. (A) The proliferation profiles of the original and recovered HepG-2 cells in 5 days. (B) The fluorescent images of HepG-2 cell after live/dead staining. (C) Quantitative result of live/dead cell-staining assay.
该工作进一步在SA过度表达的HepG-2细胞和正常小鼠成纤维细胞L929细胞的细胞混合物中进行选择捕获。在捕获/释放过程的一个周期之后,细胞混合物中HepG-2细胞数量的显着增加(Fig. 6A)。HepG-2细胞的纯度从32.5%提高到89.6%,最终可以回收超过40%的初始HepG-2细胞(Fig. 6B)。此外,以小鼠全血作为替代物,模拟癌症患者含有循环肿瘤细胞(Circulating tumor cells, CTCs)的血液。实验表明,该智能捕获平台表面可从人工CTCs血液样本中捕获超过15%的掺入的HepG-2细胞,表现出可观的选择性癌细胞捕获效率(Fig. 6 C-D)。值得一提的是,通过降低温度,所有结合的肿瘤细胞都可从SIH表面释放出来,展现出简便高效的细胞回收过程。
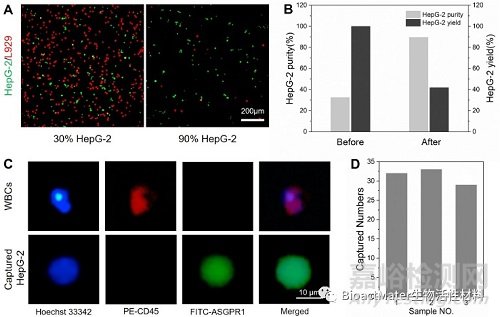
Fig. 6 (A) and (B) Selective cancer cell capture. (A) The fluorescent images of cell mixture of HepG-2 cells (green, DiO) and L929 cells (red, Dil) before (left) and after (right) on capture/release cycle. (C) Enumeration of the captured HepG-2 cells from artificial CTC blood sample spiked with 200 HepG-2 cells per mL. (D) The numbers of captured HepG-2 cells in three parallel trials.
总的来说,该工作基于人工合成受体的分子识别作用,设计出可逆识别肿瘤标记物SA的智能表面。该智能平台具有温度响应性的肿瘤细胞识别能力,可通过改变温度来选择性捕获和释放SA过表达的肿瘤细胞(例如HepG-2)。可以预期,这种基于MIT的可以分子识别平台可成为一类检测和收集CTCs乃至其他特异性细胞的的有用且通用的工具,具有很好的生物医学应用前景。
原文信息
Yue Ma, Yimei Yin, Li Ni, Haohan Miao, Yingjia Wang, Cheng Pan, Xiaohua Tian, Jianming Pan, Tianyan You, Bin Li**, Guoqing Pan*.
Thermo-responsive imprinted hydrogel with switchable sialic acid recognition for selective cancer cell isolation from blood.
Bioactive Materials 6 (2021) 1308–1317.

来源:BioactMater生物活性材料


