您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-03-26 09:11
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
Insmed阿米卡星脂质体吸入悬液日本获批上市。Insmed公司阿米卡星脂质体吸入悬液Arikayce获日本厚生劳动省(MHLW)批准上市,用于治疗对先前的多药方案(MDR)应答不足的、由鸟型分枝杆菌复合体(MAC)导致的非结核分枝杆菌(NTM)肺部感染。在一项III期临床CONVERT中,与GBT治疗相比,Arikayce联合GBT显著提高痰培养转化率(p<0.0001),两组患者消除痰中MAC引起的NTM肺病证据的比例分别为29%和9%。在美国,Arikayce已于2018年9月获批上市,是FDA批准用于这种难治性疾病的首个疗法。
国内药讯
1.百奥泰「阿达木单抗」获批用于幼年特发性关节炎。百奥泰阿达木单抗(格乐立®)新增适应症及新规格获NMPA批准,用于治疗多关节型幼年特发性关节炎(40mg/0.8ml、20mg/0.4ml)。阿达木单抗原研为艾伯维的修美乐(抗TNF-α单抗),全球范围内,修美乐已获批用于治疗类风湿关节炎、强直性脊柱炎等十多种疾病。目前,格乐立®获批适应症为强直性脊柱炎、类风湿关节炎、 银屑病、克罗恩病、葡萄膜炎、儿童斑块状银屑病和多关节型幼年特发性关节炎。
2.豪森「艾米替诺福韦」完成第一轮补充资料提交。豪森药业1类新药「艾米替诺福韦片」第一轮补充资料日前完成提交,预测该药有望在上半年获批。艾米替诺福韦片是一款新型核苷酸类逆转录酶抑制剂。一项在2021APASL会议上公布的用于治疗慢性乙型肝炎(CHB)的Ⅲ期临床结果显示,在HBeAg阴性和HBeAg 阳性两个患者队列中,艾米替诺福韦片治疗组48周后HBV DNA<20 IU/mL的患者比例分别为90.2%和52.8%(PPS 分析集),均非劣效于富马酸替诺福韦酯对照组。
3.三叶草生物新冠疫苗国际Ⅱ/Ⅲ期临床启动。三叶草生物 “S-三聚体”重组蛋白亚单位新冠疫苗在国际II/III期临床“SPECTRA” 中完成首批志愿者接种。该项临床旨在评估这款候选疫苗在与Dynavax公司的CpG 1018加铝佐剂联用的有效性、安全性和免疫原性。该试验将在拉丁美洲、亚洲、欧洲和非洲的多个临床研究中心入组22,000多名成年和老年志愿者,间隔21天完成两次接种。临床试验的中期结果预计2021年年中发布。
4.健康元重组新冠病毒融合蛋白疫苗获批临床。健康元控股子公司丽珠单抗研发的重组新型冠状病毒融合蛋白疫苗(V-01)临床试验申请获国家药监局批准,适应症为预防新冠病毒感染所致疾病(COVID-19)。V-01是丽珠单抗与中科院生物物理研究所合作研发的创新型新冠重组蛋白疫苗,具有自主知识产权。该疫苗可在2-8℃冷链运输及长期储存。
5.BI精神分裂症新药国内获批临床。勃林格殷格翰(BI)1类新药BI 425809片获国家药监局临床试验默认许可,拟用于治疗精神分裂症认知症状。BI 425809是一款Gly-T1抑制剂,旨在通过抑制Gly-T1改善N -甲基- D -天冬氨酸受体的功能减退,从而起到治疗作用。在一项II期临床(NCT02832037)研究中,与安慰剂相比,BI 425809 10mg和25mg剂量组的MCCB总体复合T评分(精神分裂症认知功能成套测验)较基线变化最大(调整后的平均差异:10mg:1.98,25mg:1.73)。
6.康方单抗AK117去年澳洲首例患者给药今年国内又报新临床许可。3月25日,康方生物1类新药AK117注射液的临床试验申请获CDE受理。这是该新药第三次在国内申报临床。AK117是该公司自主研发的一款新型抗CD47单抗,目前正在全球同步临床开发。在澳洲,该新药去年5月已完成Ⅰ期临床的首例患者入组和给药;在国内,该新药去年年底登记启动了一项用于晚期实体瘤或淋巴瘤患者中的I期临床;在美国,AK117已于去年4月获得FDA临床批件。
7.宜明昂科完成C轮融资。宜明昂科宣布完成8900万美元C轮融资。此次融资由大湾区共同家园发展基金(大湾区基金)和礼来亚洲基金共同领投,上海科创基金跟投,Pre-A轮投资方张科领弋及B轮投资方LYFE Capital(济峰)继续追加投资。本轮融资主要用于支持该公司正在中国进行的3个新药项目(CD47抑制剂IMM01、CD47/CD20双抗IMM0306、VEGF/PD-L1双抗IMM2510)的临床试验、在美国启动的IMM0306项目Ⅰ期临床以及另外5个新药项目的临床前研究。
国际药讯
1.首款治疗眼睛过敏的隐形眼镜在日本获批。日本厚生劳动省(MHLW )批准强生旗下Johnson & Johnson Vision公司开发的隐形眼镜Acuvue Theravision上市,这种隐形眼镜制作材料中包含抗组胺药物酮替芬(ketotifen),能够在眼镜佩戴时释放药物,治疗与眼睛过敏相关的眼痒。两项Ⅲ期临床结果显示,佩戴这种隐形眼镜的患者在戴上隐形眼镜15分钟后就能够观察到显著降低眼痒的效果,而且这一效果可持续12个小时。
2.阿斯利康CLL药物Calquence获英国NICE批准。英国国家卫生与临床优化研究所(NICE)批准阿斯利康(AstraZeneca)BTK抑制剂Calquence(Acalabrutinib)纳入英国国家医疗服务体系,用于治疗慢性淋巴细胞白血病(CLL)。该药物去年12月已获批单独用药治疗存在17p缺失或TP53突变的CLL患者,或者fludarabine联合cyclophosphamide和rituximab (FCR),以及bendamustine联合rituximab (BR)治疗不适用的CLL患者。NICE药物咨询委员会认为,与目前的CLL治疗方式相比,Calquence具有良好的耐受性,且副作用较小。
3.辉瑞口服抗新冠病毒疗法进入临床。辉瑞拟用于治疗新冠病毒感染的“first-in-class”口服抗病毒疗法PF-07321332已进入Ⅰ期临床的剂量递增阶段。PF-07321332是一种新冠病毒3CL蛋白酶抑制剂,已在体外实验中显示出强力的抗新冠病毒活性。而且,它对新冠病毒以外的其它冠状病毒也表现出活性。辉瑞还同时开发了一款用于治疗住院患者的静脉输注抗病毒疗法。这两款候选疗法有望为COVID-19患者提供覆盖疾病全程的治疗选择。
4.新格诺康与默沙东开展联合用药Ⅱ期临床。新格诺康(SignalChem)AXL抑制剂SLC-391拟联合默沙东KEYTRUDA® (pembrolizumab)开展一项Ⅱ期临床SKYLITE研究,评估联合用药用于治疗晚期非小细胞肺癌(NSCLC)的安全性和有效性,包括研究分析与抗肿瘤活性有关的AXL信号传导相关生物标记物。SLC-391是一种具有高效、高选择性的小分子药物,能阻止细胞分裂,抑制肿瘤生长,导致癌细胞死亡。目前SLC-391正在加拿大进行Ⅰ期临床。
5.Odonate终止长效口服紫杉醇III期临床研究。Odonate公司宣布终止其新型紫杉烷类抗癌药替司他赛(tesetaxel )的开发并结束公司的运营。根据FDA在pre-NDA会议上的反馈,替司他赛的临床数据不太可能支持该产品获得FDA的批准。在一项用于治疗HR+/Her2-转移性乳腺癌的III期(CONTESSA)研究中,与卡培他滨相比,替司他赛联合卡培他滨显著延长了患者的无进展生存期(9.8个月vs6.9个月)将疾病进展或死亡风险降低了28.4%。然而,联合治疗组不良事件导致停药的患者比例也显著高于单药治疗组(23.1%vs11.9%)。
医药热点
1.上海:中医药纳入公卫应急管理体系。上海市人大常委会24日表决通过《上海市中医药条例》,这是一部对有关中医药发展方方面面作出系统规定的地方立法,将中医药纳入上海公共卫生应急管理体系,推进中医药融入家庭医生制度建设,实现中医药在家庭医生团队服务中的全覆盖,保障市民享有优质中医药服务。条例将于今年5月1日起施行。
2.医疗机构要满足慢病患者用药需求。国务院应对新冠病毒肺炎疫情联防联控机制医疗救治组印发《关于做好当前慢性病长期用药处方管理工作的通知》。《通知》强调,医疗机构要采取切实有效措施,满足需长期用药、血液透析等特殊治疗的慢性病患者的医疗服务需求,对病情稳定的慢性病患者,一次可开具12周以内相关药品。
3.中国首例卵巢组织冻存移植成功自然妊娠。3月24日,北京妇产医院宣布,该院内分泌科阮祥燕教授团队成功完成“中国首例”卵巢组织冻存移植后患者成功自然妊娠,孕周已经15周。这是继2016年该团队成功完成中国第一例卵巢冻存组织移植术后的又一进步。卵巢组织冻存移植技术,也就是在癌症患者进行放化疗前,通过腹腔镜微创手术先取出部分卵巢组织在体外冻存,待患者原发疾病临床缓解后,再将组织移植回体内的一种新兴的生育力保护技术。
4.印度出现双重突变毒株。印度卫生部24日发表声明称,近两周以来,印度疫情呈现出明显的反弹迹象,变异新冠病毒已蔓延至印度18个邦。同时,在该国的马哈拉施特拉邦发现一种新型变异新冠病毒,该毒株出现双重突变,可能会弱化免疫效果且传染性更强。过去3个月,印度在10787个阳性样本中发现771个样本感染了新冠变异病毒,但由于样本有限,目前无法确定变异病毒与近期印度疫情反弹是否有关。
审评动向
1. CDE新药受理情况(03月24日)
申请临床:
深圳海王的二甲苯磺酸萘普替尼片、住友制药的SEP-363856片(4个规格)、百奥泰的贝伐珠单抗注射液(2个规格)、康方生物的AK117注射液、罗氏的Tiragolumab注射液。
申请生产:
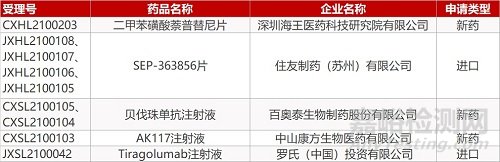
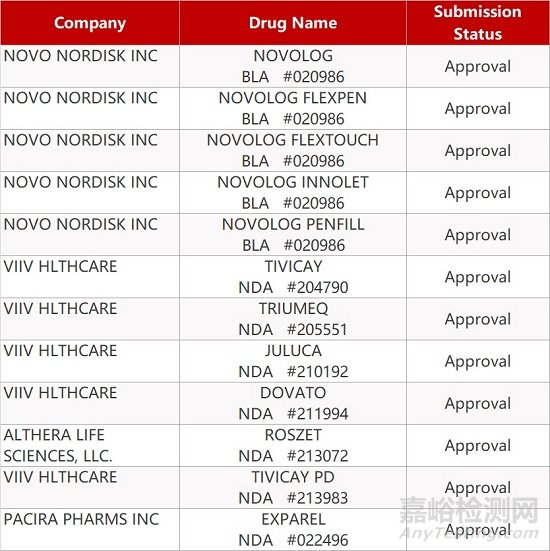
2. FDA新药获批情况(北美03月23日)
股市资讯
【科伦药业】有偿许可EllipsesPharma在除大中华区及部分亚太地区外开发,销售RET激酶抑制剂。
【恒瑞医药】多西他赛注射液(治疗局部晚期或转移性乳腺癌等)通过仿制药一致性评价。
【九强生物】(1)预计2020年营收8.48亿元,同比增长0.86%;归母净利润1.12亿元,同比减少66.20%;(2)预计2021年Q1归母净利润1.08-1.34亿元,同比增长750%-950%。

来源:药研发


