您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-07-01 22:28
摘要
凝胶制剂作为透皮给药系统(transdermal drug delivery system,TDDS)的一种新型制剂,经皮肤给药发挥全身或局部治疗作用,有使用方便、安全性好、释药平缓持久等优势,成为近年来药物制剂研发的重点之一。但现有的大多数化合物均为难溶性药物,在凝胶制剂方面的应用受限。近年来,许多新型药物载体包括纳米化技术、包合物、固体分散体等被广泛用于难溶药物增溶以及增强药物皮肤透过能力。文章详细综述了各种药物载体的特点及其在凝胶制剂的应用优势和缺陷,并汇总了现 FDA 难溶性药物凝胶产品的上市情况以及各种增溶技术在凝胶制剂的具体应用,为凝胶制剂未来的研发方向提供理论基础及实践案例。
关键词
凝胶制剂;难溶性药物;新型药物载体;增溶
正文
市面上大部分药物均为口服制剂,其存在消化道不良反应以及肝首过效应等缺陷,影响药物的生物利用度,并且在老年、儿童等存在吞咽困难的患者人群中顺应性较差。经皮给药已成为重要的给药途径,因具安全、长效、使用方便和非侵入性等特点成为近年来药物制剂研发的热点[1]。随着药物经皮促透技术的进步,传统外用凝胶制剂,不仅可起到局部作用,还可研制成起全身作用的制剂,例如美国 FDA 批准雅培旗下 AbbVie公司生产的睾酮凝胶,2013 年获得 10 亿美元的销售额。
目前以水性基质制成的外用水凝胶研究最为广泛,其具有易于涂布、洗除且不污染衣物的优点,但目前研究面临的关键性技术问题是多数药物为脂溶性,在水性基质中溶解性差,因此需要解决脂溶性药物在水凝胶中的溶解性问题,同时辅以促透技术使药物得以透过皮肤角质层屏障。传统已上市的凝胶剂较多采用无水乙醇、二甲基亚砜等溶剂对药物助溶,其存在一定毒性以及皮肤刺激性等缺点,特别是对婴幼儿及对乙醇等溶剂过敏者不适用,现代药剂学更偏向于用载体增溶技术解决药物难溶性问题。目前,研究者在难溶性药物的增溶技术方面做了许多研究工作,本研究对难溶性药物的增溶技术进行汇总,并探讨其在凝胶制剂中的应用,为凝胶剂的研发提供参考。
1、凝胶制剂概述
凝胶剂是一种适用于皮肤、黏膜及腔道给药的新型剂型。中国药典 2015 年版四部通则规定,凝胶剂系指药物与能形成凝胶的辅料制成溶液、混悬或乳状液型的稠厚液体或半固体制剂[2]。其制备工艺简易,所用辅料无毒且可生物降解,适用于皮肤类、眼科类、肛门肠道感染等各类疾病,并可直接作用于病变部位,使药物浓集,提高患处药物疗效且减轻全身不良反应,具有明显临床优势。此外,其通过控制药物存在形式或调整凝胶基质的组成可实现缓释、控释给药[3-4]。
凝胶剂的基质属于单相分散系统,可分为水性基质与油性基质。水性凝胶基质一般由高分子材料与水构成,为保证制剂的润湿性通常需要另加多元醇作为保湿剂;油性凝胶基质由液状石蜡或脂肪油与胶体硅或铝皂、锌皂构成。由于水性基质亲水能力强,与人体内环境亲和度高,可有效提高药物释放效率,并可防止组织渗出液淤积,故在临床应用上具有顺应性好的优势。
目前中国上市的凝胶剂仍然较少,主要有林可霉素利多卡因、吡罗昔康、酮洛芬、双氯芬酸钠、他扎罗汀、糠酸莫米松(mometasone furoate,MF)、异维 A 酸等。起局部和全身作用的凝胶剂的研发需要解决脂溶性药物在水凝胶中的溶解性与经皮渗透问题,并且药物促透剂也以脂溶性居多,因此溶解性问题是凝胶制备中的关键点。现已发表的文献中,以采用微乳、脂质体、包合物等药物载体用于增强其在水凝胶中的溶解和分散为主[5-6]。
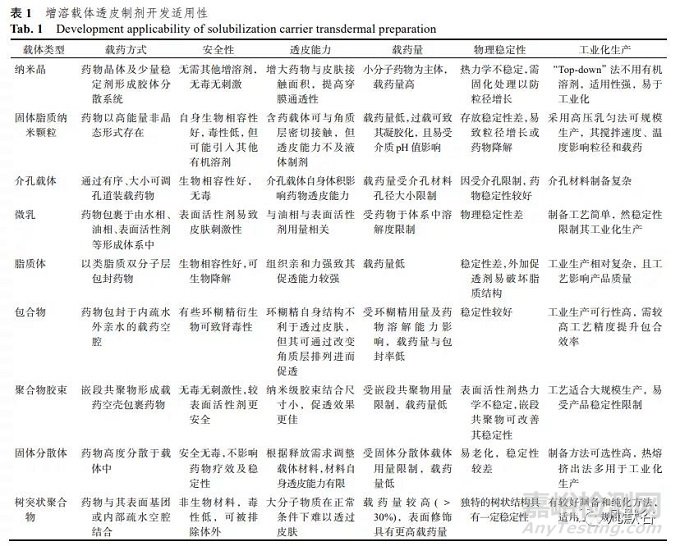
2、增溶技术在凝胶中的适用性
常用的基于药物与高分子聚合物等形成胶束、固体分散体、包合物等药物载体方式的增溶技术见表 1。综合增溶载体和凝胶制剂两者的特性,分别就载药方式、透皮能力、安全性、载药量、制剂物理稳定性以及工业化生产的难易度等方向,探讨难溶药物凝胶剂开发的可行性。
给药量、给药时间及给药部位等用药参数是评价难溶性药物是否适宜开发为凝胶等外用制剂的重要指标。微乳作为一种新型递药载体,具有粒径小、渗透性强、溶解度大、易于制备等优势,已有较多应用于凝胶制剂的文献报道,如非甾体抗炎药塞来昔布微乳凝胶[7]、降糖药瑞格列奈微乳凝胶[8]、抗病毒药喷昔洛韦微乳凝胶[9]等;脂质体以其低毒性、强组织亲和力和可实现缓控释给药等特点,被广泛应用于透皮制剂,如双氯芬酸脂质体凝胶[10]、灰黄霉素脂质体凝胶[11]、透明质酸钠脂质体凝胶[12]。但微乳与脂质体载药量较低,在经皮递药系统主要适用于对皮肤渗透能力要求高,但给药剂量较小的药物。
包合物因能够显著提高药物水溶性,在凝胶制剂中应用广泛,例如,已被 FDA 批准上市的以甲基环糊精增溶的他扎罗汀凝胶。其主要应用于难溶性药物水凝胶的开发。聚合物胶束无毒、安全性好,主要应用于滴眼液,在外用制剂中报道较少,但在眼部凝胶领域具有很好的前景。亲水性固体分散体可提高药物溶解度及溶出度,但以改善溶出为主,且其存在载药能力不足以及稳定性不佳等问题,适用于给药剂量较小且易受复杂工艺影响的药物,临床上多用于腔道或黏膜给药的温敏型原位凝胶的研究。
纳米晶安全性好,载药量可高达 100%,粒径极小,具有巨大的比表面积,能减少促渗剂以及表面活性剂的使用,采用联用技术,易于工业化,其在经皮给药领域具有很大前景,但现阶段保持药物粒径不增长是一个较大的挑战。固体脂质纳米粒(Solid lipid nanoparticles,SLN)与纳米晶相比,粒径较大,透皮能力较弱,且载药量远低于纳米晶,因而在透皮给药系统中处于劣势。介孔载体与树状聚合物安全无毒,易于操作,具有一定稳定性。但其载药量受到限制,且大分子物质难以透过皮肤,故较少用于透皮制剂,如需开发成经皮给药制剂则主要用于稳定性较差,但需长期缓释给药的药物。
3、增溶技术在凝胶剂中的应用
难溶药物作为药物市场中重要组成部分,在口服制剂、注射制剂以及经皮给药制剂等方向上都有许多上市产品,FDA 上市药物中的难溶药物凝胶产品见表 2。

由表 2 可见,目前已上市的难溶性药物凝胶产品,大部分是借助乙醇、丙二醇、二甲基亚砜等有机溶剂助溶,少量通过调节 pH(如加入碱性溶液)、添加表面活性剂或环糊精等方式增溶,也有个别通过添加液状石蜡或脂肪油等做成油凝胶。水凝胶剂具有利于药物释放,不影响皮肤透气,易于涂展、洗除,无油腻感,稠度小,能吸收组织渗出液等特点,临床适用性高。采用脂质体、胶束、固体分散体、微乳等作为药物载体的方式,解决药物难溶性问题已成为主要的发展方向,例如已上市的他扎罗汀凝胶利用环糊精水溶液溶解药物,使其水溶性显著提高。近 5 年上市难溶药物凝胶产品的研究进展见表 3,纳米药物载体(如纳米乳、纳米脂质体)具有提高药物溶解度、促进药物经皮吸收、控制药物释放以及可靶向给药等优点,被广泛应用于难溶性药物凝胶制剂的研发。另外,也有不少学者研究固体分散体和环糊精包合物等增溶方法。
3.1 固体分散体凝胶
布洛芬(ibuprofen,IBU)是一种非甾体解热镇痛抗炎药,其水溶性差,口服给药可能引发消化道出血、消化性溃疡等严重不良反应,在老人、婴儿、昏迷或者呕吐患者等特殊群体中顺应性较差。有研究将其制备成固体分散体提高 IBU 的水溶性,之后制备成温敏型原位凝胶用于直肠给药,体外释放数据显示,常规固体栓剂仅为 25%左右,而原位凝胶可达 80%左右。体内药动学研究表明,原位凝胶的 AUC(0-∞)为(88.70±13.90)μg·min·mL–1,远高于常规固体栓剂的(27.21±4.90)μg·min·mL–1,且与固体栓剂相比,原位凝胶的 Cmax 提高了 76.8%左右。两者均表明以固体分散体为载体制备的 IBU原位凝胶可提高药物吸收,优于传统固体栓剂[26]。

姜黄素是一种多酚类化合物,具有抗炎、抗氧化、抗肿瘤、抗凝血、增强免疫功能等多种药理作用。由于其水溶性差、生物利用度低、稳定性差和体内代谢快等缺点,致使临床应用受到限制,但其在治疗阴道感染等局部炎症方面具有开发前景。有研究利用固体分散体作为载体提高了姜黄素的水溶性,并且探讨了姜黄素固体分散体原位水凝胶对大鼠阴道感染模型的治疗作用,证明其开发为一种用于治疗阴道细菌感染和改善阴道伤口愈合的局部制剂的可行性[27]。固体分散体是指药物以分子、无定型、微晶态等高度分散状态,均匀分布在载体中形成的一种分散系统。其能有效增加药物溶解度,加强难溶性药物的释放,在口服制剂中应用较多,但该载体系统热力学稳定性差,在凝胶药物贮存过程中要注意药物析出等问题。温敏型原位凝胶在体温下呈凝胶状,具有三维网络结构和良好组织相容性,可有效改善固体分散体热力学不稳定的缺陷。温敏型原位凝胶适用于腔道给药或黏膜给药,能够显著减轻栓剂的不适感,具有较好的市场前景。
3.2 环糊精凝胶
雄激素性脱发症(androgenetic alopecia,AGA)是影响男性和女性头部美观的最常见疾病。米诺地尔(minoxidil,MXD)是一种嘧啶衍生物药物,被广泛应用于 AGA 的局部治疗。由于其有限的水溶性,MXD 局部制剂必须含有高百分比的助溶剂如乙醇和丙二醇,因此对皮肤的刺激与毒性较大。为提高 MXD 的水溶性,Lopedota 等[28]通过制备MXD环糊精水凝胶,解决了药物水溶性差的问题,同时发现包合物还能增强水凝胶制剂的物理化学稳定性,促进其吸收。醋酸地塞米松已被证明具有治疗角膜炎症的功效,且没有增加眼压的不良反应。然而其水溶性差,导致眼部局部给药后,药物的生物利用度和渗透率低。因此有研究者尝试利用环糊精来改善其水溶性[29],并将其制备成凝胶,以延缓其在眼部的滞留时间。
环糊精单体为中空的环筒状结构,药物与筒内部和侧链烷基醚结合,包合性好,能显著提高药物水溶性。其水解产物为葡萄糖,毒性小,生物相容性高,因而被广泛用做包合材料。水凝胶基质的亲水特性是难溶性药物制成水凝胶的难点,导致了制剂载药量不足。而环糊精能够增加药物的溶解度以及溶出速率,提高了药物的生物利用度。此外,包合物通常可减缓药物降解速率,显著提高稳定性。有研究提出,将海藻酸钠凝胶基质与环糊精包合物的优势结合起来,可分别调控多活性成分凝胶中水溶性与难溶性物质的释放特性[30]。
3.3 纳米药物载体凝胶
3.3.1 SLN 凝胶
氟康唑是第 3 代三唑类抗真菌药,微溶于水,现已上市的主要是口服和肠外剂型,常伴有不良反应,如胃肠道反应、皮疹、红细胞减少,甚至肝毒性等,而局部用药可减少全身不良反应。El-Housiny 等[31]利用 SLN 负载氟康唑,将其制备成凝胶剂,发现其对于花斑癣的治疗效果优于已上市的乳膏。
MF 是一种糖皮质激素,具有抗感染、抗瘙痒、抗高增殖活性,主要用于治疗各种慢性炎症和银屑病。现已上市的 MF 乳膏和 MF 洗剂(0.1%)等产品,常伴有轻微皮肤刺激性、烧灼感等不良反应。SLN 具有亲脂特性,因此被认为特别适于作为局部给药的脂溶性药物如 MF 的载体。Madan 等[32]采用溶剂注射法制备了 MF-SLN,再将其制备成凝胶。其结果表明,SLN 加载凝胶的皮肤渗透性比市售乳膏高 15.21 倍,并且显示出 83.52%的皮肤沉积,其比市售的乳膏高出 2.67 倍,比普通载药凝胶多 20 倍,具有良好的局部作用特性。
SLN 是通过将油/水乳状液中的液体脂质替换成固体脂质或混合固体脂质,其平均粒径约 40~1 000 nm。SLN 尺寸小,比表面积大,可增加难溶药物的溶解度。其水合作用有助于药物渗透进皮肤组织,但同时由于该载体为固体脂质,于皮肤内释药时间高于液体制剂,有很高的皮肤沉积效应。因此该载体与局部外用制剂适配度高,药物可有效积聚于患处起到长效治疗的作用。
3.3.2 聚合物胶束凝胶
盐酸氮卓斯丁(azelastinehydrochloride,AZT HCl)是一种疏水性药物,具有选择性组胺 H1 拮抗作用以及抑制其他参与过敏反应的介质释放作用,主要应用于很多已上市的滴眼液中。Devi 等[33]采用薄膜水化法制备了有较高载药量的 AZT HCl 聚合物胶束,再将其加入到凝胶基质中,所开发的凝胶剂显示了长效(高达8 h),且无刺激性和角膜毒性的特性,比市售制剂的渗透性更好。此外,该制剂通过局部富集,可延长药物于结膜患处的滞留时间,具有一定靶向性。
聚合物胶束通过两亲性的嵌段共聚物可将药物装载于内部从而提高药物溶解度,其稳定性与表面活性剂胶束相比,有明显改善,但依然存在局部富集、粒径增长的风险。而凝胶作为半固体制剂,可较大程度避免以上问题。在难溶性药物的凝胶剂开发过程中,纳米级尺寸胶束可提高药物的皮肤透过能力,具有较高的应用价值。
3.3.3 树状大分子凝胶
地蒽酚是治疗银屑病的重要药物之一,为避免药物的毒性,需使药物在患病局部起到精确治疗的作用。微海绵技术是一种独特的局部药物控释技术,它通过将药物包裹在树状聚合物中,在增加药物溶解能力的同时,对皮脂腺表现出化学亲和力,从而在皮肤上停留较长时间。Tripathi 等[34]将该药物包裹在 PAMAMG4树状大分子中,控制药物氧化速度以及增加其通透性,并采用准乳液溶剂扩散法成功地研制出地蒽酚聚合物微海绵凝胶配方。这种配方可以增强药物的溶解度,防止其自动氧化,有较好的生物利用度,且对于皮肤无刺激性。
树突状聚合物为球形结构,具有多个内腔,可与药物形成稳定的主客体配合物。树状大分子包裹药物可以有效地将其缓慢运送,且避免其组分降解,起到长效缓释的作用。其与凝胶剂结合可准确定位至患处,且可对皮肤产生水化作用,帮助药物树状大分子复合物透过皮肤,从而起到治疗效果。
3.3.4 其他
除上述常用纳米药物载体外,尚有研究报道利用纳米晶负载孟鲁司特[35],增加药物溶解度的同时,改善了药物的透皮传递,并提高了其化学稳定性。脂质体作为丹皮酚的载体[36],降低其挥发性的同时,具有一定控释作用。相较于固体分散体不稳定,环糊精对于药物分子大小有所要求,纳米药物载体所用材料生物相容性好,毒性低,能够改变药物在体内的分布,且具有一定促透作用的优势,近年来,其在制剂研发中占有很大比例。
4、总结与展望
难溶性药物增溶技术的发展,为经皮给药制剂的开发带来了新的思路。纳米药物载体生物相容性好,且安全性高;固体分散体对于腔道、黏膜给药的温敏性原位凝胶的研发特别适用;环糊精多用于解决水难溶性药物制备成水凝胶的难题。增溶技术的发展和应用将在未来很大程度上促进凝胶剂的研发,而凝胶剂的经皮促透技术是另一个需要研究的关键技术。化学透皮促进剂也多为脂溶性,加入凝胶中的溶解性问题可同样采用上述的增溶技术解决。
此外,有不少学者开始尝试将增溶技术与常用的物理促透方法结合以解决药物促透问题。例如将微针与胶束和包合物结合[37-38],将离子导入与环糊精和纳米乳剂结合[39-40]。对于离子导入来说,利用增溶技术使药物能够溶解在适合应用电流的水配方中,是其进行促透的先决条件。且水凝胶与微针的发展也密不可分,这同样离不开增溶技术的运用。相较于其他增溶技术,纳米药物载体本身就具有一定促透性,与传统物理促透方法联用,有协同效果,因而前景更广。
作者 | 江蕾蕾,江昌照,王秀敏,马瑞,叶金翠
杭州医学院,浙江省神经精神疾病药物研究重点实验室

来源:中国现代应用药学 2021年


