您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-09-09 11:07
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
安帝康抗流感1类新药获批临床。安帝康生物自主研发的Cap依赖型核酸内切酶抑制剂ADC189获国家药监局临床试验默示许可,拟开发用于治疗和预防甲型、乙型流感。ADC189具有全新的抗流感作用机制,可直接抑制病毒的复制。一项头对头研究的数据显示,与同靶点对照药物相比,ADC189具有无中枢神经系统副作用、口服吸收不受食物影响、更高安全剂量等安全性优势,显示出“best-in-class”的特征。
国内药讯
1.康希诺新冠疫苗加强针效果积极。康希诺腺病毒新冠疫苗克威莎用于两针灭活疫苗后加强产生的中和抗体增长水平显著优于同源加强的效果。两针灭活疫苗后再接种一针克威莎作为加强,接种者14天后中和抗体GMTs为197.4 (167.7, 232.4),抗体水平升高约78倍;若第三针用灭活疫苗进行加强,抗体水平为33.6 (28.3, 39.8),升高约15.2倍。此外,临床中未发现疫苗相关的严重不良反应。相关研究成果发表在medRvix上。
2.信达PI3Kδ抑制剂启动国际Ⅲ期临床。信达生物PI3Kδ抑制剂parsaclisib片登记启动一项治疗骨髓纤维化患者的Ⅲ期临床。这是一项国际临床,将在对芦可替尼反应不佳的骨髓纤维化患者中评价Parsaclisib联合芦可替尼治疗的效果,主要研究者为浙江大学医学院附属第一医院主任医师金洁博士。此前,parsaclisib片用于复发性或难治性滤泡性淋巴瘤的适应症,已被CDE纳入突破性治疗品种。
3.甘莱THRβ激动剂美国I期临床积极。歌礼旗下甘莱制药肝脏靶向性前体药物ASC41片健康受试者药物相互作用和非酒精性脂肪性肝病患者药代动力学(PK)美国I期临床取得良好顶线数据。使用或不使用伊曲康唑或苯妥英,活性代谢物ASC41-A的暴露量无显著差异。ASC41/ASC41-A与患者常用的抗抑郁药物之间产生药物相互作用的可能性小。美国药代动力学结果与ASC41中国I期研究的结果相当。
4.苑东NGF单抗获批镇痛临床。苑东生物旗下优洛生物1类生物药EP-9001A注射液获国家药监局临床试验默示许可,拟用于治疗骨转移癌痛。EP-9001A是一款NGF单抗,通过选择性靶向结合并抑制NGF,阻止来自肌肉、皮肤和器官的疼痛信号进入脊髓和大脑。临床前研究显示,EP-9001A对多种疼痛模型均有显著镇痛效果,起效剂量低,镇痛效果良好且持久。
5.和黄HMPL-453获批临床。和黄医药FGFR 1/2/3抑制剂HMPL-453获国家药监局临床试验默示许可,拟联合化疗或抗PD-1单抗用于晚期实体肿瘤的治疗。根据该公司的最新业务进展,HMPL-453有望在今年年底启动这项联合用药的临床研究。目前,该产品已在国内开展的两项Ⅱ期临床中,评估用于治疗晚期恶性间皮瘤,以及晚期肝内胆管癌的安全性和有效性。
国际药讯
1.全球首个新冠DNA疫苗获批上市。印度药监部门日前批准印度药企Zydus Cadila新冠DNA疫苗ZyCoV-D上市,用于预防12岁及以上人群的新冠感染。ZyCoV-D是全球首款获批的新冠DNA疫苗。它无需注射,通过按压在皮肤上的无针装置,利用细小的高压液体流刺穿皮肤,与注射相比痛苦更轻。在Delta毒株肆行期间, 28,000志愿者参与的大规模临床试验中,该疫苗的有效率为67%。
2.Oxbryta两项儿科新应用获FDA优先审查。FDA受理Global Blood Therapeutics公司镰刀型细胞贫血病疗法Oxbryta(voxelotor)的一份补充新药申请(sNDA)和一份新药申请(NDA)。其中,sNDA寻求加速批准Oxbryta用于治疗4-11岁镰状细胞病(SCD)儿童患者;NDA寻求批准Oxbryta一种新的、适用于儿科患者的适龄分散片剂型。FDA已授予NDA和sNDA优先审查,PDUFA日期为2021年12月25日。
3.皮下注射RNAi疗法Ⅲ期临床积极。Alnylam公司RNAi药物vutrisiran治疗ATTR淀粉样变性的Ⅲ期临床HELIOS-A最新结果积极。该试验今年4月已达到主要终点和所有次要终点,vutrisiran治疗组9个月时患者mNIS+7评分(评估神经病损伤的一种方式)与基线相比平均下降2.24点,而历史安慰剂组平均上升14.76点。新数据进一步支持其主要和次要终点结果。Vutrisiran目前正接受FDA的审评,PDUFA日期为明年4月份。
4.右旋普拉克索Ⅱ期临床积极。Knopp公司公布右旋普拉克索(dexpramipexole)治疗中重度嗜酸性粒细胞性哮喘的Ⅱ期临床EXHALE的生物标志物数据。该试验此前已达到主要终点,显示出剂量依赖性的嗜酸性粒细胞减少。新的数据显示,该药使嗜酸性粒细胞的降低,与患者支气管扩张剂前FEV1的改善显著相关(联合300 mg/天和150 mg/天右旋普拉克索,p<0.0001)。并且,右旋普拉克索对鼻嗜酸性粒细胞过氧化物酶(EPX)水平也具有剂量依赖性作用。
5.Moderna联手ILCM公司开发mRNA疗法。Moderna公司与The Institute for Life Changing Medicines(ILCM)就Moderna拟用于治疗1型Crigler-Najjar综合征(CN-1)的候选药物mRNA-3351达成授权协议。mRNA-3351是一款新型mRNA疗法,已被FDA授予用于治疗CN-1的罕见儿科疾病资格。根据协议,Moderna将在ILCM无需预付费用或支付任何下游付款的情况下,授予其开发mRNA-3351的权益,而ILCM将负责mRNA-3351的临床开发,计划在2022年启动研发工作。
6.罗氏布局iPSC同种异体细胞疗法。罗氏旗下基因泰克与Adaptimmune公司达成研发和许可协议。Adaptimmune公司将利用诱导多能干细胞(iPSC)衍生同种异体细胞技术平台来生成T细胞,基因泰克公司将负责设计T细胞受体(TCR),两家公司将联合开发靶向5种癌症相关靶点的同种异体T细胞疗法,以及个体化同种异体T细胞疗法。根据协议,Adaptimmune将获得1.5亿美元的前期付款,以及可能超过30亿美元的研发、监管和推广里程碑付款。
医药热点
1.美国多州检出新冠Mu毒株。据福克斯新闻当地时间9月7日报道,已在美国的49个州检测到新冠变异病毒Mu毒株。根据变种病毒追踪网站GISAID数据,截至7日,美国已有2400人感染Mu病毒,数量位列全球第一。美国传染病学专家福奇表示,Mu变种病毒具有一系列突变,也许能够逃避某些抗体的保护。
2.北京出台全科医生转岗培训方案。北京市发布《北京市全科医生转岗培训实施方案(2021年版)》,要求原则上在2025年年底前,社区卫生服务中心(站)尚未注册(含加注)全科医学专业执业范围的医生应全部完成全科医生转岗培训。全科转岗培训由理论培训、临床轮转、系列病例讨论和基层实践4个部分组成,培训时间为1年,要求修满24学分。其中,必修的病例讨论内容不少于8学分。
3.甘肃今年培训180名县级骨干专科医师。甘肃省卫健委印发《2021年甘肃省县级医院骨干专科医师培训实施方案》。《方案》明确,2021年县级医院骨干专科医师培训任务共180名。其中,省内培训基地承担130名培训任务,委托上海交通大学附属瑞金医院承担50名培训任务,培训方向为呼吸与危重症医学、心血管病学、妇产科学、超声诊断学、普通外科学、重症医学6个专业。
评审动态
申请临床:
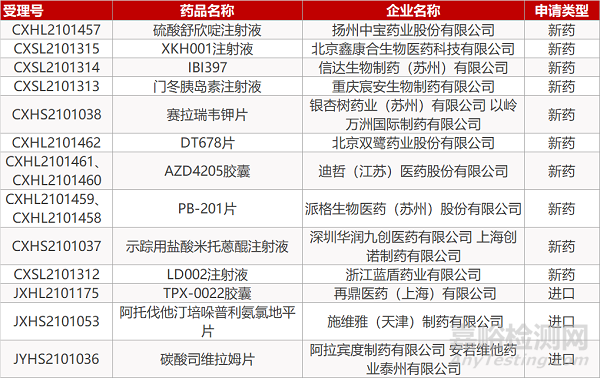
扬州中宝药业的硫酸舒欣啶注射液、北京鑫康合生物的XKH001注射液、信达生物的IBI397、重庆宸安生物的门冬胰岛素注射液、北京双鹭的DT678片、迪哲(江苏)的AZD4205胶囊(2个规格)、派格生物医药的PB-201片(2个规格)、浙江蓝盾的LD002注射液、再鼎医药的TPX-0022胶囊。
申请生产:
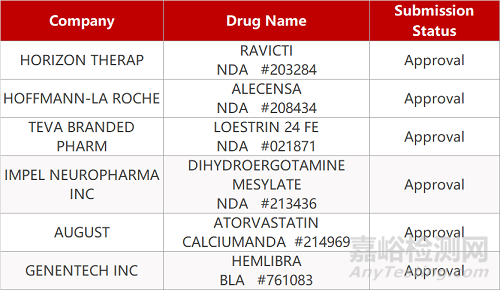
银杏树药业/以岭万洲的赛拉瑞韦钾片、深圳华润九创/上海创诺的示踪用盐酸米托蒽醌注射液、施维雅的阿托伐他汀培哚普利氨氯地平片、阿拉宾度制药/安若维他药业的碳酸司维拉姆片。

来源:药研发


