您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-11-05 22:53
3D打印又称增材制造(additive manufacture),是一种由数字化设计逐层生成三维实体的快速成型技术[1]。其应用于药物制剂领域则具体指通过计算机辅助来为制剂设计打印路径并创建指令,即可通过层层打印,完成数字3D模型向3D实体转化的一种新兴技术[2]。制药领域使用的3D打印按成型技术原理分类主要包括立体光固化成型(stereolithgraphy apparatus,SLA)、粉末 3D打 印(inkjet 3D printing)、热 熔 沉 积(fused-deposition modeling,FDM)和半固态挤出(semi-solid extraction,SSE)等[3-6]。
药物递送系统是指在剂量、时间和空间上调控药物在体内分布的技术体系[7]。因便于携带和储存,固体制剂的应用最为广泛,然而传统工业大批量生产的固定规格的固体制剂难以满足患者的个性化用药需求[7-8]。相对于传统制药技术,3D 打印药物制剂灵活的个性化定制能力和精准的剂量控制是其核心优势[9]。借助3D打印技术“按需”生产药物制剂可克服传统制造方式的“一刀切模式”,可满足患者在年龄、体质量、器官功能和疾病严重程度方面的个性化用药需求[10];加之 3D 打印设备正朝着桌面化、智能化的方向发展,有望“落地”基层药房,促进传统药房向数字药房的转型升级,应用前景广阔[11]。基于此,本文回顾了近年来 3D 打印技术在药物递送系统中的应用进展及其面临的挑战和机遇,以期为该技术在开发个性化药物递送系统中的应用提供参考。
1 3D打印在药物递送系统中的应用
1.1 速释制剂
口服固体速释制剂是一种在服用后能迅速崩解的固体制剂,具有药物吸收快、生物利用度高的优点,特别适合于需要快速起效的药物[12]。相较于传统压片工艺,粉末3D打印是一种非压缩式的生产技术,所制备的制剂具有疏松多孔的结构,有利于液体的渗透,进而促进药物崩解、加速有效成分的释放[13 - 14]。2015 年,美国FDA批准了第1个3D打印药品左乙拉西坦口崩速释片上市,该片剂是基于粉末3D打印技术制备的具有多微孔结构的口崩速释片,解决了癫痫患者吞咽高剂量(1 000 mg)传统片剂的难题[15]。我国研究者 Yu 等[16]也采用粉末3D打印技术制备了豆腐果苷速崩片和对乙酰氨基酚速崩片,实验结果表明所制备的这两种速崩片的崩解时间分别为 19.8、23.4 s,且在 2 min 之内均可完全释放,硬度、崩解时间、脆碎度均符合《中国药典》的相关规定。还有一些学者进一步研究了在保证制剂机械强度和释放速度的前提下,如何通过3D打印技术进一步提升制剂的载药量,以减少患者的单次服药数量。例如Khaled等[14]以对乙酰氨基酚为模型药,使用SSE法成功制备了载药量高达80%的速释片,该片剂可在60 s内崩解完全并在 5 min 内完成药物的释放,且符合《美国药典》(USP)的标准。Cui等[11]采用SSE法制备了载药量高达 96%的左乙拉西坦片,该片剂在 2 min 内即可释放97.45%。这项研究是SSE 3D打印技术在高载药量制剂制造领域的突破,进一步验证了3D打印在制备高载药量速释制剂领域中的应用潜力。除了常规速释制剂,具有靶向性质的快速释药装置也是学者们研究的重点。例如Krause等[17]使用FDM技术构建了一种压力控制的药物递送系统,该系统可通过对胃肠道系统不同部位的压力响应来实现药物的靶向释放。该研究采用脆性聚合物Eudragit® RS作为囊壳材料制备成胶囊;经体外生物相关压力实验证明,其可作为一种压力响应性的药物递送系统将药物递送至胃肠道靶向位置,并在特定压力下使囊壳破碎,实现药物的快速、精准释放。
1.2 缓控释制剂
药动学理论表明,药物的释放速率与固体制剂的几何形状有关,制剂几何形状的改变会影响药物的释放曲线[18]。3D打印具有灵活的形状定制能力,可通过对制剂的几何形状及内部结构的设计而实现对药物释放的控制和调节[19]。Goyanes等[20]使用FDM技术制备了不同形状(立方体、金字塔形、圆柱体、球体和环面)的片剂,实验结果表明在基质溶蚀为主导的药物释放过程中,几何形状对药物释放具有显著影响,且表面积与体积的比值越大,其药物释放越快。为了进一步探究形状对药物释放的影响,Sadia 等[21]制备了一种多孔道制剂(图 1),并研究了片剂孔道的宽度、长度以及孔道与药品的对齐方式对药物释放的影响。

结果表明,在相同对齐方式的制剂中,随着孔道宽度的增加,药物释放速率逐步加快;孔道较短(8.6 mm)但多的片剂比孔道较少但长(18.2 mm)的片剂能更快地释放药物,这可能与通道内流体流动阻力的变化有关。Kyobula 等[22]以蜂蜡为辅料,制备了具有蜂窝结构的非诺贝特片剂(图2),只需通过3D打印技术控制蜂窝结构中孔的大小和表面积便可影响药物的释放,实现可变和可预测的药物释放曲线。该研究结果显示,在药物释放过程中,当孔径大于0.41 mm时,药物的释放速率与表面积成正相关;当孔径小于 0.41 mm时,药物的释放速率随着表面积的增加而变缓,这是因为过小的孔径不利于液体的润湿,对流体的流动形成了阻碍作用,不利于药物的释放。

此外,3D 打印技术除可实现固体制剂复杂形状的定制外,还能同时改变其相关性能,进一步提升制剂对药物释放的控制和调节能力。如Li等[23]采用SSE法成功制备了一种疏松多孔的胃漂浮缓释片剂(图3),该片剂在烘干后具有低密度的特性,通过调节片剂填充率可实现长达8 h的药物缓释以及稳定的漂浮性能。

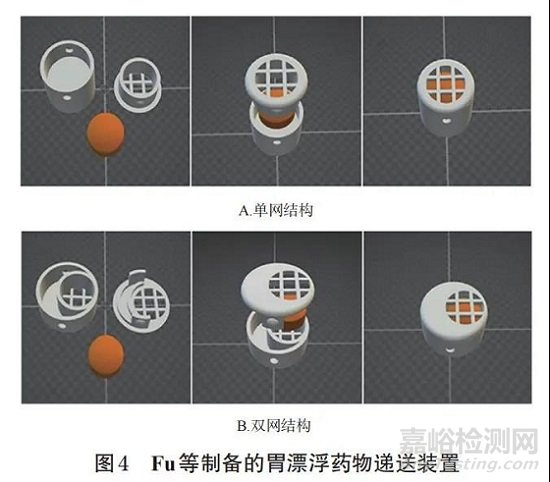
Fu等[24]进一步利用FDM技术制备了一种结构复杂的药物递送装置(图4),该装置具有独立的空气仓和载药仓(单网和双网结构),将直接压片法获得的片剂装载于载药仓后,可实现72 h的药物缓释并可在释药期间保持稳定的漂浮。
此外,Wu 等[25]尝试将磁靶向技术与 3D 打印结合,制备了一种具有磁靶向能力的双相药物递送系统(图 5),在两边的醋酸纤维素膜上分别装载布洛芬和对乙酰氨基酚,中间以含有磁性纳米颗粒的聚己内酯连接,折叠装载于胶囊壳中以便于患者服用。该研究显示,在外部磁场的介导下,复合膜可长时间滞留于胃肠道中的特定位置,有利于药物递送系统在胃肠道中靶向缓释药物,初步验证了3D打印在开发具有胃肠道局部靶向缓释特性的多药载体中的可行性。总而言之,利用3D打印制备具有不同3D结构特征的制剂,可实现对药物溶出度的调节,结合局部靶向递药的理念,有助于设计具有特定药动学特征或针对特定部位精准释药的新剂型。

1.3 植入物
植入物可以将药物有效地递送到作用部位,但是传统的植入物难以根据患者的年龄、解剖学差异、性别和疾病情况等实现个性化植入,这可能会降低治疗效果并带来安全性问题,而3D打印技术的快速发展推动了植入物在个性化治疗中的研究与应用[9]。Yi 等[26]采用 3D打印技术将抗癌药物氟尿嘧啶打印成各种形状和孔隙度的外科手术贴片(图6),并经家兔胰腺肿瘤模型实验研究证明,上述贴片可显著缩小肿瘤体积;同时,该贴片克服了传统化疗药物全身递药的缺点,可将足够剂量的药物精准递送至肿瘤部位,可大幅度降低化疗药物在其他组织器官中的分布,减少毒副作用。

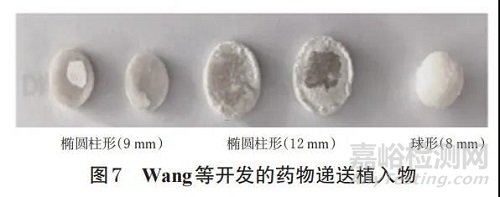
Wang等[27]则根据肿瘤解剖学和生物力学设计了球形和圆柱形植入物模型并3D打印成型(图7),实现了化疗药物的局部递送,表现出良好的生物降解性和生物相容性。
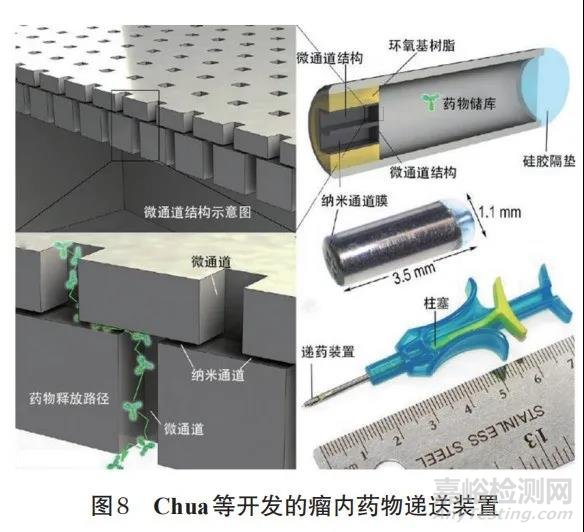
该研究团队随后进行的大鼠骨肉瘤模型研究结果表明,以瘤内注射甲氨蝶呤、顺铂、多柔比星或环磷酰胺为对照,每种药物的植入物均在体内实现了长达12周的药物持续释放,且病灶组织中的药物浓度显著高于血药浓度,可显著抑制骨肉瘤的生长。为了实现持续的局部药物递送并避免反复的肿瘤内注射,Chua等[28]开发了一种基于纳米流体的肿瘤内药物递送装置(图8),该装置主要由药物储库和控制药物释放的微通道结构组成,可通过微创套管针法进行瘤内植入,实现局部持续释药,以减少给药频次。该研究团队经4T1原位小鼠乳腺癌模型研究发现,与瘤内注射给药组相比,该瘤内递送装置可显著抑制肿瘤细胞的增殖,并显著减少小鼠的肝损伤。可见,3D打印可根据病灶或手术需求定制个性化植入物,以满足不同患者的个性化需求。
1.4 复方制剂
联合用药通常是多种单方制剂的联用,患者需要同时服用多种药物,存在漏服、错服和单次服用数量多的问题,且传统制药工艺难以制备个性化制剂,这使复方制剂的应用受到了很大的限制。在药物递送领域中,个性化定制药物组合、药物剂量和释放行为的多功能治疗递药系统已经引起学者越来越多的关注[3]。复方制剂作为一种包含多种药物的固体剂型,对于需要通过多种药物来治疗多种疾病的患者是有益的,可以避免患者单次服用多种药物,提高其用药依从性[29-30]。采用 3D 打印技术可实现多种有效成分的共同装载,可根据患者需求定制各组分药物的释放行为[31]。Gioumouxouzis等[32]将二甲双胍和格列美脲分别嵌入尤特奇缓释层和聚乙烯醇缓释层中,制成抗糖尿病的双相释药系统(图9),两种药物均可在预期的时间内完全释放,表明3D打印技术可为多药联用的治疗方案定制固体制剂。

Siyawamwaya等[33]采用SSE法制备了包含依非韦伦、富马酸替诺福韦酯和恩曲他滨等 3 种抗人类免疫缺陷病毒 1 型 (HIV-1)药物的控释递送系统(图 10),并证明了这 3 种药物在递送系统中相容性良好,实现了肠道靶向和药物控释的功能,且富马酸替诺福韦酯和恩曲他滨的最大吸收浓度均显著优于常规片剂中相同剂量药物的最大吸收浓度。

Khaled 等[34]则制备了一种包含阿司匹林和氢氯噻嗪的速释室以及包含普伐他汀、阿替洛尔和雷米普利的缓释室的共5种活性成分的片剂,用于心血管疾病的治疗。这一多活性固体剂型不仅提高了目前正在服用多种单一药物的患者的依从性,还可以根据患者个人需要随时定制特定的药物组合。为了尽可能地避免不同药物之间的相互作用,提高制剂稳定性,Maroni 等[35]还制备了一种两腔室的药物载体,可将不同药物装载于不同的腔室之中,避免不同药物之间的直接接触(图11)。该药物载体的腔室由速溶、可溶胀、易蚀或肠溶性聚合物组成,可通过调整腔室壁的厚度来控制药物的释放时间,实现双脉冲模式的药物释放。可见,3D打印在个性化和多组分制剂的开发中潜力巨大,可将具有协同作用、服药频次相同的药物制成复方制剂并根据患者实际需求调整各组分剂量和释放行为,有利于提高患者的依从性和疾病的治疗效果。

1.5 外用制剂
口服固体给药是最常用的一种药物递送方式,药物需要经历在胃肠道中溶解并吸收进入血液循环而发挥治疗作用的过程,这可能会增加患者(尤其是老年患者)胃肠道和心血管系统的负担以及副作用的发生率。通过体外局部给药以实现对疾病的治疗是近些年来的研究重点,而3D打印技术的兴起,为个性化外用制剂的发展提供了新的研究方向和应用潜力。Pere等[36]使用甘露醇、木糖醇和海藻糖作为药物载体,应用SLA法制备了一种微针基体,并采用喷墨打印机在微针基体上喷洒胰岛素溶液,可实现胰岛素在30 min内的快速释放。Wu等[37]将 G-胰岛素嵌合到苯基硼酸(PBA)衍生物上得到活性产物,采用SSE法制备圆柱阵列;将此圆柱阵列拉伸后形成针尖,喷以氯化钙溶液固化,经脱水干燥后即可得微针贴片(图12)。该研究发现,相较于传统造模制备微针的方法,此法更为简便、可控。该团队随后的小鼠 1 型糖尿病模型实验结果表明,该微针贴片可利用PBA及其衍生物与葡萄糖结合能力的浓度依赖特性,根据血糖浓度自动调节胰岛素的释放,使得糖尿病模型小鼠的血糖可维持正常水平长达40 h。
Long等[38]将盐酸利多卡因装载于壳聚糖-果胶聚合物水凝胶中并打印成网格状敷料(图 13),用于伤口包扎。该敷料显现出良好的柔韧性、黏合强度高且易剥离,可实现长达 6 h 的药物控释,延长了药物的作用时间。
Liang等[39]制备了一种针对不同患者牙齿特征的个性化载药牙套(图14),采用聚乙烯醇和聚乳酸作为热熔材料、丙酸氯倍他索作为有效成分用于缓解口腔炎症。该研究结果表明,该牙套可在14 h内实现药物的持续释放。
为了使3D打印制备的外用制剂更符合每位患者的实际需求,Goyanes 等[40]将 3D 扫描技术与 3D 打印技术相结合,对患者鼻进行 3D 扫描并构建数字模型,利用FDM法制备了个性化水杨酸鼻贴用以治疗鼻部痤疮(图15),这种技术为生产符合不同患者实际需求的外用制剂提供了可能。可见,3D 打印在外用制剂领域应用潜力巨大,可实现局部精准药物递送且避免了首过效应的发生,提高了药物的递送效率;而与 3D 扫描技术的结合,为精准开发在形状、大小和结构均符合患者个性化需求的外用制剂提供了可能。
2 分布式3D打印中心
3D 打印在药物递送系统研发的研究报道很多,但仍难以实现实际量产,很多学者认为与其成本高、产率低有关[10]。笔者认为,提高 3D 打印设备生产效率固然重要,但更需关注的应是3D打印设备朝小型化智能终端方向发展的潜力。3D打印技术并不会完全取代传统制药技术,而是作为传统制药技术的一个补充,其最大优势在于可为有个性化用药需求的患者提供相应的药物制剂,故小型化的智能终端应是3D打印走向实际应用的重要方向。
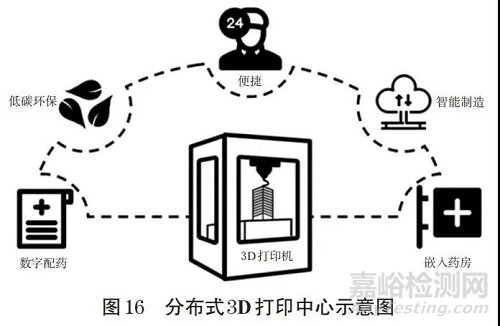
3D 打印作为新兴制造技术的代表,契合分布式制造理念[41]。新兴的分布式3D打印中心可实现患者个性化用药按需制造,例如使用治疗窗狭窄、需要精准控制剂量的药物时[42],或多种药物联合使用时[34],或需要定制化的药物释放曲线时[22],或可根据患者身体实际需求定制的植入剂时[43]。与此同时,相较于传统集中式生产,按需生产的分布式3D打印中心可减少药品说明书和内外包材的使用、药物运输和洁净区维护等造成的化石能源浪费[44]。分布式3D打印中心示意图见图16。
尽管分布式3D 打印中心拥有以上种种好处,但在现阶段中,从集中式的生产转向分布式制造,仍面临着监管、伦理道德以及法律方面的问题[45]。3D打印应用于实际也面临着诸多挑战,如数据传输与存储的安全性、中间材料的运输与储存、质量控制与监管、防伪与溯源等。当然,随着相关研究的深入,一些解决方案正在被逐步提出。在防伪与溯源方面,Trenfield等[46]提出了通过 2D 打印与 3D 打印相结合,将二维码印刷于 3D 打印制剂上,通过智能终端(如智能手机)即可实现产品的防伪和溯源。在质量控制方面,Zheng等[47]将市售制剂与适当的辅料组合并于超净台下完成制剂打印,制备了不同剂量规格的螺内酯片,并在住院患者中进行了应用。相较于传统手工分剂量的方式,3D 打印的螺内酯分剂量片具有剂量更准确和更个性化的特点,提示3D打印技术还可成为一种医院药品调剂的新方法。由广东省人民医院与广东药科大学共同制定的《医疗机构3D打印药品分剂量片技术规程》团体标准已于2020年底开始实施,在一定程度上规范了 3D 打印制剂的生产过程。现阶段,开发适用于3D打印制造流程的监管制度、安全的数据传输与存储系统是十分迫切的;此外,还需进一步完善3D打印制剂的生产操作规程、现场质量控制方法、防伪溯源方案等。
3 讨论
正如前文所述,3D 打印可用于开发多种结构新颖或具有个性化要求的药物递送系统,但不同细分技术仍存在着局限性。其中,SLA的分辨率是最高的,最适用于开发高精度产品,但其载药基质为光敏材料,种类少,且要求药物对光稳定[6]。粉末3D打印最适用于速释制剂的生产,但通过打印液溅射实现固体粉末黏结的方式易造成制剂机械强度不足。FDM是目前研究最广、成本最低的3D打印技术,打印过程需要对材料进行热熔加工,不适用于热不稳定的原辅料[10]。SSE也称生物3D打印技术,起步较晚,工艺条件温和,被广泛应用于生命科学领域;但该技术要求其原辅料能形成相对稳定的膏状物体系,且为非压缩式生产工艺,需要特别关注其膏状物体系的稳定性和制剂的机械强度[48]。总之,3D打印技术在开发新型递药系统潜力巨大,开发时可根据目标制剂的功能和处方组成选择合适的细分技术。
尽管传统制药工艺可以满足大多数患者的用药需求,但也存在着一定的局限性:工业化大批量固定规格的生产模式,有利于制剂质量的控制,且成本较低,但难以实现个性化制剂的生产。3D打印精准的剂量控制和灵活的形状定制能力,可实现对药物剂量、释放行为和局部靶向等的控制。目前3D打印技术仍存在着部分缺陷,如成本高、产量低、操作难度大,但相信这些问题会随着技术的进步而得以解决。随着3D打印技术的成熟以及其与分布式制造的结合,有望实现3D打印落地基层医院及药房,并实现按需定制和个性化给药。










来源:中国药房


