您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-12-31 16:16
口服药物在服用后要溶解,吸收后才能起到药效作用。溶解、吸收都在胃肠道中,胃肠道的环境影响着药物的溶解吸收。因此了解体内胃肠道生理至关重要。本文从影响溶解和吸收的因素、胃肠道特性来对体内胃肠道生理环境进行阐述,增加对胃肠道生理环境的了解。
影响溶解和吸收的因素
吸收是最终将口服给药的药物带入肠膜以转移到血流中的过程。在吸收之前,药物必须溶解,并且药物可以在胃肠道中局部起作用。因此,从根本上理解影响溶解和吸收的关键药物特性非常重要。例如,根据Amidon等人的研究,吸收的药物比例是药物溶解度,剂量和胃肠道通透性的函数。根据方程1,穿过肠壁的药物通量Jw是依赖于肠壁通透性,Pw (有效通透性),以及药物在壁上的浓度,Cw。该等式适用于沿膜的每个点,假设每个参数取决于时间和位置,并假设上皮细胞中的药物浓度基本上等于零。假设没有腔反应,吸收率由方程式2给出,其中A是可用于吸收的区域(即,与药物接触的膜表面),m是质量。

通过研究简单的Noyes-Whitney方程可以理解影响溶解的因素

药物溶解的质量随时间的变化。其中M是质量,D是药物扩散系数,A是可用于溶解的药物表面积,h是流体动力学边界层的经验厚度,Cs 是固体液体界面的溶解度,Cb 是原料药浓度。
从以上可以看出,体内的溶解和吸收取决于生理环境的性质和药物本身的性质。关键的生理参数包括胃肠道的尺寸,液体的体积和成分,液体流体动力学(即流速,胃排空率,剪切率)和肠膜的性质。重要的药物特性包括剂量,溶解度,pKa,扩散系数,渗透性和粒径。表1中提供了影响口服药物溶出和吸收的更完整的药物特性和生理特性表1。
表1 药物特性和生理特性

胃肠道特点
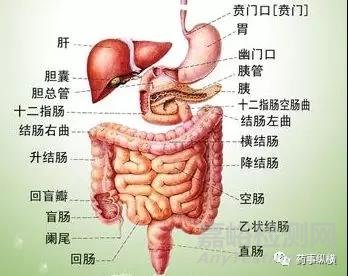
图1.胃肠道示意图
1、组成
胃:胃液由唾液,胃分泌物,膳食食物和液体,以及来自十二指肠的回流液体组成。胃液成分随着液体的混合和输送到十二指肠而变化。主要成分包括氢离子浓度、胆盐、脂肪酶和蛋白质消化酶胃蛋白酶
小肠:肠上部的液体成分由胃中的乳糜以及肝脏、胰腺和小肠壁的分泌物组成。成分受流体分隔、混合模式、流体进入肠壁的吸收以及沿肠道传输的影响。胰腺的分泌物包括碳酸氢盐和蛋白酶(主要是胰蛋白酶和胰凝乳蛋白酶),淀粉酶和脂肪酶。肝脏分泌胆汁,胆汁含有胆汁盐,磷脂,碳酸氢盐,胆固醇,胆汁色素和有机废物。小肠壁分泌矿物离子,如碳酸氢盐,钠和氯,以及水。分泌碳酸氢盐以中和胃肠腔和十二指肠中的胃分泌上皮细胞保护十二指肠上皮免受酸相关损伤。由于食物摄入引发小肠中的许多分泌物,所以进食状态肠液的组成可以与禁食状态肠液变化很大。当在进食状态和禁食状态下给药时,组合物的这种差异可以部分地导致生物利用度的差异。对于某些药物在进食状态下所见的生物利用度增加可归因于由于胆汁和胰腺分泌物以及外源性脂质产物的存在而增强的肠液增溶能力。
2、pH
胃肠道pH随着不同位置和不同时间不一样,汤丽娟老师在同写意培训上的ppt中介绍了不同位置进食和禁食的pH。见图2。
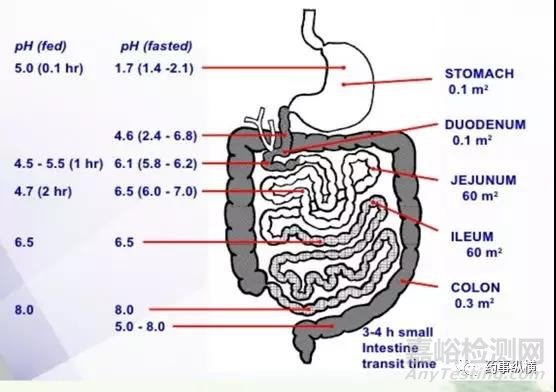
图2.胃肠道中典型pH值的近似值
通过Clarysse等人测量的五个健康志愿者在禁食和进食状态下的个体和平均值pH与时间的关系图。如下图3所示。
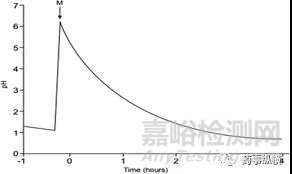
图3.胃中典型pH值的近似值。字母“M”表示食物摄入量
3、肠道传输时间
药物在肠道中的(即停留时间)是溶解和吸收的强决定因素。它影响药物在胃肠道中溶解和吸收的时间。剂型在胃肠道的不同区段中的通过时间取决于诸如胃排空率和流速的因素,个体内也显著变化。
从人体胃中排空盐水的半衰期为12分钟,有发现将300毫升水排空的半衰期为15.8分钟。餐后胃排空很大程度上取决于膳食大小和成分。有人从文献中总结了人类典型的固体食物半排空率,发现它们的范围从70到130分钟。
在禁食状态下,约3-4小时的小肠转运时间显著长于约15-60分钟的平均胃停留时间。此外,也有报道在盲肠和结肠中的停留时间分别为约3-7小时和12-24小时,也显著长于所报道的小肠平均3小时的停留时间。
食物对胃肠道运输有较大影响。汤丽娟老师在同写意培训上的ppt中介绍标准美国低纤维餐和高纤维餐的滞留时间比较,见下图。

图5 标准美国低纤维餐和高纤维餐的滞留时间比较
4、其他胃肠道特性

5、疾病的影响
胃内的pH受病理生理条件的影响,如胃酸分泌减少或缺乏,或高胃酸分泌症(胃酸分泌过多且pH< 2)和如受H2受体拮抗剂和质子泵抑制剂的影响的艾滋病。这对弱碱性药物的溶出度和生物利用度有影响;酮康唑在胃pH升高的艾滋病患者中的生物利用度降低。另一项研究观察了药物引起的胃酸缺乏(使用质子泵抑制剂奥美拉唑)的影响,显示酮康唑的生物利用度降低。有趣的是,通过与酸性饮料(可口可乐)一起给药,它们能够比对照(水)提高65%的生物利用度。
6、微生物
细菌在胃肠道中无处不在。与胃肠道中的细菌浓度相比,胃和近端小肠中的细菌浓度适中,这使得结肠中的高细菌浓度成为一个独特的特征,并且影响腔体环境以及药物和剂型行为。肠道中有超过1000亿个细菌和400个不同的物种,它们发酵未消化的物质,具有代谢活性,并影响下肠道的氧化还原电位和pH。
药物治疗(质子泵抑制剂、阿片类药物、抗生素)饮食或疾病可能导致微生物区系波动。特别是,转运时间改变的条件,如肠易激综合征和炎症性肠病,可以改变细菌数量;结肠运输缓慢导致细菌增多。
微生物触发的药物释放是我们如何利用胃肠道条件来控制药物释放的一个例子,并且在直链淀粉(COLALTM)的情况下非常成功。但是必须还考虑其他。1000亿个代谢活性细菌对药物稳定性有潜在的严重影响。事实上,已经有人提出胃肠道微生物群落有能力作为一个器官,其代谢潜能等于或大于肝脏。迄今为止,已有30多种药物被确定为肠道细菌的底物,其中包括奥美拉唑、地高辛、拉尼替丁、尼扎替丁和硝基安定。一种药物的细菌代谢有三种潜在的药理学结果:不活动、活性或毒性。后者的一个重要而令人担忧的例子是1993年在日本使用了sorivudine。这种药物通过肠道菌群转化为(E)-5-(2-溴乙烯基)尿嘧啶,在5-氟尿嘧啶存在下,(E)-5-(2-溴乙烯基)尿嘧啶会变得剧毒。在到达日本市场后的40天内,sorivudine与口服5-氟尿嘧啶前药联合造成18名患者的死亡。不久,索里夫定就被从市场上撤回。这不仅突出了研究药物细菌代谢的重要性,而且它们对药物相互作用的影响。
结 论
通过以上汇总可以看出,体内生理环境是个复杂多变的环境,个体差异也比较大((文献1和文献2对此进行了详细的说明,感兴趣读者可以阅读),这对药物的研发提出巨大的挑战。随着技术的发展,对体内的研究也越来越详细,在平时的工作中要与之联系。
本文为笔者学习各个文献的读书笔记,限于笔者水平不正之处敬请指正。
参考文献
1. Deanna M.Mudie, Gordon L. Amidon, and Gregory E. Amidon .Physiological Parameters forOral Delivery and in Vitro Testing
2. Emma L. McConnell, Hala M. Fadda, Abdul W. Basit.Gutinstincts: Explorations in intestinal physiology and drug delivery .InternationalJournal of Pharmaceutics 364 (2008) 213–226
3. 应用生物药剂学与药物动力学第13章 .【美】L.夏盖尔吴幼玲余炳灼著李安良等译(原著第五版)
4. YasuhiroTsumea, Deanna M. Mudiea, Peter Langguthb, Greg E. Amidona, and Gordon L.Amidon. The Biopharmaceutics Classification System: Subclasses for in vivo predictivedissolution (IPD) methodology and IVIVC
5. 汤丽娟.同写意培训PPT.人体生理环境与BCS分类的应用

来源:Internet


