您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-04-22 13:55
面对新药的难溶性,对于制剂开发人员来说,确实不像普通口服固体制剂开发那样轻车熟路,但是也不是无计可施。粒径减少(粉碎、微粉或者纳米晶)在一定程度上提高了制剂的溶出;而成盐,共晶筛选,无定形固体分散体或者脂质制剂在提高溶解度的同时,也可以提高制剂的溶出。当然不同的产品需要“因材施治”,根据项目的独特性,选择恰如其分的技术路线。
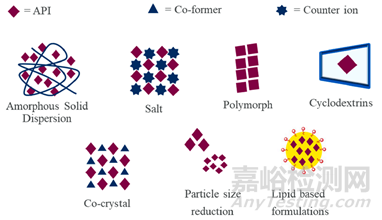
难溶性药物常见增溶策略(来自于参考文献1)
一个选择恰如其分的技术路线,需要从一下四个维度进行考虑:
1)化合物特性:
①物理化学性质
在口服固体制剂开发过程中,一个至关重要的研究过程便是处方前研究。处方前研究的重点工作便是化合物物理化学性质。最基础的起点便是化合物分子的结构特征,而化合物的特征又尤其特征官能团和基本框架所决定。分子间的作用以及分子自身的构象、互变等构成了不同的晶体结构,即多晶型现象。分子如若以长程无序,短程亦无序的状态存在,这变称之为无定形态。
口服制剂开发一般选择众多晶型中,最稳定的晶型作为开发晶型,稳定可控,易于制定质量标准,稳定来源于体系内分子间牢牢的作用力,整个体系处于最低能量状态。但是这有一个不利的后果,便是晶体晶格能太强,分子间牢牢缩合,溶剂分子无法突破溶质分子间的作用,造成了化合物难以溶解。
结构决定性质,一个化合物的性质由其基本的结构特征所决定,而由许多化合物分子堆叠构成的晶体药物的性质由化合物分子的性质所决定,而由晶体药物聚集而成的粉体性质则由化合物分子的性质和晶体特性所决定。难溶窥其根源也不过是化合物分子特异性结构所致。
除了上面说的固态性质,化合物理化性质还有很多,如溶解度,引湿性,稳定性,pKa,LogP,熔点,分子量,原辅料相容性等等。下图对化合物的性质之间的关系进行了总结。
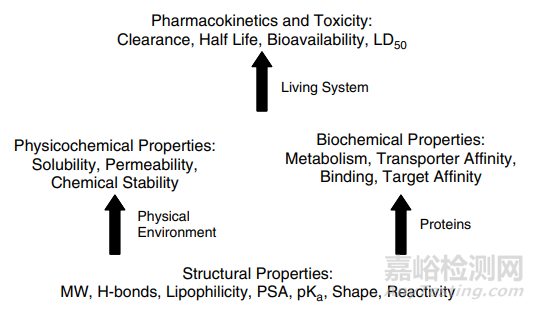
Compound structure determines the fundamentalproperties that determine physicochemical and biochemical properties, whichultimately determine pharmacokinetics and toxicity
(来源于参考文献2)
无论进行何种制剂开发,全面了解化合物相关的性质是绝对不可少的,是研究基线,也是制剂后续开发疑难问题的根源。普通口服固体开发一般选择优势晶型进行开发,而固体分散体则是反其道而行之,这种固态性质的根本性改变,完全改变了研究的难度。如何根据收集到的化合物理化性质,做进一步开发决策不是本文的主要研究内容。
②生物学性质:制剂开发中我们把很大的中心放心处方前,处方工艺开发,对于药物的生物学性质其实关注是不够的,甚至很少去关注药物在临床开发中药物的ADME过程,制剂开发部门与临床前GLP执行部门有断裂的情况发生。
在某些情况下,仅仅通过克服低吸收的物理化学障碍可能不会产生所需的BA水平。在这些情况下,暴露的生物障碍可能很明显,包括
•吸收的药物回流到肠腔(通常是P-gp或BCRP转运蛋白介导),
•肠道中的系统前药物代谢(主要通过细胞色素P450酶),以及
•广泛的肝脏首过药物代谢
一个很好的例子强调了实现高药物吸收但低BA的可能性是睾酮。尽管其水溶性相对较低(<25µg/ml),但睾酮能很好地从肠道吸收,但在广泛的首过代谢后显示出极低的BA。像这种情况一味的想着增加溶解度,但是还是无法提高药物体内吸收的生物利用度。
技术选择离不开对于化合物特性的表征收集和总结,当然获取了大量的信息如果通过一些手段去预测药物的体内吸收情况,或者对于技术的选择具有指导的作用那也是极其好的。在广泛的研究与考察的基本上,尽可能获取多的数据去支持我们进行增溶手段的决策,找到限制药物血药浓度的“七寸”。
2)预测手段
药物产品在人体体内的实际的情况,在临床前是无法获取的,一来鉴于产品的安全性问题,需要有关部门的审批批准;二来临床试验需要大量资源的投入,不可能轻而易举的开展临床试验,需要建立在相关的研究结果之下,三来不可能事事需要提高试验去确认。那么,在能否有手段去预测人体体内的情况呢,其实这也是生物药剂学与药物动力学一个重要的发展方向。下表也给出了预测性的理论的发展历程。目前,新出了许多的通过体外研究数据预测人体体内吸收的理论或者软件,如PBPK。

来源于参考文献3
3)市场需求
①最终产品的目标概况:中国目前开的新的药物大多数属于me-too、me-better产品,一般也有fast follow的阳性化合物。一般阳性化合物的剂型大小、形状、外观和包装都会成为国内创新药制剂产品的开发依据或者参考,毕竟分子结构有所差异,但是终究是差异不大。当然了,选择不同的技术平台可能也会略有不同,特别是在结构改造的同时,导致化合物性质发生了质的变化的,如溶解度极具的降低,不得不开发更加难以控制的制剂策略。在化合物筛选时,关注构效关系的同时,也应关注结构与化合物性质间的关系,如何在保证药效的前提下,尽可能关注到化合物的理化性质足够满足生产、放大及制剂开发的需要。
②产品的临床顺应性
固体分散体由于API以无定形形式分散在聚合物分子里面,通常载药量在10-30%,特别对于化合物无定形形成能力较差的化合物,就需要更多的聚合物去保证其稳定性,以防止转晶的发生,这样就造成了制备的固体分散体中聚合物的量较多,加之添加额外的填充剂,崩解剂,润滑剂去制备成制剂,最终产品质量过大,病人难以吞咽,造成临床的投诉。
固体分散体在原料药的基础上,加入一倍以上的聚合物分子来保证药物无定形的稳定,至少在货架期的无定形形态不改变,这样往往造就了最终制剂产品的“大肚子”。适时调整片剂形状或者寻求对于高负载剂型的开发,需要在项目立项之时,关注这个方面。
4)开发经验及实验室车间条件
众所周知,固体分散体技术已经发展60来年了,但是FDA批准上市的产品不过30来个,可见固体分散体开发之路不是那么的艰难,需要花费时间,投入资源,一来修炼本领,去领悟去模仿去掌握去利用去创新,二来打造自我开发平台,摸索中前行以获取经验,经验中创新以制造壁垒。固体分散体与传统固体制剂相比,仅仅多了一步固体分散体的制备,其实工业上也主要采用喷雾干燥和热熔挤出。设备操作简单,易于放大生产。但是固体分散体最基本的理论基础涉及到热力学、动力学,其表征手段之多,如DSC、XRD、PLM、DVS、IR、Roman等。如何正确认识固体分散体这项技术,如何去切实掌握其开发秘诀,如何在新药开发中切实解决难溶性药物的问题?这些都需要去学习,模仿,掌握。
参考文献:
1.Amorphoussolid dispersions: Utilization and challenges in preclinical drug developmentwithin AstraZeneca.
2.Advantagesof Good Drug-like Properties: concepts, structure design and methods
3.Rate-and Extent-Limiting Factors of Oral Drug Absorption: Theory and Applications
4.Pharmaceuticalamorphous solid dispersion: A review of manufacturing strategies
5Technology Selection for Bioavailability Enhancement

来源:药事纵横


