您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-04-28 10:35
脱敏剂通常为单组份或双组份液剂、糊剂或凝胶。根据不同的作用机理,可以分为以下几种:
1.1无机填料/再矿化型:发挥脱敏作用的主要成分通常为氟化钠、氯化锶或羟基磷灰石等;其余成分可能包含摩擦剂(如碳酸钙、磷酸氢钙、二氧化硅等)、润滑剂(如甘油)、赋形剂、调味剂等。
1.2胶原变性封堵型:例如以戊二醛为主要成分,其余成分可能包含2-羟乙基甲基丙烯酸酯。
1.3薄膜封闭型:例如涂布后可迅速形成透明薄膜覆盖于牙本质表面。
以上几种类型可能是单一成分发挥脱敏作用,也可能是几种成分协同发挥作用。此外,还可能有其他脱敏成分的产品,如含有硝酸钾、精氨酸或单氟磷酸钠等。
在产品结构组成中应规范完整表述各组分的名称,原则上不能采用“等”字概述;应明确产品所含水质级别,如纯化水。
2.产品工作原理/作用机理
临床使用较为普遍的脱敏剂产品主要通过堵塞牙本质小管,减少液压传导从而脱敏,如下图所示:
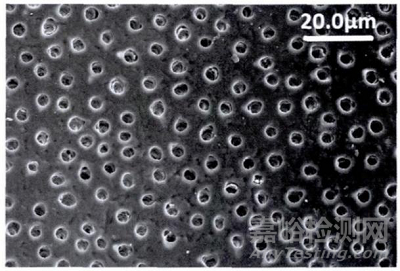
脱敏剂处理前的牙本质表面扫描电镜图(×1000)

脱敏剂处理后的牙本质表面扫描电镜图(×1000)
根据不同的作用机理,脱敏剂可以分为无机填料/再矿化型、胶原变性封堵型、薄膜封闭型等。①无机填料/再矿化型:例如含氟化钠的脱敏剂,通过氟离子参与到牙齿表面羟基磷灰石的溶解再沉积过程,形成氟化钙、氟磷灰石并沉积封堵,促进牙齿再矿化,同时起到防龋及脱敏的效果;含氯化锶的脱敏剂通过形成难溶性锶盐,如碳酸锶、锶磷灰石沉积在牙本质表面实现封堵;含羟基磷灰石的脱敏剂,羟基磷灰石在形态结构方面和牙釉质中磷灰石晶体结构十分类似,可促进牙齿再矿化,进而堵塞暴露的牙本质小管,起到脱敏的作用;②胶原变性封堵型:如含戊二醛的脱敏剂,戊二醛使牙本质小管中的液体蛋白变性、凝固,封堵牙本质小管,2-羟乙基甲基丙烯酸酯可溶于牙本质小管液,协助戊二醛进入小管内发挥作用,从而达到脱敏目的;③薄膜封闭型:例如产品涂布后可迅速形成透明薄膜覆盖于牙本质表面,起到初期封闭和保护作用。
以上描述来源于已上市产品信息及参考文献,未列举完全,仅供参考。注册申请人应结合申报产品特点论述产品作用机理,明确各组分的作用及构成比例设定的依据,是单一发挥作用还是协同发挥作用。
3.型号规格
对于存在多种型号规格的产品,应当明确各型号规格的区别。应当采用对比表及带有说明性文字的图片、图表,描述各种型号规格的结构组成、功能、产品特征和性能指标等内容。
4.包装描述
以图示及文字描述的方式说明所有产品组成的包装信息。
6.适用范围和禁忌证
6.1适用范围:用于缓解因牙本质暴露而引起的牙齿敏感症状。
6.2适用人群:适用于有牙本质敏感症的人群。
6.3预期使用环境:一般在医疗机构、牙科诊所内使用;部分产品可能多次使用或家用,应说明谨遵医嘱或在专业人士指导下使用。
6.4禁忌证:应明确产品可能存在的禁忌证,至少包括已知对脱敏剂成分过敏者禁用。
7.不良事件情况(如适用)
应当提交申报产品的上市、销售、不良事件和召回等相关情况分析资料。
(三)非临床资料
1.产品风险管理资料
应对牙科脱敏剂进行风险分析(参照YY/T 0316《医疗器械风险管理对医疗器械的应用》),对产品生命周期全过程实施风险管理。以下依据YY/T 0316附录E列举了牙科脱敏剂的主要危害举例(见表1)。
表1牙科脱敏剂的主要危害举例
|
危险(源) |
可预见的事件序列 |
危险情况 |
|
|
生物学和化学危险(源) |
生物污染 |
包装破损或使用时操作不规范造成生物污染;产品微生物指标过高 |
产品带致病菌,引起患者身体不适或感染 |
|
环境污染 |
生产环境污染产品,如外来的粉尘、微生物、其他杂质等 |
引起患者身体不适或感染 |
|
|
生物相容性 |
采用了不合格原辅材料;生产引入了外来物质 |
产生毒性或刺激 |
|
|
化学危害 |
生产工艺控制不严 不正确的配方(化学成分) 未按照工艺要求配料 添加剂或助剂使用比例不正确 氟离子含量超出安全范围 |
造成毒性危害 |
|
|
操作 危险(源) |
由不熟练/未经培训的人员使用 |
操作不熟练、操作失误 |
无法保证使用安全性 导致操作失误,导致无法达到满意的脱敏效果 |
|
使用产品时未按照说明书中操作方法操作 |
错误操作;未采取相应的保护措施 |
无法保证使用安全性 导致操作失误,导致无法达到满意的脱敏效果 |
|
|
忽视说明书中禁忌证、警示信息等内容 |
患者在使用过程中出现过敏;产品接触到牙龈、皮肤、眼睛等其他部位 |
引起患者过敏,牙龈、皮肤、眼睛等其他部位产生刺激性 |
|
|
信息 危险(源) |
不正确的标签 |
外部标记不全面、标记不正确或不能够清楚易认 |
错误使用;储存错误; 产品辨别错误 |
|
不正确的说明书;说明书上的注意事项、禁忌证不全 |
缺少详细的使用方法、必要的警告说明 |
错误操作;无法保证使用安全有效性 |
|
|
对医疗器械寿命终止缺少适当的决定 |
没有标识产品有效期 |
超出有效期的产品被使用,或因材料老化产生而导致产品性能不符合要求 |
|
|
不适当的产品包装(产品污染和/或变性) |
生产、运输、搬运和储存过程中导致包装破损;包装封口不严密;包装材料选择不适当;使用前未检查产品包装状态 |
产品使用性能无法得到保证 |
|
|
再次使用和/或不适当的再次使用 |
未说明产品配件(如有)使用方法;产品多次使用,未说明具体操作方法 |
出现细菌感染、交叉感染等现象 |
|

来源:嘉峪检测网


