您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2022-05-20 06:05
摘要:本文对《中国药典》2020年版三部通则3601进行解读,主要对该通则的主要特点、内容以及质量控制指标等进行阐述,为通则的实施提供参考。
关键词:生物制品;实验动物;质量控制
Abstract: The paper interprets the General Principle 3601 of the Chinese Pharmacopoeia 2020 Volume III, and emphasizes on characteristics, contents and quality monitoring, which provides a reference for the implementation of the General Principle 3601.
Key words: biological products; laboratory animals; quality monitoring
实验动物作为生物制品的起始原材料或用于产品质量检定,与产品的安全性和有效性密切相关,因此,进一步完善实验动物的质量控制尤为重要。《中华人民共和国药典》(简称《中国药典》)2015年版三部“实验动物微生物学检测要求”(通则3602)和“实验动物寄生虫学检测要求”(通则3603)整体要求偏低,引用的实验动物标准为2001年版国家标准(GB),未随着新的国标修订而更新;同时,相关要求与国际上先进技术标准也存在差异。《中国药典》2020年版三部基于我国国情,结合国际标准相关要求,对原通则内容进行了增修订,以进一步提升我国生物制品质量和产品的国际竞争力。本文介绍了《中国药典》2020年版三部通则3601主要内容,为标准的贯彻实施提供参考。
1 2020年版修订的基本考虑要点
1.1 科学性
用于生物制品生产与检定的实验动物,其质量要求有所不同,前者主要考虑实验动物本身对制品带来的风险,而后者侧重于保证动物试验结果的稳定性。因此,本次修订分别制订了检定用实验动物和生产用实验动物的质控标准,体现其用于不同目的时对实验动物质量要求的区分,强化使用动物组织或细胞生产人用生物制品的质量和安全性保障,突出标准修订的科学性。
1.2 先进性
参考美国、欧盟、日本等药典的最新要求,以及国际实验动物相关机构如ICLAS(International Council for Laboratory Animal Science)、FELASA(Federation of European Laboratory Animal Science Associations)等国际行业技术标准进行本通则增修订,体现技术要求的先进性[15,9]。
1.3 协调性
不再直接引用实验动物国家标准(GB),建立符合生物制品特点的实验动物质控标准,避免因《中国药典》未与GB同步更新而导致相关技术要求滞后或不一致的情况。
2 修订的主要内容
2.1 凡例修订内容
本版药典凡例关于实验动物的要求,突出强调了对检定用动物体重和日龄的对应关系。此前药典仅要求动物的体重范围,未对年龄提出要求,导致同一体重范围的动物日龄有差异,由于不同日龄动物生长发育阶段不同,其生理反应不同,可能导致检定结果出现偏差。对于检定用动物级别依然要求清洁级以上。
此外,对于小鼠遗传特性方面,基于近交系小鼠遗传特性更加稳定,更有利于生物检定的考虑,在原要求“应来自封闭群动物 (closed colony animals) ”的基础上,增加了近交系动物(inbred strain animals)的要求。
2.2 实验动物质量控制通则的主要内容
2.2.1 定义、等级与动物种类的选择 明确生产用和检定用实验动物的定义,前者是指用于生物制品生产的实验动物,后者是指用于生物制品检定的实验动物。
微生物和寄生虫等级,沿用《中国药典》2015年版分类体系,按照实验动物携带微生物与寄生虫情况分为普通级实验动物[conventional (CV) animal]、清洁级实验动物[clean (CL) animal]、无特定病原体级实验动物[specific pathogen free (SPF) animal]、无菌级实验动物[germ free (GF) animal]四个级别。依据生物制品各论所涉及的动物类别,建立了小鼠、地鼠、长爪沙鼠、家兔、豚鼠、猴、马和SPF鸡等常用8种试验动物的质量要求。
2.2.2 通用要求 明确本通则是对生物制品生产用和检定用实验动物微生物与寄生虫的质量控制要求,且实验动物管理应符合国家相关要求。疫苗生产与检定应采用适宜级别的实验动物,具体应符合相关各论的要求。
增订实验动物质量检测频率一般不少于3个月,SPF鸡检测频率为4~8周1次的要求。强调从源头进行质量控制,选择符合要求的供应商。
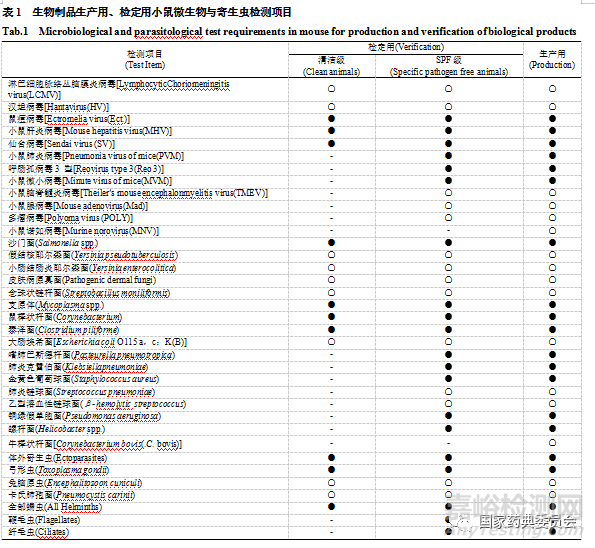
2.2.3 检测项目指标 生物制品常用8种动物的具体检测项目要求见表1~8。其中必须检测项目,是指在日常检查时必须定期检测,用●表示;必要时检测项目,是指在供应商评估或者怀疑有感染时进行检查,根据需要而定,用〇表示。-为不要求检测的项目。
小鼠,分为生产用和检定用两大类,检定用小鼠细分为清洁级和SPF级,检测项目有所区别(见表1)。与GB14922.2[6]相比增加了诺如病毒、牛棒状杆菌检测项目。
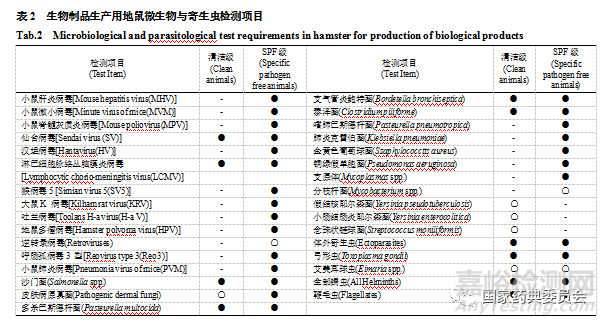
地鼠仅限于生产用动物,检测指标设定主要是参考WHO TRS980[8],比现有GB14922.2增加了10项检测指标(见表2)。
长爪沙鼠作为我国特色实验动物,仅限于生产用动物,指标设定主要参考已发布的DB11/18092020[12],为SPF级动物(见表3)。
《中国药典》2015年版三部仅一个品种使用生产用家兔,具体要求为符合普通级,本版药典通则未单独制定生产用家兔微生物与寄生虫学检测项目及要求。但考虑到实际情况,将检定用家兔分为普通级和清洁级标准,具体要求均引自GB14922.22011[6]和GB14922.12001[7],供使用者选用(见表4)。
猴作为生物制品常用实验动物,既用于生产也用于检定,本版药典通则设定了两个类别。指标上主要考虑对制品的影响,基于麻疹病毒是一种稳定的单型病毒,一旦种群感染难以彻底清除,从而干扰试验研究;猿猴空泡病毒40常污染猴肾细胞生产的生物制品,如脊髓灰质炎疫苗,造成疫苗的废弃,蒙受经济损失;猴副流感病毒在猴群中多呈隐性感染,但在组织器官尤其是猴肾细胞中广泛存在,是猴源细胞培养物中的常见污染物,对使用猴源细胞进行的研究工作及生产的生物制品可产生严重的干扰,因此要求应排除麻疹病毒、猿猴空泡病毒40、猴副流感病毒5型(SV5)的感染(见表5)。

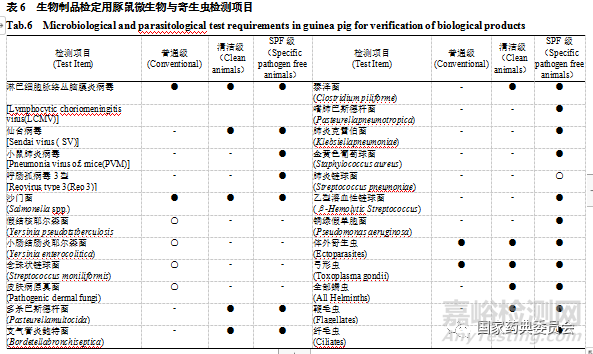
豚鼠主要用于生物制品检定,本版药典通则对其微生物和寄生虫学检测的要求引自GB14922.22011和GB14922.12001,考虑到生物制品实际情况,保留了普通级(见表6)。
鉴于马免疫血清制品生产需要,对马的微生物检测项目进行了调整,由原来的4项增加到6项,主要依据农业部门马属动物产地检疫规程新增马流行性感冒和马鼻腔肺炎2项检测(见表7)[1011]。

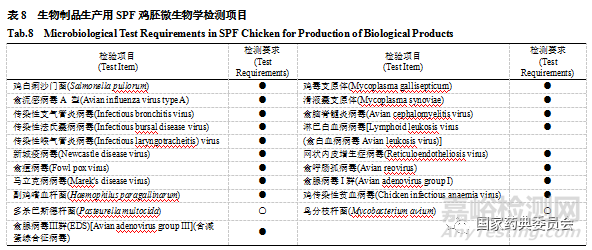
SPF鸡的标准主要依据GB/T 179992008[13]以及WHO等质量标准,本版药典通则新增禽结核杆菌(鸟分枝杆菌),主要基于该病原菌对禽类造成慢性消耗性疾病,且一旦感染,很难清除(见表8),此外,人、哺乳类动物也会感染禽结核杆菌。
3 讨论
《中国药典》2020年版和现行国家标准(GB)均收载实验动物的相关技术要求,两者相辅相成。药典通则3601是以国标相关内容为基础,结合生物制品特点建立的实验动物质量控制要求,重点考虑实验动物对生物制品安全性影响的风险。
《中国药典》2020年版关于实验动物相关通则3601的实施,应基于药典凡例和各论选择符合规定级别、且日龄相近并符合体重范围的动物,并按照通则3601要求进行微生物检测合格后用于生物制品生产和检定。
参考文献
[1] 李冠民,邢瑞昌.国际实验动物科学理事会(ICLAS)情况介绍[J].中国实验动物学杂志,2001,11(2):118
LI GMXING RC. Introduction of international council for laboratory animal science (ICLAS)[J]. Chin J Lab Anim Sci, 2001,11(2):118
[2] M MAHLER (CONVENOR), M BERARD, R FEINSTEIN, et al. FELASA recommendations for the health monitoring of mouse, rat, hamster, guinea pig and rabbit colonies in breeding and experimental units[J]. Lab Anim, 2014, 48(3):178
[3] Routine Health Monitoring of Charles River Rodent Barrier Production Colonies in Europe and North America [EB/OL]. [2022226]. http://www.civer.com
[4] Jackson Laboratory[EB/OL]. [2022303]. www.jax.org/jaxmice/health[5] Oriental BioService Health Monitoring Program[EB/OL]. [2022303]. http://www.oyc.co.jp
[6] 国家质量监督检验检疫总局,国家标准化管理委员会. GB14922.22011,实验动物微生物学等级与监测[S]. 2011
General Administration of Quality Supervision, Inspection and Quarantine of the People′s Republic of China, Standardization administration. GB14922.22011, Laboratory animal—Microbiological standards and monitoring[S]. 2011
[7] 国家质量监督检验检疫总局,国家标准化管理委员会. GB14922.12001,实验动物寄生虫学等级与监测[S]. 2001
General Administration of Quality Supervision, Inspection and Quarantine of the People′s Republic of China, Standardization administration. GB14922.12001,Laboratory animal—Standards and monitoring for parasitology[S]. 2001
[8] WHO Expert Committee on biological Standardization. WHO Technical Report Series (No.980) [M]. 2012:417418
[9] European Pharmacopoeia 8.0 (2013) see http://www. pheur. org/
[10] https://www. oie. int/en/whatwedo/animalhealthandwelfare/animaldiseases/
[11] 中华人民共和国农业部.中华人民共和国农业部公告第1125号[EB/OL]. (20081211) http://www. moa.gov. cn/ nybgb/2009/ dyq/201806/t20180606_6151187.htm Ministry of Agriculture of the People′s Republic of China No. 1125, list of animal diseases category Ⅰ, Ⅱ and Ⅲ, 2008
[12] 北京市市场监督管理局. DB11/T 1809—2020实验动物微生物学检测[S]. 2020
Beijing administration of Market Supervision. DB11/T 1809—2020, Laboratory animal—Microbiological testing[S]. 2020
[13] 国家质量监督检验检疫总局,国家标准化管理委员会.GB/T 17999.12008, SPF鸡微生物学监测第1部分:SPF鸡微生物监测总则[S].2008
General Administration of Quality Supervision, Inspection and Quarantine of the People′s Republic of China, Standardization administration. GB/T 17999.12008, SPF Chicken—Microbiological surveillancepart 1: General rules for the microbiological surveillance for SPF chicken[S]. 2008
《中国药品标准》杂志 2022年第23卷第2期,岳秉飞1, 王吉1, 王淑菁1, 夏放2, 代解杰3, 王锡岩4, 魏强5,孙德明6, 卢选成7, 范昌发1
(1.中国食品药品检定研究院, 北京 102629; 2.成都生物制品研究所有限责任公司, 成都 610023;3.中国医科院医学生物学研究所, 昆明 650031; 4.北京生物制品研究所有限责任公司, 北京 102600;5.中国医学科学院医学实验动物研究所, 北京 100021; 6.国家卫健委科学技术研究所, 北京 100081;7.中国疾病控制中心, 北京 102206)

来源:《中国药品标准》杂志


