您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-06-11 23:24
01概述
药物需要以一定的形式将活性成分释放,进而在体内吸收,从而达到治疗效果。药物传统的剂型包括片剂、胶囊剂、软膏剂以及注射剂,那么为什么要做成这些剂型?制剂进入体内后又都经历了什么过程?而相比于传统的这些剂型,控释给药系统又有哪些优势以及劣势?小编将通过这篇文章简略的讲述剂型的选择、药物的体内过程以及控释给药系统设计的几点考虑。
02剂型
(1)为什么要做成不同剂型
一般来说,药物都是需要通过不同的递送系统进行给药的,原料药直接在临床上使用是比较罕见的,因为直接使用很难控制剂量,并且剂型不合适,也会影响药物的吸收,从而影响药物的生物利用度。那么药物为什么会有不同的剂型呢?有以下两点原因:
①首先我们需要根据临床需求进行给药设计,例如该药物是局部给药还是全身给药,局部治疗如贴剂以及滴眼剂。第二,病人是重症病人还是轻症病人,如果是重症病人,一把不推荐开发常规的口服给药,因为不易吞咽;
②由药物自身的理化性质决定,药物都有一定的缺点,例如味道不好,容易首过代谢,半衰期短等等问题,那么我们就可以通过剂型来克服。如半衰期短,那么我们可以将其开发成控释制剂,有严重的首过代谢效应,那么我们应避开首过代谢,例如开发为舌下片。总之设计成不同剂型的目的就是为了满足临床需求,同时确保产品的安全性以及有效性。
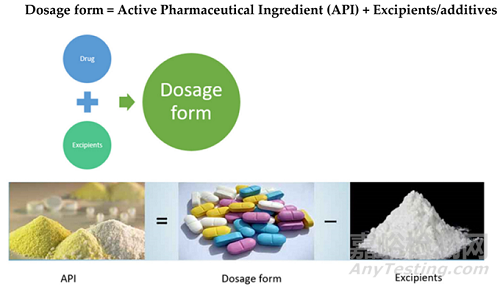
图1 制剂组成
(2)药物BCS分类
生物药剂学分类系统根据药物的渗透性和溶解度将药物分为四类。Ⅰ类药物具有高渗透性和高溶解性,吸收性好。它们的吸收率大于排泄率,如美托洛尔、扑热息痛等。II类药物渗透性高但溶解度低,生物利用度受溶出速率的限制,如格列本脲。III类药物渗透性低但溶解度高,此类药物快速溶解,然而吸收受到渗透性的限制。IV类药物渗透性低、溶解度低,通过肠道吸收差。此类药物适合开发为注射剂。
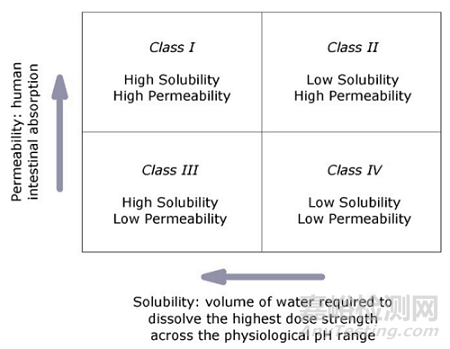
图2 药物BCS分类
(3)辅料
原料药总是与辅料一起制备的。通过添加辅料,可以增加药物的稳定性、掩盖苦味、增加适口性并且有利于放大生产。此外,辅料可提高生物利用度,改善贮存或使用期间制剂的整体安全性或功能,提高患者的耐受性。
(4)不同给药途径
药物具有多种给药途径,最常见的剂型包括片剂、胶囊、丸剂、膏剂、糖浆和注射剂。首选给药途径取决于三个主要因素:即被治疗的身体部位、药物在体内的作用方式以及药物的溶解度和渗透性。例如,某些药物在口服后容易被胃酸破坏,导致生物利用度较低,因此,这类药物可以通过包肠溶衣或者非胃肠道途径给药。
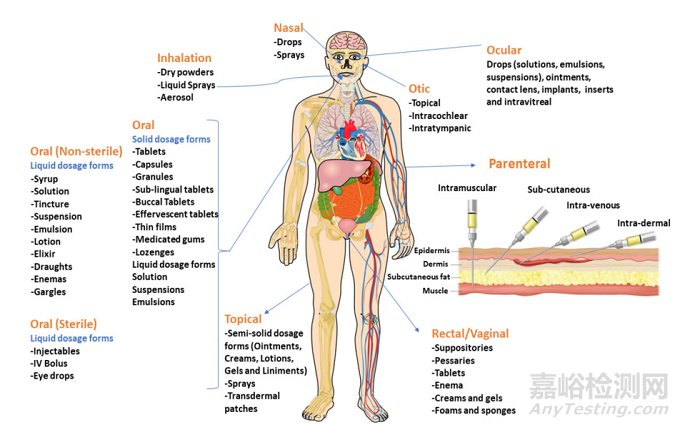
图3 多种给药途径
03药代动力学
药代动力学就是药物在体内的转运过程,此过程一般包括药物吸收、分布、代谢以及排泄。简单的说,此过程就是身体对药物的作用。药代动力学示一般过程如下图所示。
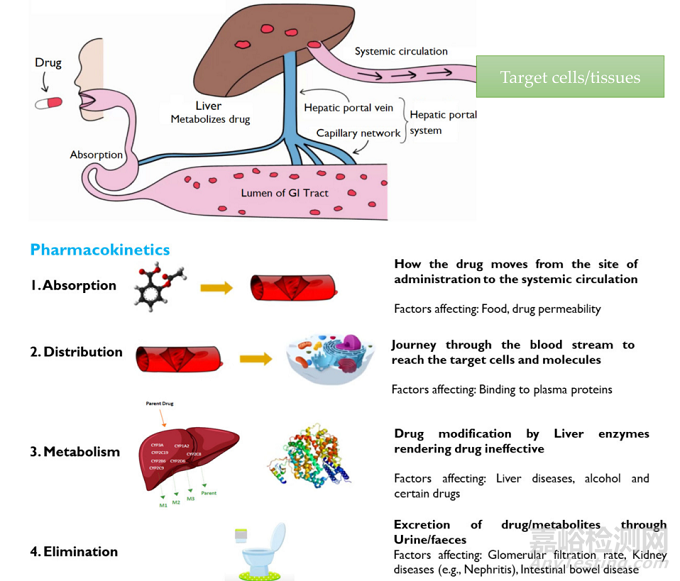
图4 药物药代动力学过程
(1)吸收
吸收是药物从给药部位到血液的过程。药物吸收的速率和程度取决于几个因素,例如给药途径、药物的物理化学性质、制剂类型以及药物-食物相互作用等。通过体循环到达目标部位的药物占总量的百分比我们称为生物利用度,一般我们认为药物的静脉内给药为100%的生物利用度,因为该剂型直接给药到血液中。口服剂型由于吸收不完全和肝脏首过效应而导致生物利用度差,肝脏首过效应会在肝脏中代谢药物,使其活性降低或无活性。
转运过程一般分为被动转运以及主动转运。被动转运涉及药物从高药物浓度区域(如胃肠道)穿过细胞膜移动到低药物浓度区域(如血液)。这是一个被动过程,不需要能量,药物扩散速度与浓度梯度成正比。影响被动转运的其他因素包括药物的物理化学性质,如脂溶性、分子大小、电离程度和药物表面积等。主动转运需要能量来促进药物分子逆浓度梯度的转运,这通常发生在小肠等特定部位。
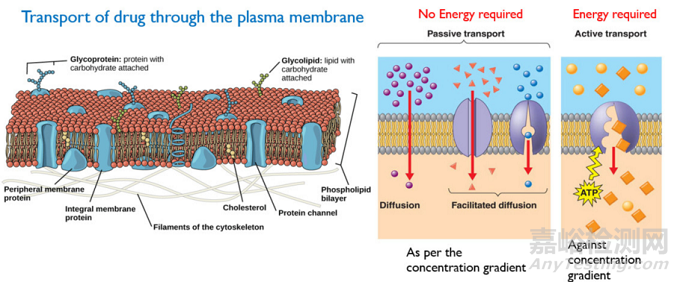
图5 被动转运以及主动转运
(2)分布
分布是药物在血液和身体的其他组织如脂肪、肌肉和脑组织之间的可逆转移。与身体其他部位相比,药物分布决定了药物到达目标部位的量,因此在药物疗效和毒性方面起着重要作用。影响药物分布的各种因素包括血流、药物的亲脂性、分子大小以及药物与血浆蛋白的结合亲和力。此外,在某些器官中存在屏障,如血脑屏障,可防止某些药物进入脑组织。亲脂性高、体积小、分子量低的药物可以穿过血脑屏障。
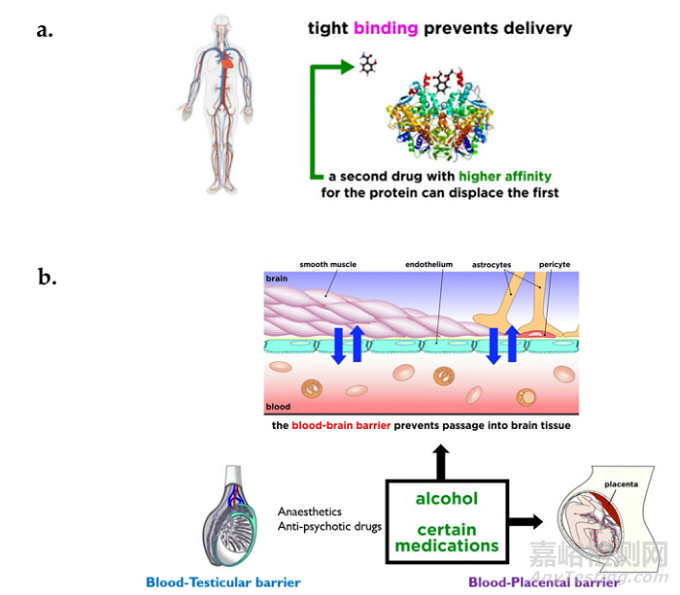
图6 药物分布障碍示意图
(3)代谢
药物在被吸收到体循环之前,会一部分代谢为非活性或活性较低的成分,例如肝肠循环会将一部分药物代谢。药物的浓度,尤其是口服后,在到达血流之前会显著降低。它是药物在吸收过程中丢失的部分,而肝脏的细胞色素CYP450酶对临床使用的约70-80%药物的代谢或生物转化起着重要作用,药物代谢如下图所示。
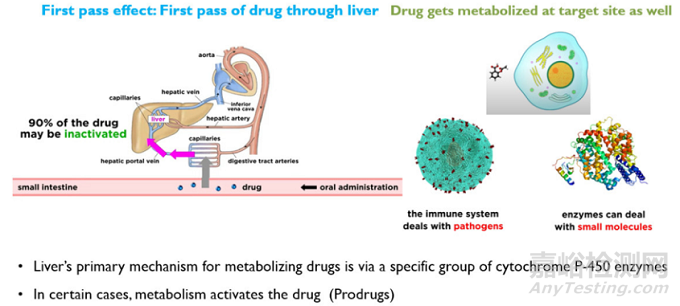
图7肝脏及细胞中药物代谢
(4)排泄
从体内清除未原形药物或其代谢物的过程称为药物排泄。此过程具有许多不同的排泄途径,包括通过尿液、胆汁、汗液、唾液、眼泪、以及粪便等途径。下图为药物排泄的各种模式。
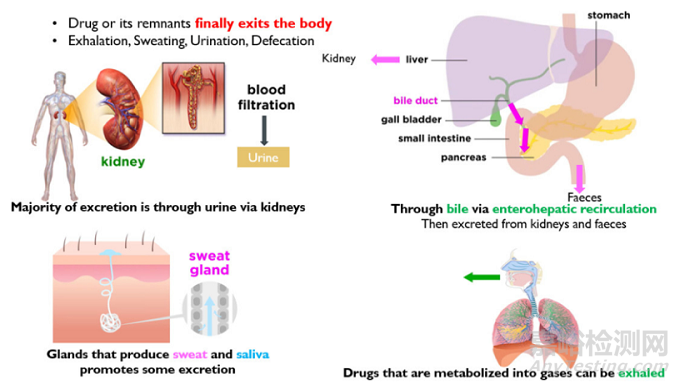
图8 药物排泄方式
(5)生物利用度
前面也提到了,药物的生物利用度就是吸收到体循环中的药物占药物总量的百分比。肝脏代谢高、排泄快的药物一般生物利用度低,对于低生物利用度的药物,则需要高剂量。通过胃肠道吸收的药物首先会通过肝门静脉循环到肝脏。然后肝脏充当过滤器,将部分药物代谢,只有部分药物可以进入体循环。首过效应越大,生物利用度越低。下图为导致药物生物利用度降低的因素。
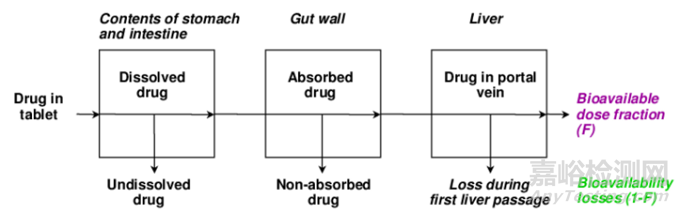
图9 生物利用度降低因素
04传统给药系统及控释给药系统
传统的给药系统如片剂、胶囊剂、糖浆剂等会很快从体内排出,并且剂量不能很好地保持在治疗窗范围内。服用单次常规剂量后,药物代谢非常迅速,血药浓度升高,随后下降,有效时间一般较短。
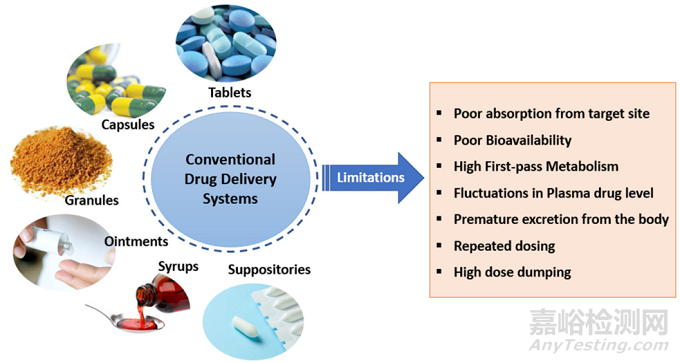
图10 传统给药系统的局限性
因此,为了维持药物浓度高于最低有效浓度且低于毒性浓度,我们需要开发控释给药系统。控释给药系统可以将血药浓度较长时间维持在治疗窗范围内,在较长的时间内提供所需的治疗效果。以下为常规给药系统和控释给药系统的优点和缺点。
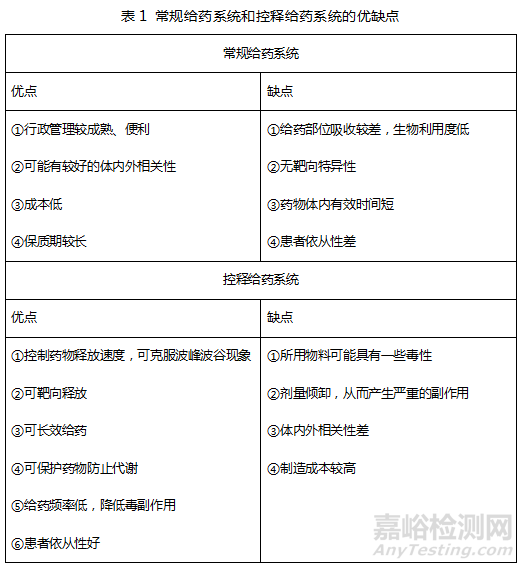
05控释给药系统的PK曲线
控释给药系统中药物的有效浓度在血液和组织中可以稳定保持较长的时间。下图为常规给药系统与控释给药系统的PK曲线对比。常规给药系统的药物血药浓度在最低有效浓度上下波动,而控释给药系统显示零级药代动力学,药物血药浓度水平始终保持在治疗窗口范围内。
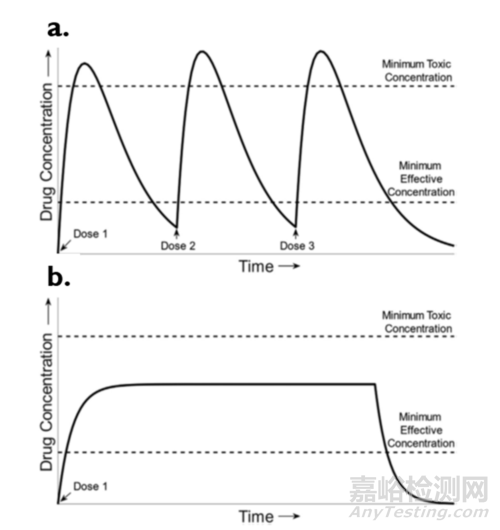
图11 常规与控释给药系统PK曲线
控释给药系统通过在一段时间内释放确定剂量的药物来不断的维持药物的血药浓度。这有助于减少给药剂量和给药频率,并提高患者的依从性。较少的药物暴露量可降低药物毒性和副作用,增强了药物的有效性。以下为控释给药系统的医学原理图。
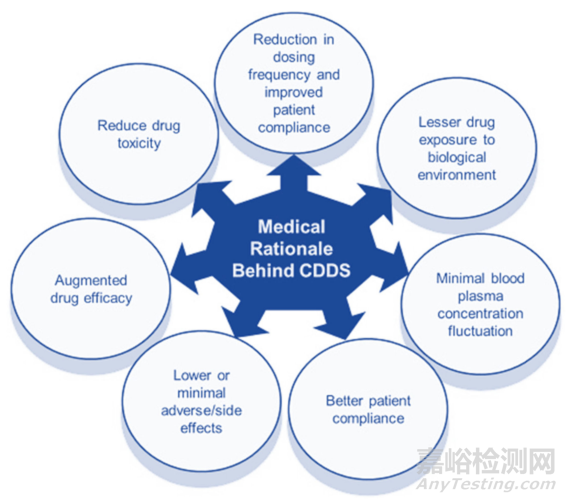
图12 控释给药系统的医学原理图
在设计控释给药系统时,需要考虑各种因素和参数。下图为设计控释给药系统的注意事项,主要与配方及药物相关。处方方面我们应注意生物材料特性、给药途径、药代动力学以及稳定性等方面。此外,药物相关参数如药物与血浆蛋白的结合效率和药物跨越生物屏障的能力、监管方面也是控释给药系统设计的首要考量事项。
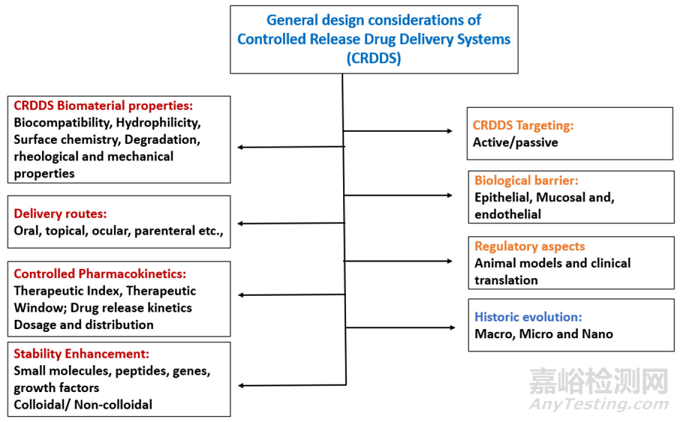
图13 控释给药系统设计的一般考虑因素
06控释给药系统设计的实际考虑
开发控释给药系统的目的就是降低剂量和给药频率,减少药物血浆的波动水平、患者依从性和副作用,以及降低药物的毒性。控释给药系统为了达到所需的药物治疗浓度并在特定时间内维持药物浓度,制剂可由两部分组成,药物的第一部分应该迅速释放,使药物快速达到有效浓度水平,第二部分应该缓慢释放,以维持药物的药理作用。
07聚合物在控释给药系统中的应用
聚合物有助于调节药物的药代动力学,聚合物的选择对制剂的理化性质以及药物的释放起着重要作用。选择的聚合物应该是生物相容的、可生物降解的、无毒的,优选亲水的和粘膜粘附的。以下为在控释给药系统中所使用的一些聚合物。
表2 控释给药系统中所使用的一些聚合物
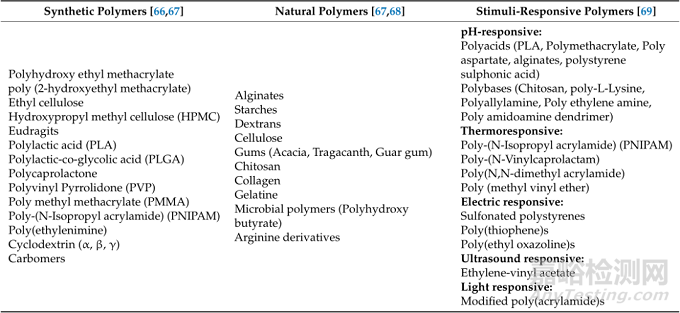
08总结
药物选择合适的剂型的可以一定程度上提高药物的稳定性以及生物利用,也能提高患者的顺应性。所以制剂开发阶段我们应了解我们药物的用途以及理化性质,这样才可以更好的判断选择什么样的剂型。而熟知药物的体内过程,可以帮助我们更好的了解药物,例如药物吸收差怎么解决,药物发生首过效应,都在哪个部位,如何解决或者降低首过效应?这都需要我们对药物在体内的过程所熟知。
控释给药系统可提高生物利用度,延长药物释放时间,并将药物血浆水平维持在治疗窗内,同时将副作用降至最低,其具有传统剂型所没有的优势。新型药物传递系统的研究和开发是当今药剂学研究领域的热点,口服缓控释制剂的开发和应用也日趋成熟。今天的分享就到这里了,小编水平有限,如有不足,欢迎各位同仁批评指正。
参考文献
[1] Garg T , Rath G , Goyal A K . Colloidal drug delivery systems: current status and future directions.[J]. Critical Reviews in Therapeutic Drug Carrier Systems, 2015, 32(2):89.
[2]胡拥军. 药物剂型的选择与合理性评价[J]. 亚太传统医药, 2010, 6(4):4.
[3] Zhang J , Zhang J , Wang R . Gut microbiota modulates drug pharmacokinetics[J]. Drug Metabolism Reviews, 2018, 50:1-12.
[4]刘朋朋, 季金苟. 缓控释制剂给药系统的研究进展[J]. 河北化工, 2007, 30(12):14-17.

来源:药事纵横


