您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-06-29 12:18
药学申报资料M4的3.2.P.2.6中明确要求了相容性的研究内容,在药学研究中相容性直接影响药品的质量和安全。相容性的研究不但包括原辅料的相容性,还包括与包装材料,生产组件及给药器具的相容性。本文以化药注射液为例,阐述在药学研究中不可轻视的相容性研究有哪些,并对相应的研究方法与考察的指标进行了讨论和小结。
举例:某注射液为主成分A和辅料B及注射用水组成的灭菌水溶液,包材为安瓿。本文以A注射液为例,对其药学中的相容性研究的方法及考察指标进行讨论与小结。
一 原辅料的相容性考察
1 研究方法
根据处方中辅料的种类和用量设计相应的相容性研究方法
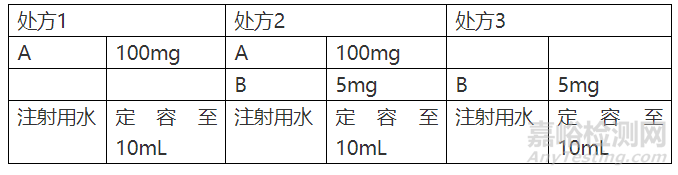
分别将处方1、处方2和处方3的样品放置于60℃和(或)40℃的影响因素稳定性试验箱中,取样时间点为5天,10天和30天。
分别将处方1、处方2和处方3的样品放置于4500±500lx和(或)紫外光下的影响因素稳定性试验箱中,取样时间点为5天,10天和30天。
2考察的指标
2.1 含量
在设计的影响因素取样点取样测定关键指标含量,考察处方2相比于处方1,主药含量是否有超过5%的下降。
2.2 有关物质
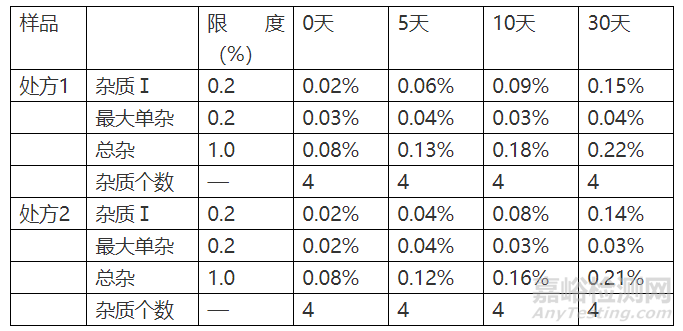
在设计的影响因素取样点取样测定关键指标有关物质,在扣除处方3的色谱峰后,考察处方2相比于处方1,杂质个数是否增加,杂质水平是否有明显的增加。
3 实验结果
3.1 含量结果
3.1.1 影响因素60℃
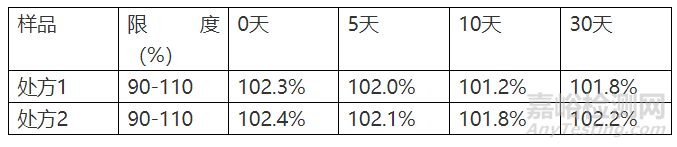
3.1.2影响因素光照4500±500lx
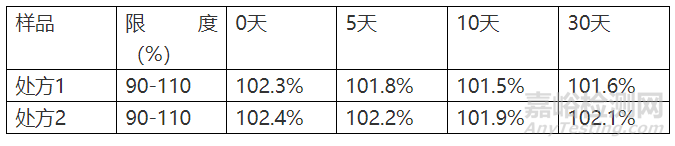
3.2 有关物质
3.2.1 影响因素60℃
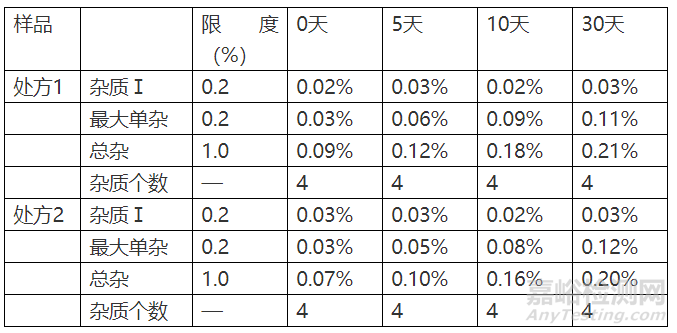
3.2.2 影响因素光照4500±500lx
4 结论
通过影响因素高温和光照的设计考察原料与辅料相容性,结果相容性良好,可以排除因为原辅料不相容造成的药物杂质增加。
二 工艺中相容性考察
1 研究方法
根据工艺流程,注射液一般涉及过滤,所以在相容性的考察方法设计可按下表考察:

2 考察的指标
2.1 性状
观察溶液的颜色和状态是否有明显的变化。
2.2 有关物质
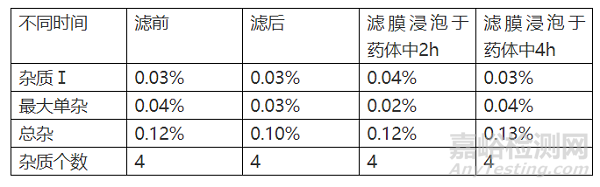
考察过滤后,不同时间过滤后,超滤后,不同时间超滤后较过滤和超滤前的杂质个数是否增加,杂质水平是否有明显的增加。
3 实验结果
3.1 性状
3.1.1 滤膜相容性

3.1.1 超滤柱相容性

3.2 有关物质
3.2.1 滤膜相容性
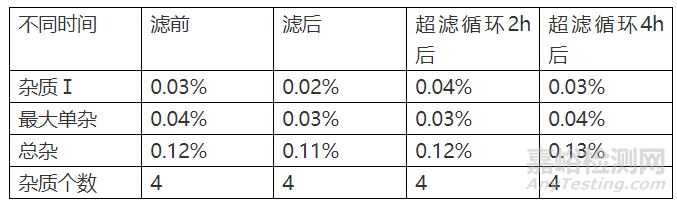
3.2.2 超滤柱相容性
4 结论
考察过滤后,不同时间过滤后,超滤后,不同时间超滤后较过滤和超滤前的杂质个数是否增加,杂质水平是否有明显的增加,药液的性状变化能对工艺中的过滤和超滤组件与药液的相容性进行有效的考量。
三 包装材料相容性考察
1 研究方法
在包装材料相容性的研究中需要结合产品的包装材料的信息,产品特性及工艺综合设计研究方法。
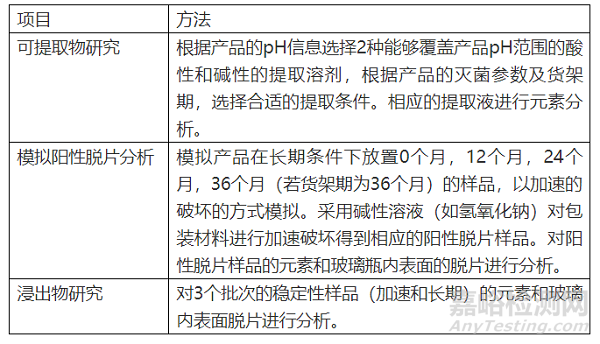
2 考察的指标
可提取物考察的指标:根据毒理学阈值评估,ICHQ3D的元素,产品需要关注的元素进行相应的方法学研究。元素方法学验证的项目包括:专属性、线性、定量限、准确度、精密度(重复性、中间精密度)、溶液稳定性。
模拟阳性脱片考察的指标:元素和内表面的脱片。
浸出物考察:用验证的元素的方法考察测试的结果,定量限,控制阈值及限值。
3 实验结果
3.1 元素方法学验证
对浸出物中的元素如Si、Pb、Co、Cd、As、Sb等进行属性、线性、定量限、准确度、精密度(重复性、中间精密度)、溶液稳定性,各项结果符合验证要求。
测定0天,加速3、6月,长期3、6月的样品的待测元素均在限度以下,无元素增长。
3.2 阳性脱片分析
应用SEM测定0天,加速3、6月,长期3、6月的样品的内表面,安瓿玻璃内表面的平整程度一致,没有玻璃侵蚀风险。
4 结论
通过元素和阳性脱片的分析,可以充分证明包装材料与药液的相容性,避免因为玻璃脱片造成元素显著增长,给注射液的质量造成影响。
四 生产组件相容性考察
1 研究方法
结合工艺组件,产品的特性和工艺过程综合设计研究方法。

2 考察的指标
可提取物研究考察的指标:根据毒理学评估,需要关注的元素,有机物和特殊化合物进行考察。素方法学验证的项目包括:专属性、线性、定量限、准确度、精密度(重复性、中间精密度)、溶液稳定性。根据毒理学阈值评估,有机物进行相应的方法学研究。有机物方法学验证的项目包括:专属性、线性、定量限、准确度、精密度(重复性、中间精密度)、溶液稳定性和耐用性。
模拟生产过程考察:用验证的元素和有机物的方法考察模拟生产样品溶液的测定。
3 实验结果
3.1 方法学验证
对浸出的元素和有机物进行相应的方法学验证,均符合验证的要求。
3.2 测定结果
测定的样品中待测元素和有机物均在限度以下。
4 结论
以组件提取和模拟生产样品测定的结果可以充分证明生产组件与药液的良好相容性。
五 给药器具相容性考察
1 研究方法
结合产品给药器具、产品的特性和工艺综合设计研究方法。

2 考察的指标
可提取物考察的指标:根据毒理学阈值评估,ICHQ3D的元素,产品需要关注的元素进行相应的方法学研究。元素方法学验证的项目包括:专属性、线性、定量限、准确度、精密度(重复性、中间精密度)、溶液稳定性。根据毒理学阈值评估,有机物进行相应的方法学研究。有机物方法学验证的项目包括:专属性、线性、定量限、准确度、精密度(重复性、中间精密度)、溶液稳定性和耐用性。
模拟临床的考察指标:用验证的元素和有机物的方法考察模拟临床样品溶液的测定。
3 实验结果
3.1 方法学验证
对浸出的元素和有机物进行相应的方法学验证,均符合验证的要求。
3.2 测定结果
测定的样品中待测元素和有机物均在限度以下。
4 结论
以给药器具提取和模拟临床给药后样品测定的结果可以充分证明给药器具与药液的良好相容性。
小结:
随着CDE相应的相容性指导原则的发布,在药品注册的药学研究中相容性不能轻视,相容性的研究直接影响药品的质量可控性和安全性,从质量可控性的维度出发,相容性研究包括原辅料的相容性,生产工艺中的相容性。从安全性的维度出发,相容性的研究包括包装材料,生产组件和给药器具的相容性。相容性的研究不但可以保障药品的质量和安全,还可以为药品的包装材料的选择,临床给药器具的选择等提供参考,保证药品的全生命周期中的安全性和质量可控性。

来源:Internet


