您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-08-29 13:04
作为从蚕茧中提取的天然聚合物,丝素蛋白(SF)由于其显着的力学性能、可控的生物降解、和生物相容性,显示出作为生物医学材料的巨大应用潜力。SF具有三种晶体结构,其中最稳定的是反平行β-折叠结构。β-折叠作为网络的物理交联点,在SF水凝胶的形成中起关键作用。然而,由外部诱导的β-折叠交联的SF水溶液的凝胶化通常需要很长的时间,并且需要相对严格的条件,这限制了它们的生物医学应用可能性。
天津大学的刘文广教授团队提出了一种简单直接的策略,通过食品和药物管理局批准的一种生物相容性好的氨基酸表面活性剂——乙基月桂酰精氨酸盐酸盐(LAE)诱导SF的超快速凝胶化。在60°C下,凝胶化时间短至15秒;在体温附近也在1分钟内凝胶。揭示了SF超快速凝胶化的独特途径和热力学,说明了β-折叠超快速的完全去折叠、异相成核结晶和更快速的形成对SF的超快速组装的重要性。并首次利用LAE诱导的原位超快速凝胶化机制制备了可注射的抗菌生物降解止血水凝胶,用于治疗不可压迫性肝出血。该工作以题为“Amino Acid Surfactant-Induced Superfast Gelation of Silk Fibroin for Treating Noncompressible Hemorrhage”发表在《Advanced Functional Materials》上。
【SF-LAE水凝胶的合成与表征】
选择了LAE、月桂酰谷氨酸钠(SLG)、十二烷基硫酸钠(SDS)和水合胆酸钠(SC)四种表面活性剂进行比较,凝胶时间呈现出温度、表面活性剂浓度和SF浓度依赖性的变化趋势,并且凝胶时间随着温度的升高以及SF和表面活性剂浓度的升高而减小。与其他表面活性剂相比,LAE可以以更快的速度诱导SF凝胶化,并且凝胶化时间在体温附近减少到小于1分钟。

图1:SF-LAE水凝胶和海绵的合成路线及止血应用示意图

图2:SF的凝胶化过程研究
【LAE诱导的超快凝胶化机制】
较高浓度的SF和表面活性剂可以促进β-折叠的快速形成,更多地诱导β-折叠作为物理交联剂形成致密的水凝胶网络。几种表面活性剂都诱导了β-折叠的形成,其中SF-LAE水凝胶表现出最强的β-折叠特征峰。且LAE有助于在溶液内形成大量富含β-折叠的成核。通过高灵敏度检测痕量β-折叠的形成,观察到LAE系统中显着的下降,这可以用SF的超快和完全展开来解释。对比均相成核的常规路径,这种完全展开状态可以降低能垒导致多步成核路径。
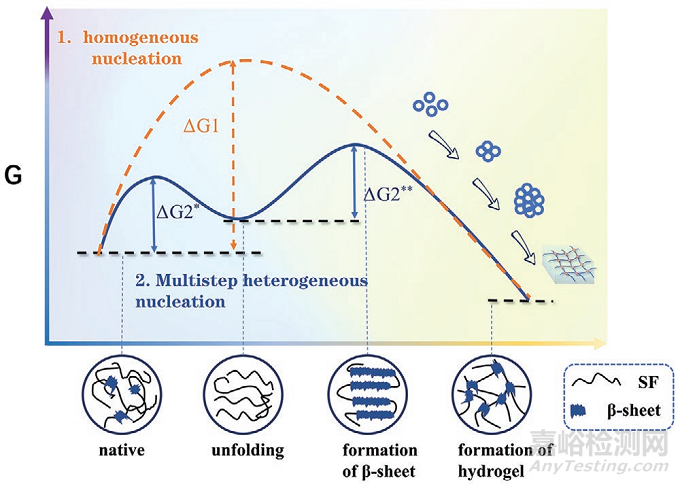
图3:丝素蛋白超快凝胶化的途径和热力学示意图
【SF-LAE-H水凝胶的止血应用】
选择20 wt.% SF和15 wt.% LAE的水凝胶(SF-LAE-H)用于止血实验,实验温度设定为42℃。SF-LAE-H可以很好地适应不规则形状的伤口,且不会在体内重新膨胀以压迫伤口。在大鼠肝穿透损伤模型中评估止血效果。SF-LAE-H前驱体溶液注入伤口后及时凝固,最终实现完全止血。与对照组相比,SF-LAE-H的失血量最少,止血效果最好。止血完成后取出水凝胶没有血液流出,表明水凝胶不仅可以通过物理阻断来止血,还可以刺激内在的止血途径。
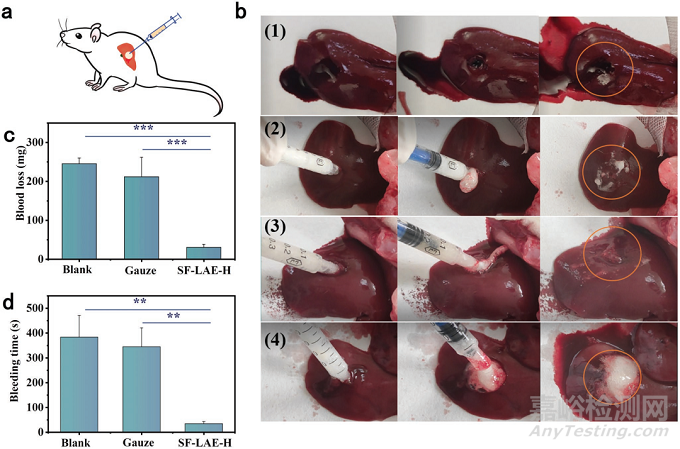
图4:SF-LAE-H的体内止血作用
【SF-LAE-S海绵的合成、表征与应用】
由于SF前驱体溶液和LAE混合过程会产生大量的气泡,将气泡稳定能力与超快凝胶效应相结合,构建了一种不对称多孔海绵,用于治疗不可压迫止血的大出血。由于浮力和重力作用,更多的大气泡向上移动,而较少的小气泡留在水凝胶的下部,从而形成上层松散下层密集的多孔水凝胶。进一步冷冻干燥,得到具有不对称孔的SF-LAE-S海绵。其上部的大孔可以排出血液,下部的密集孔可以防止血液流出以封闭伤口。在兔肝脏穿透损伤模型中评估SF-LAE-S的体内止血性能,SF-LAE-S组的总失血量和失血时间明显低于其他组,表明其作为止血材料的潜力很大。此外,SF-LAE-H与SF-LAE-S都具有出色的抗菌效果和体内可降解性。
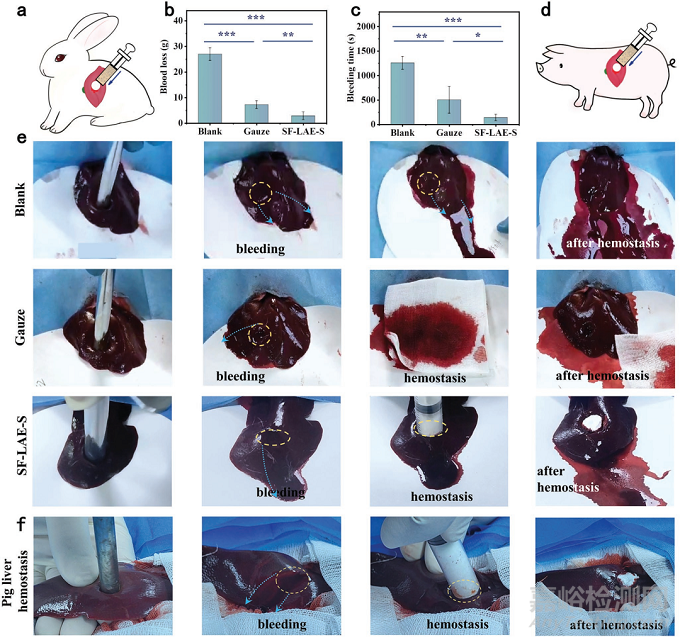
图5:SF-LAE-S的体内止血作用
【小结】
综上所述,该工作证明了氨基酸表面活性剂LAE可以在室温下诱导SF水溶液的超快凝胶化。提出了三个重要因素决定了水溶液中的超快SF组装:首先,由阳离子LAE和SF之间的静电缔合诱导的SF的超快速和完全展开导致更多地转化为新的β-折叠;其次,过量的SF导致异质成核种子;异质成核发生在较低的能垒处,β-折叠聚集加速了水凝胶的形成。这种独特的机制将SF在体温的凝胶化时间缩短到小于1分钟。根据该机制构建了一种可注射的抗菌生物可降解止血水凝胶,用于治疗不可压迫止血的内出血,有望成为一种适用于紧急情况下控制出血的止血剂,且可以用于指导开发用于生物医学应用的新型SF水凝胶。

来源:高分子科学前沿


