您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2022-12-16 19:11
本文适用于采用离子交换色谱法[包括高压液相色谱法或高效液相色谱法(HPLC法)、低压液相色谱法(LPLC法)]对人体血液中HbA1c浓度进行检测的分析仪。
糖化血红蛋白分析仪,按照《医疗器械分类目录》,产品的管理类别为Ⅱ类,产品分类编码为22-10-04。
糖化血红蛋白分析仪(以下简称分析仪)通常由进样模块、分离模块(色谱柱)、检测模块、软件组件等组成。

图1 产品结构组成示意图(例)
一、糖化血红蛋白分析仪组成及功能
1、糖化血红蛋白分析仪组成
1.1 进样模块:通常由吸样针、清洗模块、废液模块等组成。
1.2分离模块:主要由色谱柱(层析柱)组成。经预处理的样品通过分离模块,根据样品与洗脱液以及色谱柱(层析柱)填充剂三者之间亲和程度,来决定HbA1c在内各成分的洗脱顺序。
注:为了确保分离时的温度,也有仪器带有加温部件。
1.3检测模块:主要包括光源(如LED-发光二极管)、光电检测器单元组件等。通过检测从色谱柱(层析柱)分离样本中各组分的吸光度值,并将其转换电信号,最终形成色谱。
1.4软件组件:利用检测到色谱的各峰面积,换算成各成分的浓度,其报告结果包含HbA1c测定值以及色谱图,并一般以常用单位(又称NGSP单位)的%报告糖化血红蛋白测定结果,同时报告国际单位(又称IFCC)的mmol/mol的结果。
1.5应详细写明通过研究确定的关键组件信息,包括质量控制参数等内容。
2.糖化血红蛋白分析仪工作原理
离子交换色谱法[如高压液相色谱法或高效液相色谱法(HPLC法)、低压液相色谱法(LPLC法)]:
通常基于HbA1c与其它血红蛋白组分(HbA1a、HbA1b、HbF、HbA0)所带电荷不同,在一定的缓冲液离子强度下可与色谱柱(层析柱)树脂表面偶联的离子基团不同程度的结合,从而将HbA1c与其它组分区分开而分离,检测从色谱柱(层析柱)洗脱各成分的吸光度,根据每个峰值下的面积计算HbA1c占总Hb的比例,从而获得峰鉴别和含量。
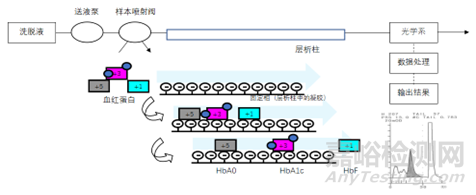
图2 离子交换色谱法工作原理图(例)
二、糖化血红蛋白分析仪性能研究实验要求
同一注册单元内所检验的产品应当能够代表本注册单元内其他产品的安全性和有效性。对同一注册单元内代表产品的选取应考虑产品适用范围、性能指标、安全指标、结构组成等。
1.功能性指标研究
功能性指标研究应包括进样模块、分离模块(色谱柱)、检测模块、软件组件的功能性指标或者模块中主要元器件功能性指标的研究。
产品若包含色谱柱(层析柱),其性能指标除明确配套试剂评估的相关要求外,申请人还应当考虑色谱柱(层析柱)的相关要求,如柱效能、柱压、柱温等。
2.安全性指标的验证包括电气安全指标和电磁兼容指标两大类。电气安全指标应当包括GB 4793.1《测量、控制和实验室用电气设备的安全要求第1部分:通用要求》、GB 4793.6《测量、控制和实验室用电气设备的安全要求第6部分:实验室用材料加热设备的特殊要求》(如分离模块包含加热、孵育功能,则适用)、GB 4793.9《测量、控制和实验室用电气设备的安全要求第9部分:实验室用分析和其他目的的自动和半自动设备的特殊要求》、YY 0648《测量、控制和试验室用电气设备的安全要求第2-101部分:体外诊断(IVD)医用设备的专用要求》及其他适用的国家标准和行业标准中的所有指标;电磁兼容指标应当包括GB/T 18268.1《测量控制和实验室用的电设备电磁兼容性要求第一部分:通用要求》和GB/T 18268.26《测量、控制和实验室用的电设备电磁兼容性要求第26部分:特殊要求体外诊断(IVD)医疗设备》及其他适用的国家标准和行业标准中的所有指标。
3.产品有效期和包装研究
产品有效期验证包含易耗、易损、需定期更换或者具有固定使用寿命的主要元器件,确定产品使用期限或者失效期。具体参见《有源医疗器械使用期限注册技术审查指导原则》的相关要求。
包装及包装完整性:在宣称的有效期内以及运输储存条件下,确保包装完整性。
4.软件研究
参照《医疗器械软件注册审查指导原则(2022年修订版)》的相关要求。
4.1应结合医疗器械软件研究资料框架开展相应的研究,软件的安全性级别需结合软件的预期用途、使用场景、核心功能综合判定。

图3 医疗器械软件研究资料框架
4.2软件版本命名规则:明确软件完整版本全部字段的位数、范围、含义,若软件模块(含医用中间件)单独进行版本控制亦需提供其版本命名规则,并明确与软件版本命名规则的关系。软件和软件模块的版本命名规则均需与质量管理体系保持一致。
5.网络安全要求
应结合医疗器械网络安全研究资料框架开展相应的研究。参照《医疗器械网络安全注册审查指导原则(2022年修订版)》的相关要求。

图4 医疗器械网络安全研究资料框架
6.其他安全有效性的研究
6.1应开展分析系统关于性能评估的研究,包括线性、准确度、精密度、特异性等项目,其中特异性研究应当考虑HbA2、HbF以及异常血红蛋白(HbC、HbD、HbE、HbS等)对测定值的影响。
6.2产品如果声称除了可报告糖化血红蛋白(HbA1c)测定结果外,还可报告HbA2和HbF,以及异常血红蛋白(HbC、HbD、HbE、HbS等)的测定结果,应当考虑检测项目关于准确度、精密度等的研究,另外对于HbA2和HbF,还应当考虑检测项目关于线性的研究。
三、糖化血红蛋白分析仪主要风险
产品主要的风险包括能量危害、环境危害、与使用有关的危害、功能失效及老化有关的危害等。初始事件和环境示例见下表。
|
通用类别 |
初始事件和环境示例 |
|
不完整的 要求 |
设计参数的不恰当规范:可触及金属部分、外壳等与带电部分隔离/保护设计缺陷,导致电击危险防护较低,可能对使用者造成电击危害;设备插头的插销从内部电容器接收电荷过高;工作台支撑件强度不足,设备面、角、边粗糙,可能对使用者造成机械损伤;受潮防护能力不足,造成电击危害;运动部件功能失效,造成机械危害;电磁兼容性不符合要求,导致设备自身不能正常工作或干扰其他设备的正常工作;管道漏液、堵塞和设备浸水,导致电击危害。 性能参数不恰当规范:准确性、重复性等不符合要求。 机械模块失效:无法进样、吸样量不准确、传送错误、定位不准确,导致检测结果异常。 与废液处理相关的生物安全性问题。 服务中的要求不恰当规范:说明书未对糖化血红蛋白分析仪的使用方法、设备的维护、保养进行说明。 元器件、附件或组件功能失效:显示故障、打印故障和配件错误,导致设备无法正常工作,安全性能出现隐患。 |
|
制造过程 |
控制程序(包括软件)修改未经验证,导致产品的性能参数不符合要求。 生产过程中关键工序控制点未进行检测,导致部件、整机不合格。 供方的控制不充分:外购件、外协件供方选择不当,外购件、外协件未进行有效进货检验等。 |
|
运输和贮存 |
不适当的包装:产品防护不当导致设备运输过程中损坏。 不恰当的环境条件等:在超出设备规定的贮存环境(温度、湿度、大气压力)要求下,导致设备不能正常工作。 |
|
环境因素 |
物理学的(如热、压力、时间):过冷、过热的环境可能导致设备不能正常工作;未对使用环境的条件进行严格验证,以致使用条件的不适应而导致检查结果不准确。 电磁场(如对电磁干扰的敏感度):抗电磁干扰能力差,特定环境中设备工作不正常;A类设备在B类设备的环境中使用会对公共电网产生影响,干扰公共电网中其他用电设备的正常运行。 不适当的能量供应:设备的供电电压不稳定,导致设备不能正常工作或损坏、检查结果不准确。 |
|
清洁、消毒和灭菌 |
未对冲洗、清洁过程进行确认或确认程序不规范。 使用者未按要求进行冲洗、清洁等。 |
|
处置和废弃 |
没提供信息或提供信息不充分:未提供产品使用后处置或提示不充分等。 |
|
人为因素 |
设计缺陷引发的使用错误等。 ——易混淆的使用说明书 如缺少详细的使用方法、缺少必要的技术参数、缺少必要的警告说明、缺少运输和贮存环境条件的限制;设备在故障状态(如变压器过载、断开保护接地线、设备的元器件出现故障)下运行可产生危险警示不足;使用前未检查设备工作状态;操作说明过于复杂,不易懂;未说明如何正确维护、保养设备/附件。 冲洗、清洁程序不明确或不清晰。 设置或测量参数未标示单位。 样本的生化危害性,人员防护问题。 控制与操作不对应,显示信息与实际状态不对应。 由缺乏技术的/未经培训的人员使用:使用者/操作者未经培训或培训不足,不能正确使用和维护、保养设备。 |
|
失效模式 |
由于老化、磨损和重复使用而导致功能退化/疲劳失效等。 |

来源:嘉峪检测网


