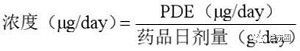由于元素杂质本身不能为患者提供任何的治疗作用,且超过每日允许暴露量(PDE)会产生一定的毒副作用,甚至有些元素杂质在低于毒性阈值的情况下也可能会影响药品的其他质量属性(如对原料药降解有催化作用)。因此,药品研发过程中应尽可能基于质量出发拟定相应的元素杂质控制策略,不建议一概而论。
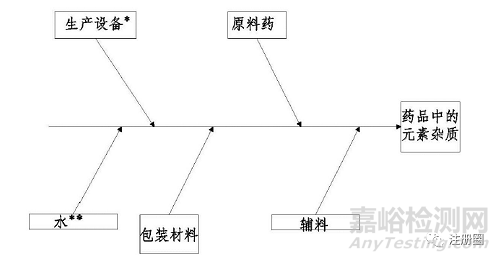
2、元素杂质的来源
①在原料药、辅料或其他药品组分生产中有意添加的元素(如催化剂)的残留。
②非有意添加但在药品生产所用的原料药、水或辅料(物料)中可能存在的元素杂质。
③生产设备可能引入到原料药或制剂中的元素杂质。
④包装系统可能浸出至原料药和制剂中的元素杂质。
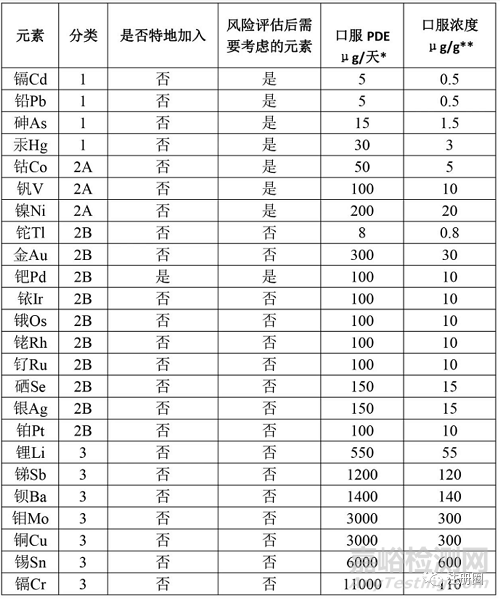
3、元素杂质的分类
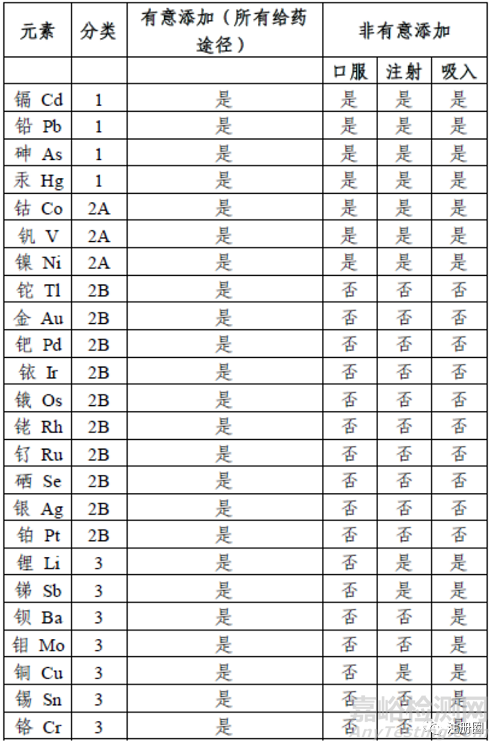
根据元素的毒性(PDE)及其在药品中出现的可能性,分为4类。
1 类:人体毒素,在药品生产中应限制使用或禁用,包括铅(Pb)、砷(As)、汞(Hg)、镉(Cd)。
2 类:给药途径依赖型的人体毒素,根据它们出现在药品中的相对可能性,进一步分为2A和2B两个亚类。2A类元素出现在药品中的相对可能性高,包括钴(Co)、镍(Ni)、钒(V)。2B类元素丰度较低并且与其他物料共生的可能性较低,除非在原料药、辅料或其他药品组分生产中有意添加这些元素,否则无需进行风险评估。包括:银(Ag)、金(Au)、铱(Ir)、锇(Os)、钯(Pd)、铂(Pt)、铑(Rh)、硒(Se)和铊(Tl)。
3 类:此类元素口服给药途径的毒性相对较低(高PDE值,通常>500μg/天),但在吸入和注射给药途径的风险评估中仍需考虑。除非有意添加,否则口服给药途径的风险评估中不需要考虑。包括:钡(Ba)、铬(Cr)、铜(Cu)、锂(Li)、钼(Mo)、锑(Sb)和锡(Sn)。
其他元素:固有毒性低和区域监管差异,PDE值未被确定。如铝(Al)、硼(B)、钙(Ca)、铁(Fe)、钾(k)、镁(Mg)、锰(Mn)、钠(Na)、钨(W)和锌(Zn)。
4、元素杂质限度计算公式
元素杂质限度计算公式一般都是基于下列公式,但是其中PDE的确定需要考虑各种因素。
公式中药品日剂量一般选10g/day或实际制剂的最大日摄入剂量(包括原料药和辅料之和)。PDE确定需要考虑各种因素,如药品中元素可能的氧化价态、可获得的人体暴露量和安全性数据、最相关的动物研究、给药途径、相关终点等。目前,比较常用的PDE计算公式多是基NOAEL/LOAEL进行计算,具体如下:
PDE=NOAEL×50Kg/(F1×F2×F3×F4×F5)
PDE=LOAEL×50Kg/(F1×F2×F3×F4×F5)
NOAEL:未见反应剂量/未见不良反应剂量;
LOAEL:最低可见反应剂量/最低可见不良反应剂量。
F1:不同属种间外推的调整因子(人:1;大鼠:5;小鼠:12;犬:2;兔:2.5; 猴:3;其他动物:10);
F2=10;不同个体差异的调整因子;
F3:短期暴露毒性研究的调整因子(10:较短期的研究;5:啮齿类3个月或非啮齿类2年研究;2:啮齿类6个月或非啮齿类3.5年研究;1:啮齿类或兔1年,猫、犬和猴为7年的研究或用于涵盖全部器官形成期的生殖研究)
F4:严重毒性的调整因子(1:与母体毒性相关的胎儿毒性;5:与母体毒性无关的胎儿毒性或与母体毒性相关的致畸作用;10:与母体毒性无关的致畸作用)
F5:NOEL未建立时的调整因子。
在特定情况下,元素杂质水平可以高于既定PDE值,如间隔给药、短期给药(如:30 天或更短)、 特殊适应症(如:危及生命的、未满足的医疗需求、罕见病)等。这种情况,推荐采用次因子法提高元素杂质限度水平,即将调整因子F2细分为两个次因子,一个代表毒动学(TK), 一个代表毒效学,具体详见ICH-Q3D。
5、元素杂质风险评估
5.1 潜在元素杂质的识别
①由有意添加的催化剂和无机试剂引入的潜在元素杂质。
②可能存在于原料药或辅料(物料)中的潜在元素杂质,如口服给药可能存在1类和2A类,对于注射和吸入给药途径,需评估1类、2A类和3类元素。
③由生产设备引入的潜在元素杂质。此来源元素杂质的贡献有限,工艺知识的应用、设备选择、设备认证及GMP控制都能保证来自生产设备的元素杂质的贡献较低。
④包装系统中浸出的元素杂质。元素被浸出进入固体制剂的可能性极小,无需在风险评估中进一步考察。液体和半固体制剂在有效期内元素杂质从包装系统中浸出的可能性高,应对包装系统的潜在浸出物进行研究。
⑤在生产过程中使用纯化水或注射用水,纯化水或注射用水符合药典标准,可降低水引入元素杂质的风险。
5.2 风险评估中考虑的元素
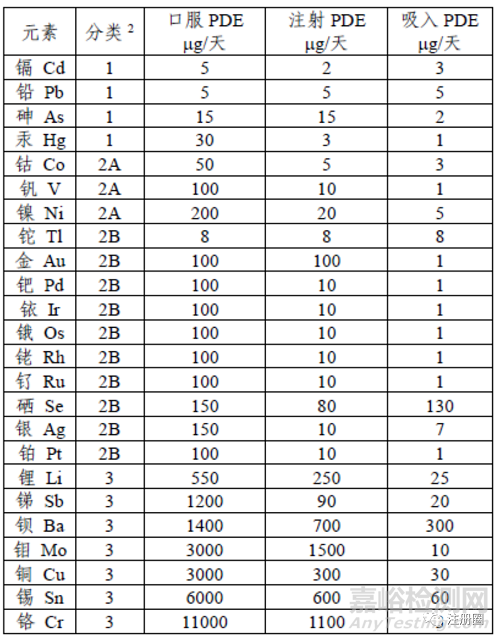
5.3 元素杂质的每日允许暴露量
5.4 评估
①风险评估过程未识别出任何潜在的元素杂质,应记录风险评估结论和支持性信息及数据。
②风险评估过程中识别出一个或多个潜在的元素杂质,对于该过程中识别出的任何元素杂质,风险评估均需考虑元素杂质来源多样性,并记录评估结论和支持性信息。
风险评估数据来源:先验知识、公开发表的文献、相似工艺数据、供应商信息或数据、在后续工艺过程中清除元素杂质的有效性、元素的天然丰度、制剂组分的检验、制剂的检验等。
5.5 风险评估过程总结
将药品中元素杂质PDE值的30%定义为控制阈值,并作为实测元素杂质水平显著性的衡量指标;控制阈值可用于评估该杂质是否需要额外控制,可通过提供3批代表性生产规模或6批代表性中试规模的组分或药品的数据来建立要元素杂质水平和变异性。
5.5.1 元素杂质的测定方法及方法学内容
测定方法有:石墨炉原子吸收光谱法、火焰原子吸收光谱法、电感耦合等离子体质谱法(ICP-MS)等。
方法学内容:专属性、检测线和定量限、线性、重复性和回收率。
5.5.2 元素杂质的控制
当元素杂质超过控制阈值时,需要采取额外的措施来确保元素杂质水平不超过PDE值,包括以下措施:
①调整生产工艺步骤,通过特定或非特定的纯化步骤将元素杂质降低至控制阈值之下。
②建立辅料或物料(如合成中间体)的标准限度。
③建立原料药的标准限度。
④建立制剂的标准限度。
⑤选择合适的包装系统。
⑥对元素杂质进行定期检测。
6、某原料药元素杂质评估示例
6.1 潜在元素杂质的识别
①除催化剂钯炭外,其余物料均不含刻意添加的元素杂质。因此催化剂钯炭中的钯残留应重点考虑;
②化学反应过程和后续处理过程均不涉及激烈的反应和强腐蚀性或者极端环境(高温高压等),溶剂和试剂以及反应液难以对设备和管道造成侵蚀,不会产生元素杂质污染产品;
③工艺中用到大量的饮用水可能还有一定的铁,中和用碳酸氢钠中的钠,会在大量水清洗和溶剂溶解后离心清洗中去除,特别是粗品和精制品制备时不使用水,仅采用甲醇和二氯甲烷作为结晶溶剂,铁、钠等元素杂质存在的几率极低,同时铁和钠作为其他类元素,毒性相对较低不用进一步考虑。
④生产工艺过程中与物料接触的部件材质主要为304型号不锈钢,304型号不锈钢所含成分为铁、镍、锰和铬,它们在工艺过程中和GMP条件下,特别是常规反应对直接接触部分影响小,同时因两步精制仅使用溶剂甲醇和二氯甲烷结晶。不锈钢中的四种元素进入产品可能性很低,而且铁、锰属于其他元素类,铬属于3类元素,因这三种元素的毒性较低可以不做进一步筛查,但镍作为2A类元素丰度稍高需要进一步测试评估。
6.2生产设备评估
原料药A生产过程中使用到的设备和器具,并列出了这些材质中可能存在的元素杂质见表:
|
设备名称 |
设备材质 |
涉及步骤 |
可能存在的元素 |
|
***反应罐/反应釜 |
搪玻璃 |
*** |
铁/铝/铜 |
|
***离心机 |
304不锈钢 |
*** |
铁/镍/锰/铬 |
|
离心滤布 |
粗涤纶 |
*** |
无 |
|
离心滤布 |
纺稠 |
*** |
无 |
|
热风循环烘箱、真空干燥箱 |
304不锈钢 |
*** |
铁/镍/锰/铬 |
|
活性炭过滤器 |
304不锈钢 |
|
铁/镍/锰/铬 |
|
钛棒过滤器 |
304不锈钢 |
|
铁/镍/锰/铬/钛 |
|
连接管道 |
碳钢 |
*** |
铁/碳/硅/锰/硫 |
|
连接管道 |
304不锈钢 |
*** |
铁/镍/锰/铬 |
|
连接管道 |
PVC |
*** |
无 |
从设备材质和生产工艺以及GMP管理结合来考虑,设备设施和管道以及工具等与物料直接接触的部分很难进入物料并传递到成品中,即便有极微量的元素进入也会被后续工序去除。同时,根据ICH Q3D,铁、锰、铝、钛、硅、硫属于其他元素类,铬和铜属于3类元素,因这八种元素的毒性较低且没有在生产过程中特地加入,可以不做进一步筛查。因极微量的铅、镉、砷和汞广泛存在有人体毒性,属于1类元素杂质,而镍属于2A类元素杂质,故铅、镉、汞、砷和镍需要进一步进行筛查。
6.3 生产物料评估
对所有原辅料供应商的物料进行元素杂质的问卷调查,调查结果结合质量标准和元素测试情况进行了汇总,结果见下表:
|
物料 |
生产商 |
用途 |
可能含有的元素杂质 |
|
起始原料 |
*** |
起始物料 |
钠镁钾 |
|
冰醋酸 |
*** |
反应试剂 |
铅、砷 |
|
醋酐 |
*** |
反应试剂 |
铁 |
|
甲醇 |
*** |
反应试剂 |
无 |
|
盐酸 |
*** |
反应试剂 |
铁、砷 |
|
钯碳 |
*** |
反应催化剂 |
钯、铁、铅、铜 |
|
饮用水 |
***自来水公司 |
反应试剂 |
砷、铬、汞、铅、镉、铝、铁、锰、铜、锌、硒 |
|
碳酸氢钠 |
*** |
反应中和 |
铁、钙、砷 |
|
活性炭 |
*** |
脱色 |
铁、铅 |
|
无水乙醇 |
*** |
反应试剂 |
铅 |
起始原料生产中使用了含镁的格氏试剂做催化剂,但是格氏反应后经过后续多个步骤的处理,如水解反应,洗涤,精制等等,因此残留的镁有限。生产过程中使用了碳酸氢钠和碳酸钾,此类无机物均溶于水,很容易在后续一系列的处理过程中去除。同时,镁、钠、钾作为其他元素毒性较低。因此,仅对起始原料中砷铬汞铅等1类元素需要考虑。
冰醋酸的供应商在生产过程中没有增加额外的元素处理,符合国标“GB1886.10-2015食品添加剂 冰乙酸”的要求,其中砷和重金属以铅计的限度分别为1ppm和2ppm,实际测定值低于限度。每生产1批原料药A(约100kg),需要消耗醋酸约53kg。砷和铅作为I类元素需要进行考虑。
醋酐的供应商在生产过程中没有增加额外的元素处理,符合国标“GB10668-2000 工业醋酐”的要求,其中仅元素铁的限度为2ppm,实际测定值低于限度。每生产1批原料药A(约100kg),需要消耗醋酐约76kg。铁作为其他类元素,其毒性较低,因此不会造成风险。
甲醇的供应商在生产过程中没有增加额外的元素处理,符合供应商企业标准和“GB338-2011工业用甲醇”的要求,没有控制金属元素的指标。考虑是精制用溶剂,本公司制定了远严格于国标的内控质量标准,经测试符合内控标准。每生产1批原料药A(约100kg),需要消耗甲醇约1400kg,仅做为溶剂,因此不会造成风险。
盐酸的供应商在生产过程中没有增加额外的元素处理,根据其的出厂检验报告,且符合GB320-93工业用合成盐酸标准,铁和砷有控制,限度分别为2%和1ppm。每生产1批原料药A(约100kg),需要消耗盐酸300kg。铁作为其他类元素毒性较低,而砷作为I类元素需要考虑引入产品风险。
钯炭的供应商在生产过程中没有增加额外的元素处理,但钯原料中包含一定量的铁、铅、铜,其符合供应商企业标准和GB23518-2009标准要求,元素杂质主要是铁/铅/铜,每种杂质要求不得过5%,供应商进行了主成分钯的测试。因铁铜为其他类元素毒性较低,因此需要严格控制钯残留和铅残留问题。
碳酸氢钠的供应商在生产过程中没有增加额外的元素处理,符合供应商企业标准和“GB1606-2008”的要求,其中元素铁的限度为50ppm,钙不得过0.05%,砷不得过1ppm,实际测定值低于限度。每生产1批原料药A(约100kg),需要消耗碳酸氢钠约70kg。铁和钙作为其他类元素毒性较低,而砷作为I类元素需要进一步考虑。
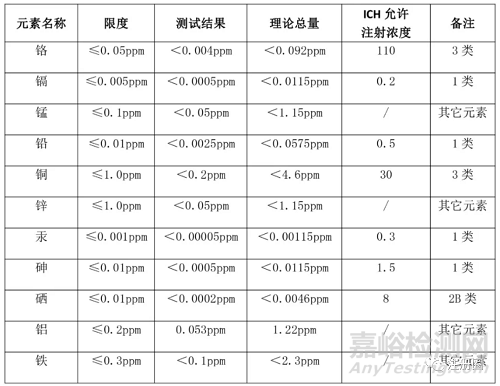
饮用水在产品生产过程中作为水析介质和无机杂质清洗的溶剂。本公司饮用水是由XX市自来水公司统一提供的,本公司按照内控标准每月测试合格,也每年一次委托外部有资质的单位全检,结果符合GB5749-2006,具体数据见下表。
饮用水中元素杂质测试信息表
每生产1批原料药A(约100kg),需要消耗饮用水约2300kg,因饮用水使用量大,本公司根据测试结果计算各元素完全进入成品中的理论含量见上表理论总量。由上述结果可知,即使全部进入原料药中也远远小于ICHQ3D指南可接受标准,事实上经过后续一系列的溶解、分离、精制其基本会得到去除。同时根据ICHQ3D指南铬、锰、铜、锌、硒和铝作为3类或其它元素毒性较低,且含量低不考虑。故饮用水引入需要考虑砷,镉,汞,铅等分布较广元素的残留问题。
活性炭的供应商在生产过程中没有增加额外的元素处理,其放行标准规定重金属限度不得过30ppm;供应商提供的COA上显示控制铁不得过0.05%。每生产1批原料药A(约100kg),需要消耗活性炭1-2kg。铁作为其他类元素毒性较低,因此不会造成风险。
乙醇的供应商在生产过程中没有增加额外的元素去处理,符合国标“GB30610-2014食品添加剂 乙醇”的要求,其中控制重金属以铅计的限度为0.8ppm,实际测定值低于限度。每生产1批原料药A(约100kg),需要消耗乙醇约80kg。铅作为I类元素需要进行考虑。
6.4 环境的评估
本公司生产场地位于XXXX工业园区内,园区内企业以制剂和原料药以及医药中间体生产为主。本公司处于园区的上风口,上风口方向远处均为居民区,上风口和平行方向附近没有粉尘产生,特别是含有元素杂质的粉尘。本产品生产区域的门窗通常处于关闭状态,特别是原料药最终暴露在空气中的工序均是在D级洁净区进行的,且时间相对很短,故从空气中带入元素杂质的风险极低。
6.5 包装材料的评估
原料药A的内包材为双层低密度聚乙烯袋,用塑料扎带密封,外包材为纸板桶。鉴于原料药A是固体原料药,元素杂质从低密度聚乙烯袋迁移到产品中的可能性非常小。因此不需要进行更深入的评估。另外,低密度聚乙烯袋生产厂家在生产过程中,未刻意添加元素杂质。生产商提供的申明明确其确实未添加辅助材料,且符合低密度聚乙烯袋包材标准要求,因此包装材料引入元素杂质的风险也极低。
6.6 风险评估总结
综上所述,从生产工艺、物料、生产设备、生产环境和包装材料五个方面一一评估后,确定了原料药A中需要考察的元素及限度要求,详见下表4。
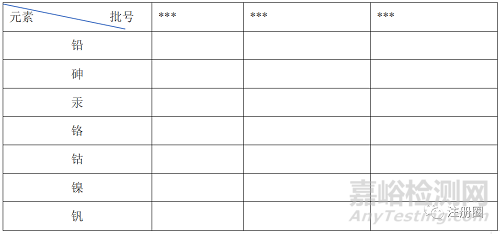
对工艺验证批原料药中的钯残留进行了测试,结果均为<1ppm。对原料药工艺验证连续前3个批次的1类和2A元素杂质进行了测试,3批的测试数据基本一样,具体结果见下表:
本公司经过评估后对原料药A制定了以下控制策略:一是对生产过程中用到的催化剂钯炭的钯残留指标订入原料药A的成品质量标准,限度为不得过10ppm,从而控制成品中钯的残留量,作为产品放行的常规测试指标之一;二对1类元素砷镉汞铅和2A类元素,因其测试结果小于ICHQ3D限度指标的30%,不纳入原料药A的质量标准的常规检测项,但是作为定期评估项目,检测频率为2年/次,每次测试原料药A连续三个批次,测试结果纳入原料药A的年度质量回顾内容并评估。同时,本公司规定至少在以下变更情况,原料药A的元素杂质需要重新评估,如:元素杂质的测试方法改变;钯炭供应商或钯炭浓度发生变化;钯炭催化工序及后续工序的工艺发生变化等等。
参考文献:
[1] ICH-Q3D(R1);
[2] ICH-Q3C(R8);
[3] EP通则5.20. Metal catalyst or metal reagent residues;