您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2023-01-06 11:28
本文适用于电力驱动式的根管预备机。
根据《医疗器械分类目录》,申报产品的管理类别为Ⅱ类,分类编码为17-03-09(口腔科器械-口腔治疗设备-根管治疗设备)。
一、根管预备机工作原理与结构组成
1.根管预备机是一种提供根管预备用器械所需的驱动力,用于根管治疗中,根管预备阶段根管成形和清理的设备。工作原理示意图见图1。

图1工作原理示意图
2.根管预备机通常由主机、马达、手机(如适用)、电源(如适用)、脚踏开关(如适用)和附件(如适用)组成。具体产品结构组成应根据实际产品确定。
2.1按供电方式不同,根管预备机的结构组成通常有3种情况,示例如下:
2.1.1由网电源直接为主机供电。
由主机、马达和马达线缆、手机、脚踏开关组成,如图2。
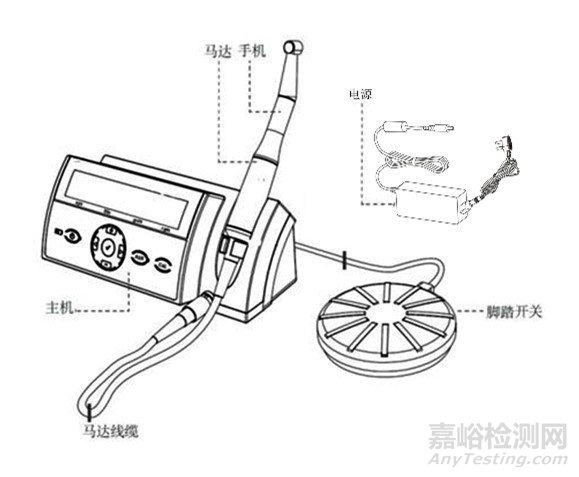
图2
2.1.2由内部电源为主机供电。
由主机(包括马达)、电池、充电器、手机组成,如图3。![]()

图3
2.1.3由牙科综合治疗台给马达供电。
由手机和马达组成,如图4。
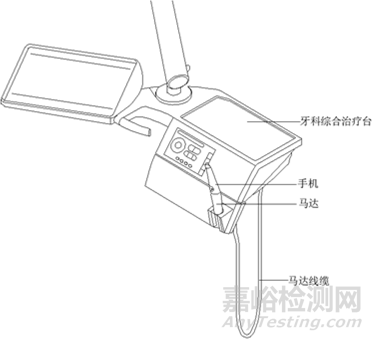
图4
2.2按控制方式不同,根管预备机的结构组成通常有4种情况,示例如下:
2.2.1通过主机控制根管预备机的功能。
由主机、马达和马达线缆、手机、脚踏开关组成,如图2。
2.2.2通过主机(包括马达)上的控制按键直接控制根管预备机的转速。
由主机(包括马达)、手机、电池、充电器组成,如图3。
2.2.3通过牙科综合治疗台控制根管预备机的转速和扭矩等。
由手机和马达组成,如图4。
2.2.4通过安装在移动计算终端上的控制软件控制根管预备机的功能。
由手机、马达、控制软件(如安装在平板电脑上)组成,如图5。

图5
二、根管预备机性能研究实验要求
应当开展产品性能研究以及明确产品技术要求的研究,包括功能性、安全性指标以及与质量控制相关的其他指标的确定,明确所采用的标准或方法、采用的原因及理论基础。
应确定产品技术要求中性能指标,性能指标参照YY/T1602《牙科学根管预备机》中相应条款制定。
1.软件研究
1.1软件
参照《医疗器械软件注册技术审查指导原则》撰写软件描述文档。通常根管预备机的软件安全性级别为B级。
1.2网络安全
若产品具有网络连接功能以实现电子数据交换或远程控制功能,或采用存储媒介(如光盘、U盘等)进行电子数据交换,参照《医疗器械网络安全注册技术审查指导原则》的要求撰写网络安全描述文档。
1.3其他
若采用无创“移动计算终端”实现根管预备机的功能,参照《移动医疗器械注册技术审查指导原则》开展相应研究。
2.生物学特性研究
生物相容性评价研究应当包括:明确生物相容性评价的依据和方法;明确产品所用材料及与人体接触的性质;若实施或豁免生物学试验应明确理由并论证。
如:根管预备机的产品组成中若含有手机,应考虑临床使用中手机机头部分在口内操作,会与口腔内生理组织接触,因此应评价手机机头部分的生物学风险。应明确机头部分的材料,以及在使用过程中与口腔黏膜组织接触的性质和时间,参照GB/T 16886.1《医疗器械生物学评价第1部分:风险管理过程中的评价与试验》要求对手机机头部分进行生物相容性评价。
3.清洁、消毒、灭菌研究
根据产品组成各部分的使用方式确定消毒或灭菌方式。应当明确灭菌/消毒工艺(方法和参数)。对可耐受两次或多次灭菌的产品,应开展相关灭菌方法耐受性的研究。
手机的灭菌要求至少应符合YY 1045.2《牙科手机第2部分直手机和弯手机》的要求,马达的灭菌要求至少应符合YY 0836《牙科手机牙科低压电动马达》的要求。
4.稳定性研究
应明确产品的使用期限,参照《有源医疗器械使用期限注册技术审查指导原则》的相关要求开展产品使用期限的验证。对于可更换/有限次重复使用的医疗器械(如手机、马达等),应单独分析或开展使用次数(如适用)验证。
应开展在使用期限内以及运输储存条件下,保持包装完整性的验证。
5.其他研究
不含有牙根尖定位功能的根管预备机属于免于进行临床评价的医疗器械,申请人应当按照《列入免于进行临床评价医疗器械目录产品对比说明技术指导原则》,从基本原理、结构组成、性能、安全性、适用范围等方面,证明产品的安全有效性。
三、根管预备机主要风险
产品主要危险因素,可预见的事件序列、危害处境和可发生的损害之间的关系详见表1、表2。
表1 产品主要危险因素示例
| 通用类别 | 初始事件和环境示例 |
| 不完整的要求 | 设计参数的不恰当规范:可触及金属部分、外壳、应用部分等与带电部分隔离/保护设计缺陷,电气绝缘强度低,导致对电击危险防护不够,可能对使用者或患者造成电击危害;工作时间过长,与人体接触的部分温度过高,手机散热不良或失效,可能引起操作者和/或患者烫伤;马达、手机和主机间连接不牢固;进液防护能力不足,造成电气危害;运动零件防脱、防裂功能失效,机械伤害自停防护功能缺失或防护功能失效,造成机械危害;脚踏开关产生误动作;主机件固定不紧固造成调节失误;工作时噪声过大干扰医护人员的正常工作;电磁兼容性不符合要求,导致设备基本性能降低或干扰其他设备的正常工作。 |
| 运行参数不恰当规范:转速、扭矩等运行不稳定或与设定值不一致。 | |
| 性能要求不恰当规范:性能参数与实际使用情况不匹配,导致机械损伤。 | |
| 服务中的要求不恰当规范:使用说明书未对根管预备机的维护、保养方式、方法、频次进行说明,如手机的注油保养,导致根管预备机不能正常使用。 | |
| 寿命的结束:超出使用期限,根管预备机/附件的稳定性等性能指标可能会降低,使用时导致根管预备机/附件的安全性能出现隐患。 | |
| 制造过程 | 制造过程更改的控制不充分:控制程序修改未经验证,导致根管预备机性能参数指标不符合标准要求。 |
| 制造过程的控制不充分:生产过程关键工序控制点未进行监测,导致部件或整机不合格 | |
| 供方的控制不充分:外购、外协件供方选择不当,外购、外协件未进行有效进货检验,导致不合格外购、外协件投入生产。 | |
| 运输和贮藏 | 不恰当的包装:产品防护不当导致设备运输过程中损坏;等等。 |
| 不适当的环境条件:未按根管预备机规定的储存环境(温度、湿度、大气压力)储存设备,导致根管预备机不能正常工作。 | |
| 环境因素 | 物理学的(如热、压力、时间):过热/冷环境可能导致根管预备机不能正常工作。 |
| 化学的(如腐蚀、降解、污染):强酸强碱清洗、消毒和灭菌溶液导致根管预备机损害;非预期使用于有麻醉剂的环境中,可能因为电气连接、设备结构、静电预防不良等引起混合气体爆炸。 | |
| 电磁场(如对电磁干扰的敏感度):抗电磁干扰能力差,特定环境设备工作不正常;A类设备在B 类设备的环境中使用会对公共电网产生影响,干扰公共电网中其他用电设备的正常运行。 | |
| 不适当的能量供应:设备的供电电压不稳定,导致根管预备机/附件不能正常工作或损坏。 | |
| 清洁、消毒和灭菌 | 未对清洗、消毒、灭菌过程进行确认或确认程序不规范:使用说明书中推荐的对直接或可能接触患者部件,如手机或相关部件的清洗、消毒、灭菌方法未经确认,不能对相关部件进行有效清洗、消毒、灭菌。 |
| 消毒、灭菌执行不恰当:使用者未按要求对根管预备机或相关部件进行防护或消毒和/或灭菌,导致交叉感染。 | |
| 处置和废弃 | 没提供信息或提供信息不充分:未在使用说明书中对根管预备机的处置和废弃方法进行说明,或信息不充分;未对设备的废弃处置进行提示性说明。 |
| 材料 | 生物相容性:与人体接触的手机部分选择不当可致过敏等反应。 |
| 人为因素 | 设计缺陷引发可能的使用错误。 |
| 易混淆的或缺少使用说明书:如缺少详细的使用方法、缺少必要的技术参数、缺少必要的警告说明、缺少电路图和元器件清单、缺少运输和储存环境条件的限制;设备在故障状态(如自停保护功能、变压器过载、断开保护接地线、设备的元器件出现故障)下运行可产生危险警示不足;使用不适当的根管预备机;使用前未检查设备工作状态;操作说明过于复杂,不易懂;未说明如何正确维护、保养设备/附件。 | |
| 设置、测量或其他信息的显示不明确或不清晰:设置或测量参数未标示单位。 | |
| 错误显示结果:测量结果显示错误。 | |
| 控制与操作不对应,显示信息与实际状态不对应:根管预备机显示的转速范围、扭矩范围与实际的转速范围、扭矩范围不一致。 | |
| 与已有的器械比较,样式或布局有争议:显示参数与多数同类设备通用的显示参数布局不相同,可用性差,可能引起参数设置错误。 | |
| 由缺乏技术的/未经培训的人员使用:使用者/操作者未经培训或培训不足,不能正确使用和维护、保养设备。 | |
| 与消耗品/附件/其他医疗器械的不相容性:未按使用说明书规定使用指定类型和型号的根管预备机,致设备损坏或人员伤亡。 | |
| 失效模式 | 由于老化、磨损和重复使用而导致根管预备机功能退化:手机由于反复消毒和灭菌、使用磨损等原因造成功能退化。 |
表2 部分危险(源)、可预见的事件序列、危害处境
和可发生的损害之间的关系
|
危险(源) |
可预见的事件序列 |
危害处境 |
损 害 |
|
电磁能(电磁干扰) |
(1)可能共同使用的设备(超声洁牙机、根尖定位仪、光固化机等)对根管预备机的电磁干扰,静电放电对根管预备机产生干扰等; (2)根管预备机产生的电磁干扰对可能共同使用的设备的影响等。 |
(1)设备活动部件意外运动;设置参数自行改变; (2)其他同时使用的设备无法正常工作。 |
设备无法正常工作或无法启动。
|
|
漏电流 |
(1)出厂产品质量控制不严,过充、过流和过压保护设计不合格; (2)可触及外壳、应用部分与带电部分隔离/保护不够,漏电流超出允许值。 |
应用部分、外壳漏电流超过标准要求。 |
漏电流超出允许值,患者感觉不舒服,严重时受到电击损伤; |
|
机械力伤害 |
(1)运动部件防脱、防裂功能失效; (2)机械伤害自停防护功能缺失或防护功能失效。 (3)运动部件(底座解锁脚踏开关位置不合理) |
应用部分不受控运动。
|
患者受到机械损伤。 |
|
功能的丧失或损坏(手机、根管预备器械) |
(1)运动部件长期使用的磨损; (2)制造时不合格。 |
防脱、防裂功能失效,根管预备器械飞脱或断裂。 |
患者受到机械损伤。 |
|
操作(脚踏开关、主机误操作) |
(1)未放置在指定位置; (2)误接触脚踏开关或主机功能键。 |
设备意外启动。 |
设备非预期启动,患者受到伤害。 |
|
不完整的使用说明书(附件安装) |
(1)使用说明书未对部件/配件使用作出详细说明; (2)使用说明书未对部件安装作出说明; (3)使用说明书未对部件承载能力作出说明; (4)错误的部件安装说明。 |
部件安装不正确,部件松动,不能正确实现预期的功能、运动部件断裂。 |
延误治疗,运动部件断裂使患者受到伤害。 |
|
细菌感染 |
(1)手机或相关可重复处理使用部件清洗、消毒、灭菌方法不当,有残留细菌; (2)使用者未按要求对手机或相关可重复处理使用部件执行清洗、消毒、灭菌,有残留细菌。 |
患者间有害细菌交叉感染。 |
器官受损、病情加重、死亡。 |

来源:嘉峪检测网


