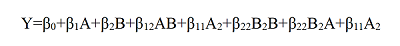2022.05.24 ICH发布了Q14 Analytical Procedure Development 分析方法的开发,以及Q2修订版Q2(R2) Validation of Analytical Procedures 分析方法的验证两份征求意见稿,提出分析方法的开发及验证应遵循AQbD(分析方法质量源于设计)的理念。征求意见稿一经发布便引发了国内各大药企的广泛讨论和关注,如何实现分析方法的QbD,是面临的主要问题,这篇文章是以QbD理念进行方法开发和验证的实例,希望对国内各大药企有所帮助。由于文章较长,现对文章中的主要方法进行陈述。
QbD(quality by design)指质量源于设计,是以预期的和预先确定的方法来实现对结果的预测。与传统或常规的方法相比,更加强调风险评估和管理,遵循分析方法开发源于设计的理念可以使开发出的方法更加耐用,稳健以及明确的设计空间。QbD的一个重要组成部分是了解各因素及各因素间相互作用对于结果的影响。文章中采用中心复合试验设计(CCD),对RP-HPLC方法的两个关键参数——流动相和pH值对头孢曲松钠的保留时间、不对称因子和理论塔板数的影响进行了研究,同时用Design Expert软件对色谱条件进行了优化,建立了相关模型,得到了头孢曲松钠HPLC方法的相对最优解。
那么文章中具体是如何采用QbD理念进行分析方法开发的呢?总的来说可以分成八个部分。下面我们分别来看一下。
一、确定目标产品质量概况(QTPP)
目标产品质量概况(QTPP)对于识别影响QTPP参数的变量起着重要作用。文章中是对头孢曲松钠含量分析方法进行开发,因此头孢曲松钠主峰的保留时间、理论塔板数和峰的不对称因子就是QTPP,而对于有关物质方法开发而言,分离度、灵敏度、主峰纯度等则是QTPP,分析人员应根据实际情况确认目标方法的QTPP,切不可生搬硬套。
二、确定关键质量属性(CQA)
关键质量属性(CQAs)是直接影响QTPP的方法参数。文章中将影响头孢曲松钠含量分析方法QTPP的关键质量属性确定为流动相的组成和缓冲液的pH值。
三、进行析因设计及开展试验
在确定了QTPP和CQAs后,采用中心复合试验设计(CCD)对HPLC方法的流动相和pH值这两个关键参数进行选择和优化。
文章使用Design Expert 软件设计了一个2因素(流动相和pH值)、3个不同水平试验,这是最适合二阶多项式用于二次响应面的设计。
其中,A和B为自变量,Y是每个因素不同组合方式得到的结果(因变量),β0是截距,β1到β22是回归系数,AB、A2和B2分别代表因素间、因素内的相互作用。
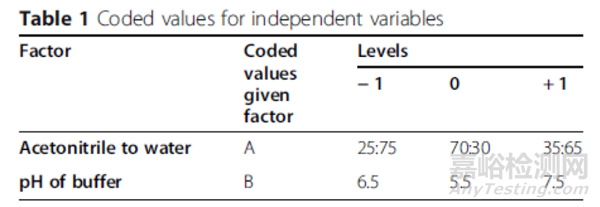
文章根据前期研究数据将流动相的组成和缓冲液的pH值作为自变量(CQAs),详见表1;保留时间、理论塔板数和峰的不对称因子作为因变量(QTPP)。
表1 自变量(CQAs)参数(2因素、3水平)
四、评估试验结果,建立模型,确认设计空间,优化参数
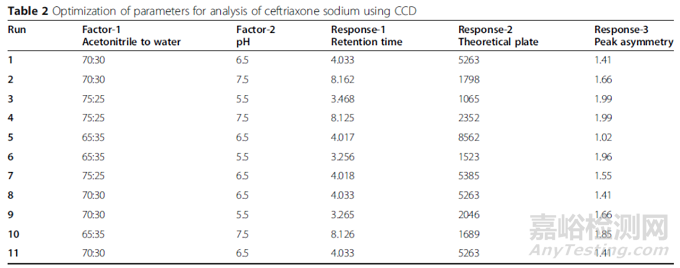
文章采用CCD方法,对试验条件进行评估,并确认方法的耐用性区间,在方法耐用性区间内可以保证不影响产品质量,以免方法验证时失败。如果建模试验没有达到预期目标,则应优化变量的水平,直到达到预期目标。试验结果见表2。
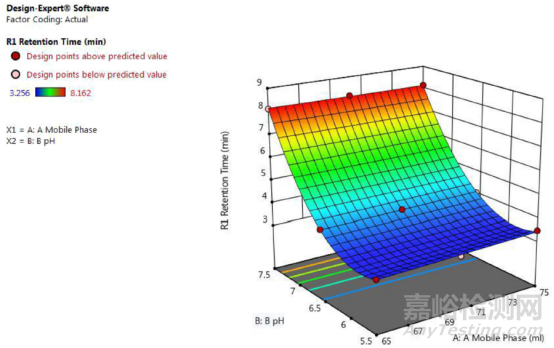
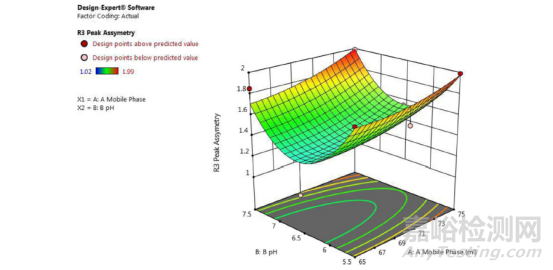
利用Design Expert建模并优化参数。流动相组成、pH值对保留时间的响应曲面见图1,对不对称因子的响应曲面见图2,采用Design Expert进行最优参数的选择见图3。优化后的参数及试验结果见表3。
表2 试验结果表
图1 流动相组成、pH对保留时间的响应曲面
图2流动相组成、pH对保留时间的响应曲面

图3 采用Design Expert进行最优参数的选择
表3 优化后的方法参数及结果
五、进行风险评估
优化的最终方法是根据该方法的关键质量属性来选择的,一个好的方法应当是有效的,可以伴随在产品的整个生命周期内。根据基于风险控制的QbD原则,应当对方法的耐用性、重现性进行研究,研究包括方法的参数、不同实验室、化学品、分析员、仪器、试剂及不同时间等。
文章中考察了3个不同浓度的头孢曲松钠(100、150、200μg/ml)在同一天,间隔2小时,以及三个不同日期进样时峰面积的RSD,结果均小于2%,表明方法在日内及日间精密度良好。
六、实施控制策略
控制策略应在方法开发后实施,应基于对方法不同参数的理解进行设计,包括目的、分析程序及风险控制。所有的参数都应确保方法和产品质量在预期范围内。
七、持续改进,管理分析生命周期
在分析方法生命周期的管理中,最好的方法是进行持续的改进,可以通过监测质量的一致性、HPLC仪器及电脑的周期性维护、软件的升级等方式进行。
八、分析方法的验证
分析方法验证后可以用来确认分析过程适合于其预期的用途。
后记:文章中详细陈述了方法验证的过程及结果,在此不再赘述。自从ICH发布Q14,Q2(R2)征求意见稿以来,分析方法的质量源于设计(AQbD)理念逐渐正式登上舞台,对于药企分析法方法的要求更高,希望本文能抛砖引玉,对国内践行ICH Q14/Q2(R2)有所帮助。
(原文:Patel K Y, Dedania Z R, Dedania R R, et al. QbD approach to HPLC method development and validation of ceftriaxone sodium[J]. Future Journal of Pharmaceutical Sciences, 2021, 7: 1-10.)