权威医学期刊《英国医学杂志》在2021年12月的专辑中分析总结了中国公共卫生政策、非药物干预措施在疫情防控中的作用,其中及早确诊病例并进行隔离治疗是中国非药物干预措施的关键一环,而发现病例需要体外诊断试剂产品。随着新冠疫情发展态势的改变,各国公共卫生政策、新冠体外诊断试剂产品的审批和应用也在演进。本文通过对比几个国家或组织的新冠体外诊断试剂审批流程、审评要求,梳理审评的产品数据差异,分析体外诊断试剂监管与公共卫生应急处置的关系,总结我国抗击新冠疫情的经验,为应急监管体系的持续完善提供参考。
一、新冠体外诊断试剂应急审批流程及审批要求对比
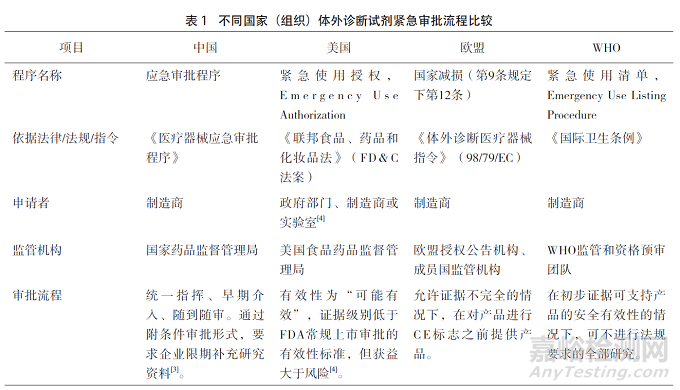
体外诊断试剂紧急审批流程对比。面对新冠疫情这一突发公共卫生事件,各国(组织)均启动对新冠体外诊断试剂的紧急审批程序。参考2020年6月国家药品监督管理局医疗器械技术审评中心发布的比较中美医疗器械应急监管的文章,本文提炼并补充欧盟和WHO相应部分内容,如表1。
新冠体外诊断试剂审评要求对比。新冠体外诊断试剂按技术原理可以分为核酸、抗体、抗原三大类型。鉴于已有文章比对中国、美国及WHO截至2020年4月在新冠核酸检测试剂审评上的差异,且2022年3月11日我国国务院应对新冠疫情联防联控机制综合组决定在核酸检测基础上增加抗原检测作为补充,因此本文选择截至2022年3月24日对抗原体外诊断试剂的质量管理、部分性能指标、临床试验要求三大方面进行简要比对,见表2、表3、表4。



二、差异原因分析
从已获批不同原理体外诊断试剂数量统计来看,美国、WHO、中国主要以核酸诊断试剂产品为主,欧盟则主要选择抗原检测试剂产品。不同类型产品取向与各国的检测产业背景、应用场景对应的数量需求不同有关。大规模核酸检测需要多环节配合,包括采样、运输、实验室建立和运行等步骤。是否使用核酸诊断试剂需要结合当地实验室建设能力、搭建检测体系成本并根据检测需求综合考量。中国和美国人口较多、检测需求大,并且有能力在短时间内改造或新建符合资质的生物实验室用于核酸检测。中国作为世界上最大的体外诊断试剂制造和出口国,使用核酸体外诊断试剂成本较低,由政府大规模集中采购的方式也使政府有一定程度议价权,进一步降低了试剂盒的使用成本。欧盟由于成员国较多国情复杂,许多小国人口较少,搭建核酸检测实验室体系的人均成本较高,选择抗原诊断试剂盒作为主要的体外诊断方式符合实际情况。WHO作为国际组织,有能力搭建完整的检测体系并组织一定规模的集中核酸检测,在审批时也通过了大量核酸诊断试剂盒。
对比各国审评要求,我国对于抗原体外试剂从质量管理要求、性能要求和临床试验要求各方面都较详细且严格。一方面,审评要求的差异与各国本身监管理念、监管传统和行业发展水平有关。而新冠体外试剂由于产品特殊性,审评要求也需要和公共卫生政策达成一致。以诊断灵敏度与特异性为例,只有中国与欧盟提及相关要求且中国对检出率要求较高。原因在于中国采用的公共卫生措施相比于其他国家更严格,检测病例是防控措施的第一环,对于后续步骤有指导作用,使用体外检测试剂出现假阳性/假阴性导致后续的隔离等环节会造成更高的社会成本。主权国家在疫情期间采取的公共卫生措施需要依赖新冠体外检测报告作为个体出入国际、地区间辅助凭证,因此其检测准确度必须在较高水平。
三、讨论与建议
科学防疫精准监督推动防疫措施落到实处。国情和非药物干预措施决定了相关医疗器械的应用场景,从而确立了“应急”的“急”在不同医疗器械上的程度,也对监管要求中性能指标、应用场景提出了具体需求。中国对体外诊断试剂的监管匹配了政府主导“快速遏制”的非药物干预措施,并且随着新变种特点、疫情情况进行演进。中国公共卫生措施中最主要的区别在于是否主动检测病例,这是所有措施中最核心的步骤,也是之后隔离治疗、密切接触者追踪隔离的前提,通过追踪已有病例行程将不同地区通过风险程度进行划分并进行大规模集中的核酸体外诊断;随着新变种成为主要流行毒株,中国增加了抗原检测作为辅助手段,并更新了主动核酸检测的组织方式。主动检测病例和后续对于密切接触者的管控隔离会对社会运作和经济产生负面影响,诊断出现假阳性或假阴性导致的机会成本大大增加,诊断产品的准确性和质量控制十分重要,因此我国主要采用核酸检测且相关质量标准较高。
建章立制健全重大公共卫生事件应对机制。以新冠这一重大卫生公共事件为契机,我国监管部门总结经验,完善相关法律法规,填补创新和紧急情况下体外诊断试剂适用的相关条例,使体外诊断试剂申请审批在紧急情况下有法可依。中国在疫情期间颁布了《体外诊断试剂注册与备案管理办法》,概括来说整个体外诊断试剂的申请流程中强化了质量管理的理念,细化了申请流程。对于医疗器械大类更新了《医疗器械监督管理条例》,强调了创新医疗器械的重要性;放开检测报告;新增“罕见疾病、严重危及生命且尚无有效治疗手段的疾病”和“特别重大突发公共卫生事件或者其他严重威胁公众健康的紧急事件”审批条件;国内尚无同品种产品上市的体外诊断试剂可自行研制使用;在特定情况下,可进口少量第二类、第三类医疗器械等。
完善科学监管体系保障公众知情权。应急情况下时间资源稀缺、产品又需要创新和技术,如何继续提高监管科学性方面我国也可以向发达国家和地区学习,引入多个相关方,拓展应急资源来源和利用效率。比如美国、欧盟和WHO均公开每一项已审批通过的试剂的详细审批信息和各技术指标、临床试验结果,这样有助于社会监督监管流程并学习了解产品信息。我国也有专家提及,作为疫情防控工作的一个环节,公布相关审评信息,以缓解公众恐慌情绪、消除疑惑。