近期首都医科大学宣武医院吉训明教授和北京大学郑玉峰教授在科爱出版社创办的期刊Bioactive Materials上联合发表研究文章:介入导管表面丝素蛋白/硅基微球复合隔热涂层的构建及其在脑靶向低温中的应用研究。创新将生物隔热涂层引入介入导管表面改性领域,利用气压喷涂技术,在导管表面构建生物安全的高孔隙率、强力结合的微米复合隔热涂层,以提高低温灌注液降温效率。
研究内容简介
脑卒中是我国成年人致死、致残的首位病因。血管内靶向低温技术可有效改善脑卒中患者临床预后,是最有效的神经保护方法之一,临床应用前景好。其中,低温导管作为该领域的重要高值耗材,国家临床需求重大。然而临床所用低温导管,多为神经介入导管,不是专为低温灌注治疗设计,导管管壁多为金属网增强复合结构,导热系数与血液相近。导管壁隔热性能差,导致管内低温灌注液与人体产生热交换,降低了低温治疗效率。因此,导管壁隔热性能差成为制约该技术临床转化推广的主要因素。
针对上述瓶颈问题,本研究选取导热系数低、血液相容性与成膜性好的丝素蛋白为成膜材料,以硅基气凝胶颗粒为隔热填料(结构),利用气压喷涂技术,联合多巴胺自聚合与等离子体化学气相沉积技术,在导管表面成功构建丝素蛋白基“界面-隔热-保护”隔热涂层体系。
图1.血管内靶向低温脑保护技术 (A),导管内低温灌注液与导管外血液热交换示(B),气压喷涂设备(C)和“界面IL-隔热TL-保护PL”隔热涂层体系示意图
一、传热模型构建与计算分析
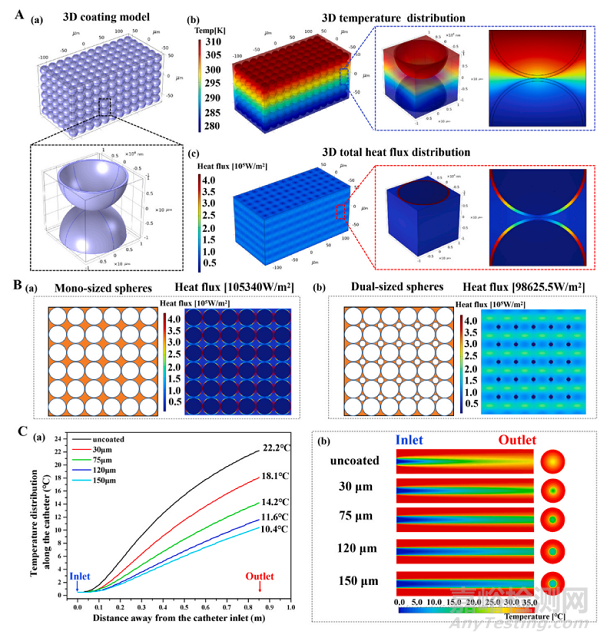
通过传热学基础理论分析,获得最优隔热性能微纳米多孔隔热涂层结构。介入导管在传输低温液体时,热量从导管外常温血液通过热对流和热传导传递至导管壁面,在壁面内部进行热传导和热扩散后传递至导管内低温液体,生物相容隔热涂层可降低管壁有效导热系数,提升热阻,从而降低导管出口灌注液升温幅度。
假设所有的空心微球具有相同的直径和壳体厚度,壳体厚度均匀且表面光滑,按照简单立方体排列,进行空心球体导热系数计算。由于简单立方体排列的对称性且导热系数是材料的固有属性,根据傅里叶传热公式,计算单元的有效导热系数。同等孔隙率下,当空心微球的尺寸在微米以下时,由于气体导热系数受克努森效应的影响显著,微球直径变小,单元有效导热系数会降低;当微球尺寸在微米以上时,克努森效应影响很小,可以认为单元导热系数变化较小。由于二氧化硅在组分中具有最高的导热系数,壳体厚度的增加和接触直径的增加都会导致其传导的热量更多,因而不利于单元有效导热系数的降低。同时通过计算可知, “大小”球堆叠结构的热通量小于单一尺寸球体堆叠结构。
图2 隔热涂层内多孔微球堆叠结构与传热云图(A);单一尺寸与双尺寸微球堆叠结构涂层热通量云图(B);不同涂层厚度下导管出口温度模拟结果(C)
二、涂层制备与隔热性能评估
图3 隔热涂层制备流程图(A);微米空心球与涂层扫描电镜形貌照片(B);与裸导管相比,不同涂层厚度下导管出口温度差值(C);涂层隔热性能示意图(D)
为确保导管涂层在脉动血流中的力学稳定性和隔热效果,建立由界面层、隔热层和保护层组成的丝素蛋白基隔热涂层系统。针对界面层,利用“生物粘合剂”聚多巴胺粘附机理,对导管表面进行多巴胺自聚合预处理,其包含的儿茶酚基团能够与其它物质形成氢键、金属配位化合物或氢醌电荷转移配合物,提高涂层与基底结合力。针对隔热层,气压喷涂技术,采用丝素蛋白/硅基微米空心球制备隔热涂层。针对防护层,利用化学气相沉积技术在涂层外表面制备Parylene-C膜层。其中丝素蛋白是一种从家蚕(Bombyx mori)中提取的天然共聚物,主要由甘氨酸、丙氨酸、丝氨酸和酪氨酸组成,其二级结构包括β-折叠、β-转角、α-螺旋和无规则卷曲结构等。丝素蛋白内氨基酸(丝氨酸/酪氨酸)侧链(-OH/-NH2)可与基底间形成氢键或配位键,在生理环境下具有较强的粘合强度,是理想的成膜材料;对涂层处理诱导形成β-折叠结构,可提高涂层结合力和弹性模量,但降低了其延展性。
三、低温隔热导管体外模拟实验
图4 脑靶向低温体外模拟平台照片(A)和局部照片(B);导管出口温度(C)、大脑中动脉温度(D)、主动脉弓温度(E)、输出制冷功率(F)、灌注体积(G)与血液稀释率(H)
构建符合人体神经介入路径真实血管分布的体外模拟低温测试平台,隔热导管从股动脉介入并放置在颈总动脉处。采用热电偶K型多通道温度测试仪测量模拟血管内和导管的各个温度,具体如下:股动脉处低温模拟血液的入口温度T0,模拟人体核心温度主动脉弓处温度T1,隔热空腔导管的出口温度T2,靶向脑组织处动脉(大脑中动脉,MCA)血管的温度T3。与对照组相比,隔热导管出口温度低,实现了对MCA处更有效的降温。
图5 体外生物相容性分析。HUVEC, HSMC 与 RAW 264.7 细胞荧光染色照片(A)和细胞增殖率(B),以及血液相容性分析(C)
采用间接接触法评估涂层细胞相容性,经过Parylene C涂层修饰后,隔热涂层细胞相容性提高,与阴性对照组相比结果无统计学差异。所制备导管涂层溶血率均显著低于ISO 5%标准。
图6 动物实验装置与流程示意图(A),DSA影像照片(B),导管出口处灌注液温度与同侧耳温(C),颈总动脉切片HE染色(D)与降温速率对比(E)
采用健康猪动物模型验证隔热导管的安全性与降温有效性。试验表明,与临床用导引导管相比,隔热导管(涂层厚度75 μm)出口处温度低1.8~2.0℃。涂层材料与颈动脉血管壁生物相容性好。
本研究将丝素蛋白隔热涂层理念引入血管内介入导管表面改性领域,丰富了丝素蛋白基复合材料微观组织结构与其隔热/力学性能关系的作用机制理论,拓展了天然生物蛋白高分子复合涂层的应用领域。一方面,解决介入导管管壁隔热性能差的问题,推动血管内低温脑保护技术临床转化;另一方面,该涂层构建技术在新生儿缺氧性脑病、心脏骤停患者脑部缺血缺氧以及重度颅脑损伤患者亚低温治疗领域、体外膜肺氧合用导管系统、腹腔热灌注治疗和肝脏介入热化疗等领域均具有潜在应用价值。