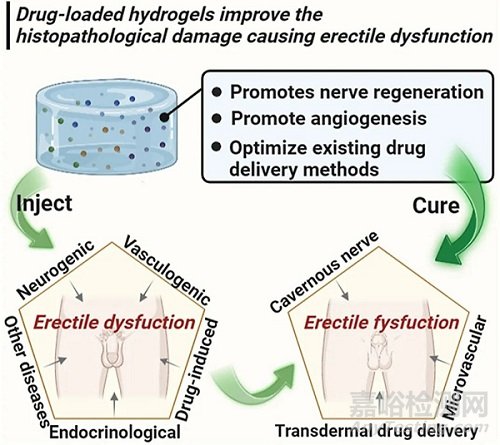
器质性勃起功能障碍(ED)是一种男性性功能障碍,通常与疾病、手术损伤、正常衰老有关,在全球范围内发病率很高。此外,ED与心血管事件风险和心血管事件死亡具有一定相关性。ED作为血管疾病的标志物,通常发生在心血管疾病(CVD)中,比心血管疾病事件提前2-5年。在最新的CVD预防临床指南中,ED被用作评估CVD风险的指标。
阴茎勃起的本质是由多种因素共同调节的神经血管事件。神经和血管损伤是导致勃起功能障碍的主要原因。目前,ED的主要治疗方案包括磷酸二酯酶5型抑制剂(PDE5Is)、体内注射和真空勃起装置(VED),然而这些策略的生物利用度低、全身不良反应高、患者体验差、侵入性强和应用有限。最重要的是,目前的这些疗法很难治愈ED。水凝胶提供了许多优于现有疗法的优势。它们可以由具有不同性能的各种原料合成,并且具有可调控的力学性能。良好的生物相容性和生物降解性也使其成为有效的药物载体。各种载药水凝胶可以促进神经和血管再生,以改善甚至逆转引起ED的组织病理学损伤。
近期,国家纳米科学中心刘颖研究员联合浙江中医药大学刘翠清教授概述了器质性勃起功能障碍的潜在机制,讨论了ED现有治疗方法的困境,并突出了水凝胶相对于其他方法的独特优势,最后重点介绍了水凝胶在ED治疗中的研究进展。该综述以题为“Advanced hydrogels: New expectation for the repair of organic erectile dysfunction”的论文发表在最新一期《Materials Today Bio》上。
男性勃起的生理机制
阴茎勃起的本质是一种由多种因素共同调节的神经血管事件。在性刺激下,海绵体神经(CN)末梢释放神经递质,使供应勃起组织的动脉和小动脉放松,并增加动脉血流量。同时,静脉丛被压迫,静脉流出量减少,导致腔内压力增加,最终实现勃起。
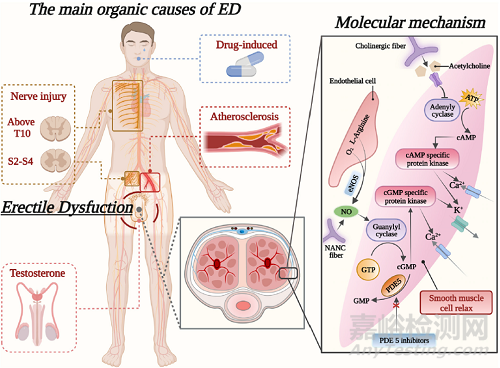
一氧化氮(NO)是该过程中放松平滑肌(SM)的主要神经递质,并参与阴茎勃起(图1)。非肾上腺素能非胆碱能(NANC)神经纤维和内皮细胞在性刺激时释放NO,从而激活鸟苷酸环化酶并提高环鸟苷单磷酸(cGMP)的浓度,80%的ED病例是由NO-cGMP系统功能障碍引起的。乙酰胆碱由副交感胆碱能神经纤维释放,激活腺苷酸环化酶,导致环磷酸腺苷(cAMP)水平升高。cGMP和cAMP都充当细胞内第二信使,激活磷酸化某些蛋白质的特异性蛋白激酶,最终降低细胞内Ca2+水平和SM松弛。当SM放松时,血液充满海绵状空间,对筋膜下小静脉造成压力,并阻断静脉流出。这样,随着动脉血流量的增加和静脉流出的阻断,腔内静脉的压力增加,完成了阴茎从依赖位置到勃起状态的转变。相反,当cGMP被5型磷酸二酯酶(PDE5)水解为一磷酸鸟苷(GMP)时,上述过程被逆转,然后阴茎松弛。因此,这些过程中的任何一种功能障碍都可能导致ED。神经源性或血管源性损伤是ED的主要病理机制。
图1. 器质性勃起功能障碍的主要原因和平滑肌弛豫的分子机制示意图
水凝胶治疗神经源性ED
阴茎平滑肌的凋亡通常发生在CN损伤后,是ED的潜在原因。水凝胶作为一种生物递送载体,在改善海绵状神经损伤、抑制平滑肌细胞凋亡和促进ED恢复方面表现出优异的性能和治疗潜力。
SHH蛋白是阴茎平滑肌及其细胞凋亡的重要调节因子,在正常勃起功能中发挥重要作用。阴茎海绵体含有大量平滑肌、弹性蛋白纤维和少量胶原蛋白。周围神经损伤后,阴茎的平滑肌和弹性纤维减少,胶原蛋白增加。这一不可逆转的过程也是ED发展的基础。在成年阴茎中,当SHH信号被抑制时,SM细胞凋亡显著增加。
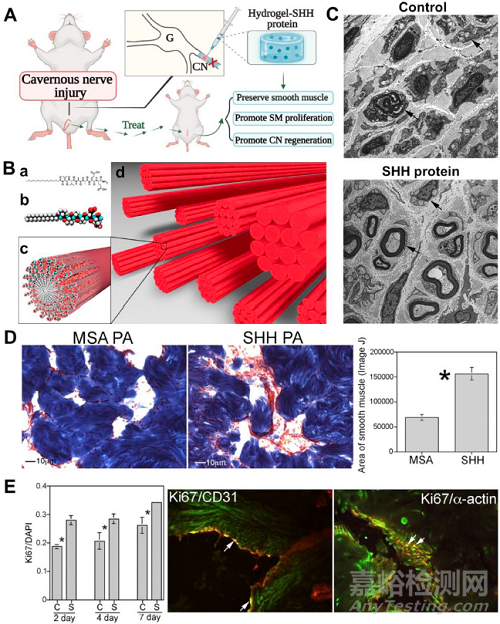
治疗海绵体神经损伤引起的勃起功能障碍可以通过应用水凝胶和SHH蛋白来完成(图2)。为了有效抑制CN损伤引起的细胞凋亡,可以使用基于肽两亲性(PA)的纳米纤维将SHH蛋白递送到阴茎海绵体SM,该纳米纤维可以自组装成水凝胶。实验结果表明,SHH-PA治疗可以有效抑制细胞凋亡,保存阴茎中的平滑肌,并促进其增殖。其他研究也表明,在前列腺切除术后的再生条件下,SHH-PA治疗可以减少胶原蛋白,增强轴突的形成,并使CN再生。
图2. 水凝胶和蛋白质的结合可改善海绵状神经损伤引起的ED。
水凝胶治疗血管性ED
保持正常勃起的先决条件是健康的海绵状组织和完整的海绵窦结构。勃起是海绵体的正常组织功能,也依赖于海绵窦内的微血管系统。水凝胶支架具有机械强度强的多孔结构,在结构和机械上与天然海绵体相匹配。因此,它为细胞生长提供了良好的微环境和空间,有助于海绵窦的修复。
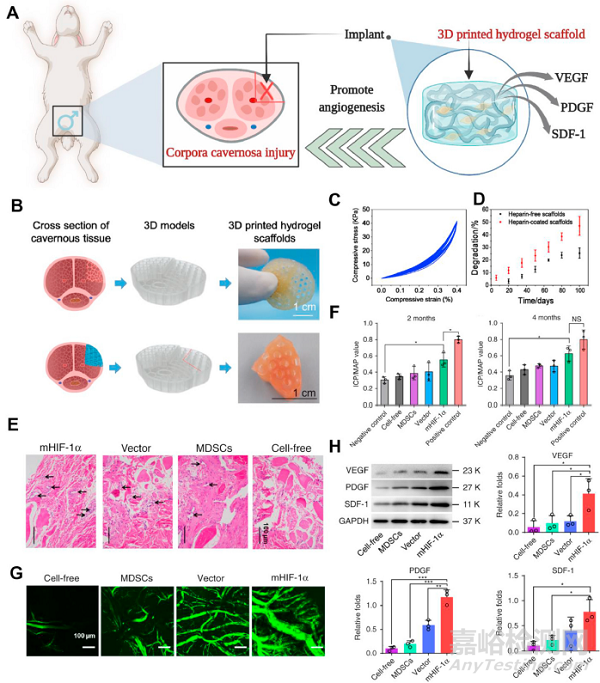
通过构建肝素涂层的3D打印水凝胶支架,植入缺氧诱导因子-1α(HIF-1α)突变的肌肉衍生干细胞(MDSCs),可修复兔子受损的海绵体(图3)。植入的3D打印水凝胶支架不会因阴茎中的结构应力升高而受损,能经受20次压缩试验(应力高达40kPa)(图3C)。水凝胶支架上的肝素可以在支架表面吸附和富集HIF-1α产生的血管生成因子,并刺激体内血管生成。新生血管的增加进一步促进了受伤海绵体勃起功能的恢复。在体外降解实验中,含有和不含有肝素的水凝胶支架都表现出很强的生物降解性(图3D)。这项工作表明,具有血管生成细胞的3D打印水凝胶在阴茎重建以恢复男性生殖能力方面具有广阔前景。
图3. 水凝胶支架修复海绵体损伤并改善ED。
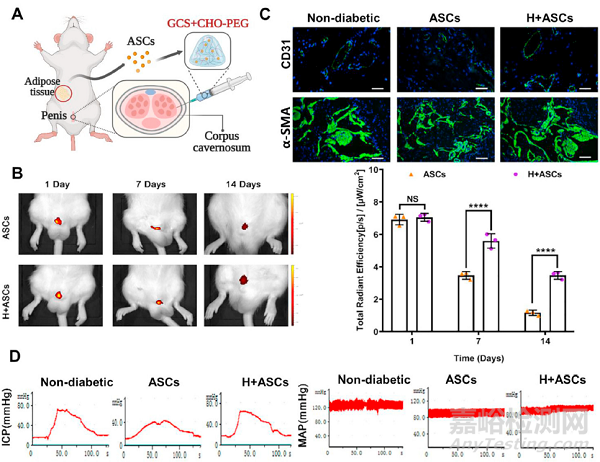
另一种负载脂肪干细胞(ACSs)的苯甲醛封端的聚(乙二醇)/乙二醇壳聚糖(CHO-PEG/GCS)水凝胶具有可注射性和自我修复性,可以延长干细胞在海绵体中的滞留时间(图4A)。它可以与ASCs协同降低cGMP水平,并增强ASCs以改善糖尿病纤维化。实验结果表明,水凝胶有效延长了ASCs在阴茎海绵体中的保留时间(图4B),抑制平滑肌细胞的凋亡(图4C)。因此,在1型糖尿病ED大鼠中,水凝胶和干细胞的共同作用实现了勃起功能的恢复。
图4. 可注射水凝胶可延长干细胞在海绵体中的滞留时间,抑制细胞凋亡,改善勃起功能。
小结
本文综述了用于治疗ED的水凝胶和水凝胶基材料的最新进展,包括改善神经损伤、促进血管生成、减少细胞凋亡、预防平滑肌萎缩和减轻辐射损伤。同时,水凝胶生物材料可以实现药物和生长因子的持续可控释放,具有一定的及时控释潜力。水凝胶有助于优化现有的治疗方法,填补现有治疗方法的空白,促进神经和血管修复,改善甚至逆转ED的组织病理学损伤。水凝胶的使用不仅优化了现有的给药方法,还改善或治愈了一些难治的器质性ED,有望为患者提供更彻底、有效和微创的治疗。
目前,水凝胶和水凝胶基材料在ED治疗中的应用仍然存在许多挑战:1)水凝胶促进有机ED修复的机制仍然相对肤浅,有待进一步改进。2)水凝胶主要用作ED治疗的生物递送载体,而水凝胶材料本身的开发仍需深入。进一步探索可单独应用于改善ED的水凝胶材料,将有助于将研究结果转化为具有更高临床价值的工业化产品。3)由于阴茎的独特性质,每个患者都有不同的病因,即使是最微创的注射药物也可能造成损伤,因此需要找到最适合ED的药物递送方法。因此,非侵入性透皮疗法值得进一步探索。4)现有的ED水凝胶治疗研究都是基于小动物的,只有一项研究应用了猪的模型,要将其推广到临床应用还有很长的路要走。