制药工业向连续制造的范式转变,最近已从概念论证发展到试生产,促进了过程系统工程( PSE) 工具的开发和应用,以实现高效和稳健的控制策略。本研究提出了一个药品连续固体制剂生产过程控制设计与风险分析的系统框架,包括系统辨识与状态空间模型; 控制设计和分析指标; 3 层递阶控制结构; 风险地图、评估和规划( 风险地图) 战略; 控制性能指标。该框架应用于进料混合系统,其中产品质量的主要差异源出现。可以证明,通过提出的控制设计和风险分析系统框架,可以缓解和管理进料配料系统中的差异。为了在先进的层次上实现有效的控制设计,用于原料药质量分数测量的过程分析技术( PAT) 工具及其相对标准差( RSD) 是必不可少的。具体而言,通过实施先进的基于模型的控制策略,控制性能的改善受到模型对象失配和 PAT 工具采样时间的限制。
在过去的 10 年中,通过广泛的研究,连续 2 次制造工艺在制药工业中的优势已经得到了体现,但主要是在概念或理论层面[1]。为了从概念性的连续设计转变为实际运行的试验工厂或制造过程,如辉瑞公司开发的便携式、连续式、微型和模块化技术( PCMM) ,鉴于监管机构、学术界和工业界的努力现集中在设计和实施问题上,具体介绍了实时释放控制结构的设计及其在连续固体制剂制造中的实现[2]。因此,本研究提出了一个系统化的控制设计与风险分析架构,以期达到有效且强健的主动过程控制。该框架由以下几个部分组成: 状态空间模型的系统辨识; 控制设计和分析指标; 3 层递阶控制结构; 风险地图、评估和规划( 风险地图) 战略; 控制性能指标。具体来说,递阶控制结构更侧重于实现,根据控制目标的规模、所需的过程理解以及处理过程干扰和风险的潜在能力对各层进行分类[3]。此外,不依赖于传递函数或卷积模型,提倡状态空间模型。
状态空间模型由于其固有的灵活性,在表示多元非线性过程和建模不可测量的干扰和过程时滞方面具有优势。除了常用的时间绝对误差积分( ITAE) 进行控制整定或性能评价外,还提出了 3 个新的性能指标,将控制性能与一致的产品质量直接联系起来[4-5]。
1、过程控制设计和风险分析的系统框架
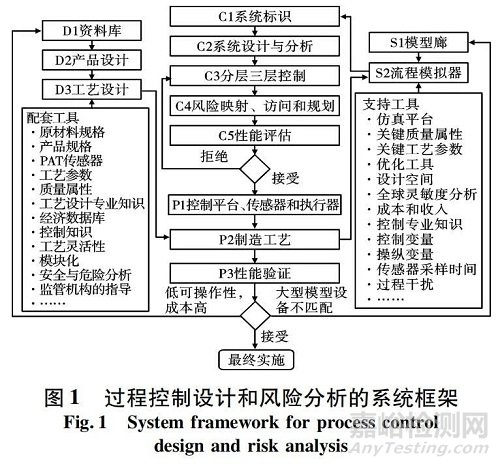
通过广泛的最终产品测试进行质量控制( 目前在传统的药品批量生产中实施) 与此相反,在连续的生产过程中,应在其指定的设定点实时监测和控制产品和通向产品的中间流的质量[6]。控制结构应能很好地响应由于过程变量、设备条件、进料原材料或环境因素的干扰和风险引起的潜在变化,以确保在产品退出过程序列时满足产品质量规范,这就是实时发布的含义。由各种过程系统工程工具组成的系统框架,用于开发和评估可行的控制策略,具体如图 1 所示。
拟议的控制框架还必须与其他辅助知识和工具相结合,以促进控制战略实施的软硬件一体化。例如,在基于从材料库( D1) 中获得的知识进行适当的产品设计( D2) 之后,将生成固体剂量的适当配方,需要特定的连续制造技术,即在工艺设计( D3) 中直接压实、干造粒或湿造粒。然后,将使用制药设备供应商提供的模块化单元操作( 进料、混合、压片等)配置试验工厂或制造工艺( P2) ,并在 P1 开发步骤中集成控制平台和 PAT 传感器。由模型库( S1) 和流程图模拟( S2) 软件组成的过程建模工具,通过加速工艺设计优化和实现期望的控制目标,在有效的全厂控制策略开发中发挥重要作用。例如,基于流程图模拟( S2) 的全局敏感性分析和系统识别( C1)可通过基本原理控制设计指标( 如相对增益阵列( RGA) ) 帮助识别和解决过程控制设计中的潜在挑战或风险,即分散、配对、稳定性、恢复力等,在控制设计与分析( C2) 中。一个分层的 3 层过程控制设计( C3) 和风险分析( C4) 将遵循严格的性能评估( C5) 。步骤 C3 到 C5 之间的迭代将继续进行,直到实现满足实时发布要求并遵守监管指南的控制器设计。所得到的控制设计将在制造过程( P2) 上实施,并在步骤 P3 中进行实验验证。制造工艺( P2) 的持续改进将通过提高模型预测精度或加强产品和工艺设计( D1 和 D2) 来实现。
2、控制性能指标
除了常用的性能指标,如用于控制整定和评估的时间绝对误差积分( ITAE) ,图 1 中建立了 C5 性能评估的 3 个附加性能指标,以明确地将控制性能与规范产品的一致性生产联系起来。如图 2 所示,第 1 个是时间到产品( T2P) ,T2P 描述干扰从其源传播到产品所需的时间量,并且它在一个或多个CQA 中被检测为偏差。在连续生产线中,如果在CPP 上游检测到不可接受的干扰,则 T2P 对于确定何时开始/准备转移不合格产品具有实际重要性。
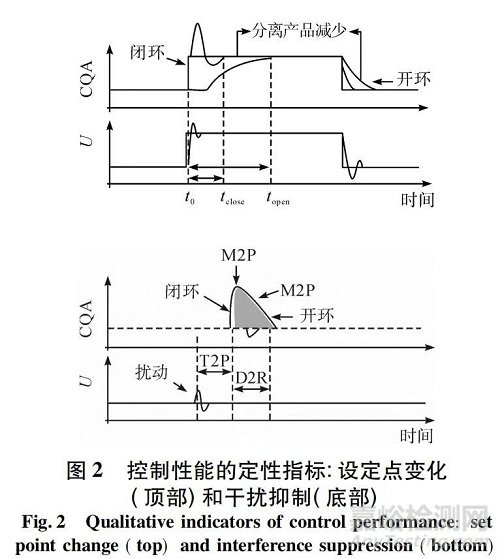
第 2 个指标,拒绝持续时间( D2R) ,是有或没有控制系统的过程消除过程干扰或达到 CQA 新设定点所需的时间长度。较小的 D2R 是理想的,这样当系统中发生过程干扰时,将产生较少数量的不合格产品。
第 3 个指标,量积比( M2P) ,描述了在操作过程时CQAs 与目标设定点的最大偏差。重要的是要限制控制动作,以避免大的 M2P,从而使 CQA 保持在设计空间内。图 2 显示了这些性能指标的定义,以及实施主动过程控制的潜在优势,与开环操作( 即手动或无需调整以维持 CQAs) 相比,这些标准定义了更好的性能。
对于如图 1 所示的制造过程( P2) 中的控制设计( C2) 的性能验证( P3) ,对于稳定的过程,应达到与 CQAs 的既定验收标准有关的统计控制状态,由于共同原因而产生的内在变异性可以用过程能力( Cp 和 Cpk) 指数来衡量。过程能力指数是一种广泛使用的统计方法,用于衡量一个过程在规范极限内产生产出的能力,表明一个过程相对于其规范极限所经历的自然变化有多大。它可以用来作为一个指标,以及如何控制过程。此外,还可以使用统计数据分析工具确定因果关系,从工艺操作条件和原材料质量中找出内在可变性的根本原因,以不断改进和优化当前工艺。
3、连续固体制剂生产中的加料配料系统
连续混合是固体制剂连续生产的第一步,原料药与辅料连续混合,以满足所需的粉末混合成分。由于通常没有进一步的下游步骤可以纠正混合成分,原料药含量及其在粉末中的均匀性是这一子系统中必须严格控制的 2 个重要 CQA。另一个需要严格控制的重要工艺参数是混合机出口粉末的总流量。这一重要的 CPP 影响固体加工线的生产率,当考虑到下游设备的有限滞留量时,这一点极为重要[7-8]。目前国内外对配料系统的系统控制系统设计和分析的研究较少; 下面将简要阐述该中试设备的进料混合系统,系统结构如图 3 所示。

连续制造过程的输入包括 2 个 Schenck Accu-Rate PureFeed AP - 300 失重给料机,它们能够通过测量和使用组合料斗和给料机装置中剩余粉末质量的变化来达到和保持规定的进料速率。这是通过嵌入 0 层控制系统实现的。喂料器将原料药对乙酰氨基酚 ( APAP ) 和赋形剂 Avicel 微晶纤维素PH - 200( MCC 200) 连续喂料到 Gericke GCM - 500连续混 合 器 中,其 中 2 种组分混合。操作条件( NOC) 包括 API 流量为 1.0 kg /h,赋形剂流量为9.0 kg /h,搅拌机转速为 200 r/min。使用近红外光谱仪( Control Development,Inc. ) 在搅拌机出口处原位测量 API 质量分数。使用 API 质量分数测量值在一个时间窗口内的平均值和方差,以相对标准偏差( RSD) 的形式对含量均匀性进行统计估计。使用基于 X 射线的质量流量计( SETXvue XP - 300,Enurga公司) 。这些设备使用 Delta V 进行集成,这些单元操作的过程变量被传输到再现 Delta V 系统,NIR 的信号处理延迟为 2 s,X 射线的信号处理延迟为 1 s。通过 LinkMaster 和 KepServer 软件包建立了 OPC DA协议,将实时过程数据从 Emerson DeltaV OPC 服务器传输到 MATLAB。
4、分层 3 层控制设计
图4 说明了建议的3 层结构在典型的连续直接压实过程中的应用,作为本工作的一个例子。一般来说,控制方法根据实现方法、复杂性和处理过程干扰和风险的潜在能力分为3 个层次。0 层控制技术包括单/多回路 SISO 控制,通常通过设备本身的可编程逻辑控制( PLC) 面板实现。简单反馈比例、积分和微分( PID) 控制、前馈比率控制或先进的专有 MPC 控制算法( 在高度非线性过程动力学情况下) 可在设备的 PLC 上实现。该控制层通常由设备供应商设计和提供,以控制单个/多个关键工艺参数,从而保持该设备的标称运行条件。
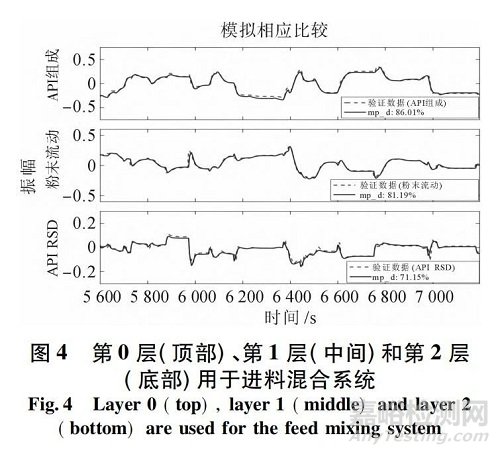
例如,失重给料机通常配备有内置控制回路,通过调整螺杆转速,将原料药、赋形剂或润滑剂等成分的流速保持在所需的设定值。在大多数情况下,1 层控制技术还涉及单回路或多回路 SISO 控制器; 然而,这些回路依赖于 PAT工具的使用来测量和直接控制 CQA,并且可能涉及多个单元操作。这些控制回路通常通过监控和数据采集( SCADA) 设备执行,例如 DCS 系统的商业 OPC服务器。OPC 服务器从现场所有单元操作设备检索数据或向其发送命令。例如,它可以在第 0 层PLC 控制面板上调整 CPP 变量的设定点。因此,第1 层控制通常使用级联回路来监督第 0 层控制,目的是实现关键质量属性( CQA) 的所需设置点,这些属性由 PAT 传感器现场测量。例如,在进料混合系统的情况下,粉末配方中的原料药成分是关键 CQA之一,可以通过在第 0 层控制器上操纵这些 CPP 的一个设定点来直接控制,例如原料药进料流量、赋形剂进料流量或搅拌机转速。CQA 可与对其具有最大影响的另一 CPP 上游配对; 因此,第 1 层控制通常跨越单元操作,并使用有效的反馈/前馈控制算法设计,以减少干扰的影响,否则可能会传播到下游。
5、结语
提出了一个基于风险的连续制造过程控制系统设计的系统框架,以评价控制系统开发的每一步。采用 SIMULINK 动态过程模型,将所提出的递阶3 层控制设计方法应用于配料系统。在风险图设计的基础上,在评价 3 层控制设计时还考虑了控制性能可能恶化的潜在风险。这些案例研究证明了在连续生产过程中,系统控制评价系统对于保证产品质量的重要性,并强调了基于 PAT 的反馈过程控制技术在药品连续生产中的应用。
这项工作的扩展将考虑 PAT 工具与现场 0 层控制的向下集成,以确保在每个单元操作中保持一致的质量属性,从而要求从上游单元到下游单元的最小程度的控制干预。这样的设计也将减少第 1 层和第 2 层全厂控制设计的负荷,并有助于单元操作的模块化。例如,如果 NIR 传感器与搅拌机集成,则可以通过调整转速将原料药含量均匀性控制下载到 L0 控制面板。研究还表明,解耦 PID 控制回路可以有效地控制原料药的混合均匀性。在我们正在进行的研究中,将建议的框架应用到完整的压片线。
参考文献
[1] SU Q L,MORENO M,GAMESH S,et al. Resilience and risk analysis of fault-tolerant process control design in continuous pharmaceutical manufacturing[J]. Journal of Loss Prevention in the Process Industries,2018,55: 411-422.
[2] SU Q,BOMMIREDDY Y,GONZALEZ M,et al. Variation and risk analysis in tablet press control for continuous manufacturing of solid dosage via direct compaction[J].Computer Aided Chemical Engineering,2018,44: 679-684.
[3] SU Q L,GANESH S,MORENO M,et al. A perspective on Quality-by-Control (QbC) in pharmaceutical continuous manufacturing[J]. Computers & Chemical Engineering:
An International Journal of Computer Applications in Chemical Engineering,2019,125: 216-231.
[4] GANESH S,SU Q,PEPKA N,et al. Design of conditionbased maintenance framework for process operations management in pharmaceutical continuous manufacturing[J].International Journal of Pharmaceutics,2020,587:119621.
[5] SU Q,REKLAITIS G V,NAGY Z K. Continuous feedingblending in pharmaceutical continuous manufacturing
[M]/ /Continuous Pharmaceutical Processing. Cham:Springer,2020.
[6] SU Q L,BOMMIREDDY Y,SHAH Y,et al. Data reconciliation in the Quality-by-Design( QbD) implementation of pharmaceutical continuous tablet manufacturing[J]. International Journal of Pharmaceutics,2019,563: 259-272.
[7] TIAN G,KOOLIVAND A,GU Z,et al. Development of an RTD-Based Flowsheet Modeling Framework for the Assessment of In-Process Control Strategies [J]. AAPSPharm Sci Tech,2021,22( 1) : 1-10.
[8] BHASKAR A,SINGH R. Residence time distribution
( RTD) -based control system for continuous pharmaceutical manufacturing process[J]. Journal of Pharmaceutical Innovation,2019,14( 4) : 316-331.
[9] SU Q L,NAGY Z K,RIELLY C D. Pharmaceutical crystallisation processes from batch to continuous operation using MSMPR stages: Modelling,design,and control[J].Chemical Engineering and Processing,2015,89: 41-53.
[10] ENGISCH W,MUZZIO F. Using residence time distributions( RTDs) to address the traceability of raw materials in continuous pharmaceutical manufacturing[J]. Journal of Pharmaceutical Innovation,2016,11( 1) : 64-81.