今日头条
云顶新耀引进肾病新药落地博鳌。云顶新耀从Calliditas公司引进的布地奈德迟释胶囊Nefecon(耐赋康)获得海南省药品监督管理局批准,将在上海交通大学医学院附属瑞金医院海南医院应用于临床使用。Nefecon是全球首款获批治疗IgA肾病的靶向药,在临床(NefIgArd)试验中较安慰剂降低患者27% (P=0.0003) 的尿蛋白肌酐比。此前,该新药已被CDE纳入优先审评,以及突破性治疗品种。
国内药讯
1.君实PCSK9单抗报降脂NDA。君实生物自主研发的PCSK9单抗注射液昂戈瑞西单抗(JS002)两项适应症上市申请获国家药监局受理,分别为用于原发性高胆固醇血症(包括杂合子型家族性和非家族性)和混合型血脂异常的治疗;以及用于成人或12岁以上青少年的纯合子型家族性高胆固醇血症的治疗。目前,国内已有两款进口PCSK9单抗获批上市,尚无国产PCSK9单抗获批上市。
2.天境CD47抗体上III期注册临床。天境生物创新CD47抗体来佐利单抗与阿扎胞苷联用治疗较高危骨髓增生异常综合征(HR-MDS)的中国III期注册临床(NCT05709093)首例患者给药。在II期研究(NCT04202003)中,该联合疗法治疗6个月时达到86.7%的客观缓解率和40%的完全缓解率。而且联合治疗总体耐受性良好,安全性与阿扎胞苷单药治疗相当。
3.上海信念血友病基因疗法完成Ⅲ期临床入组。信念医药旗下上海信致自主研发的AAV基因疗法BBM-H901注射液治疗血友病B的Ⅲ期注册临床(CTR20212816)完成全部受试者给药。该项研究旨在评估单次静脉输注BBM-H901在≥18岁且内源性凝血因子Ⅸ(FⅨ)活性≤2 IU/dL(即≤2%)的血友病B患者中的安全性和有效性。去年8月,该新药已获CDE纳入突破性治疗品种,用于预防血友病B(先天性凝血因子Ⅸ缺乏症)的成年男性患者出血。
4.伟德杰IL-6R抗体罕见病Ⅱa期临床积极。伟德杰生物重组人源化白介素-6受体单克隆抗体注射液VDJ-001治疗特发性多中心型Castleman病(iMCD)的Ⅱa期临床结果积极。iMCD是一类HHV-8阴性、病因未明,由高炎症因子介导的淋巴组织增生性罕见病。VDJ-001旨在通过与IL-6受体特异性结合以阻断IL-6经典、反式及反式呈递三种通路。该项试验数据显示,VDJ-001总缓解率达到55.6%,肿瘤缓解的中位时间为56天;药物总体耐受性良好。
5.礼新与LegoChem合作开发实体瘤ADC。礼新医药与LegoChem Biosciences达成合作许可协议,双方将使用礼新医药基于独家抗体发现平台研发的抗体资产以及LCB的ADC技术平台,针对未公开的实体瘤靶点,合作开发一种新型ADC候选产品。LCB是一家全球领先的ADC技术平台企业,在ADC开发方面拥有出色的成绩。此前,复星集团自Legochem引进了创新型定点抗体偶联药物FS-1502,拟开发用于HER2阳性的晚期乳腺癌和/或晚期恶性实体瘤的治疗。
6.药明康德2023年Q1业绩持续增长。药明康德公布2023年第一季度财务报告,公司营业收入89.64亿元,同比增长5.8%;归母净利润21.68亿元,同比增长32.0%;经调整Non-IFRS归母净利润23.42亿元,同比增长14.1%。其中,化学业务实现收入64.33亿元(+5.1%),测试业务14.53亿元(+13.6%),生物学业务5.77亿元(+8.3%),细胞及基因疗法CTDMO业务3.24亿元(+8.7%),国内新药研发服务部1.66亿元(-31.0%)。
国际药讯
1.渤健/lonis渐冻症新药获FDA批准上市。渤健与lonis公司联合开发的反义寡核苷酸(ASO)疗法tofersen获FDA加速批准上市,用于治疗超氧化物歧化酶1 (SOD1)突变所致的肌萎缩侧索硬化(ALS,俗称渐冻症)患者。这是一种进行性神经退行性疾病,SOD1-ALS是ALS的一种罕见遗传性形式。Tofersen通过与编码SOD1的mRNA结合,使其被核糖核酸酶降解,从而减少SOD1蛋白的产生。这是首款针对ALS的基因靶向疗法。
2.肾性贫血创新口服新药获欧盟批准上市。Akebia公司口服HIF-PHI抑制剂Vafseo(vadadustat)获欧盟委员会(EC)批准上市,用于治疗接受慢性维持性透析的成人慢性肾脏疾病(CKD)相关的症状性贫血。在两项INNO2VATE研究中,通过基线与主要评估期(第24至36周)和次要评估期(40至52周)之间血红蛋白(Hb)的平均变化来衡量,vadadustat与darbepoetin α(一种血红细胞刺激剂)相比达到非劣效性标准。
3.Insulet便携式胰岛素泵获FDA批准上市。Insulet公司用于输送基础胰岛素的胰岛素泵Omnipod GO获FDA批准上市,用于18岁及以上的2型糖尿病患者,可提供七种不同的预先设定好的每日输注速率。Omnipod GO为Omnipod系列的最新产品,这是一种独立的、可穿戴的胰岛素输送系统,它可在72小时内提供固定速率的连续速效胰岛素。此外,该产品具有无管、防水的输液泵设计,无需手持设备即可控制输液泵。
4.小分子α4β7整合素抑制剂Ⅱ期临床积极。Morphic Therapeutic公司口服小分子α4β7整合素(integrin)抑制剂MORF-057治疗中重度溃疡性结肠炎(UC)的Ⅱa期试验EMERALD-1达到主要终点。与基线相比,患者第12周Robarts病理指数(RHI)评分显著下降6.4分(p=0.002);Mayo内镜评分(mMCS)减少2.3分。MORF-057在每日两次100 mg剂量下的耐受性总体良好,没有严重不良事件(SAEs)和安全信号。
5.Bridge公司第四代EGFR-TKI获批临床。Bridge Biotherapeutics公司针对第三代表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)耐药的晚期肺癌患者开发的广谱EGFR-TKI产品BBT-207获FDA批准开展首次人体研究。公布于AACR2023年会上的临床前数据显示,BBT-207在针对非小细胞肺癌(NSCLC)中广泛存在的EGFR突变具有积极的抗肿瘤活性,包括那些在第三代EGFR-TKI治疗后出现的C797S突变。
6.Vedanta公司融资推进新型抗菌口服药开发。Vedanta Biosciences公司完成1.065亿美元融资,以用于推进其新型抗菌口服药VE303在复发性艰难梭菌感染(CDI)中的关键性Ⅲ期试验,以及在溃疡性结肠炎中进行VE202的概念证明Ⅱ期试验。VE303是基于从人类微生物组中分离出的细菌并从纯克隆细胞库中培养的明确菌群开发的治疗候选药物。此次投资包含现有投资者比尔及梅琳达•盖茨基金会、Skyviews Life Science等。
医药热点
1.国家儿童医学暨临床研究中心IEI联盟成立。4月25日,由复旦大学附属儿科医院临床免疫科牵头,八家单位(三家国家儿童医学中心,两家国家儿童健康与疾病临床研究中心等)共同发起的“国家儿童医学暨临床研究中心IEI联盟”正式成立。联盟将以促进国内相关医疗机构之间,基础与临床之间,儿童与成人之间在原发性免疫缺陷病领域通力合作为主要工作内容,并积极致力于促进我国在这一领域与国际间的高水准交流。
2.詹启敏院士担任健康传播工作委主委。近日,中国医师协会正式任命中国工程院院士詹启敏担任中国医师协会健康传播工作委员会主任委员。根据公开信息,詹启敏,中国工程院院士,北京大学博雅讲席教授,北京大学校务委员会副主任。担任北京大学国际癌症研究院院长,北京大学健康医疗大数据国家研究院院长、北京大学肿瘤医院分子肿瘤学实验室主任。担任苏州大学苏州医学院院长。
3.北京最大医院挂号平台停止线上预约。4月24日,北京市卫健委在京医通公众号发布重要通知,宣布即日起「京医通」原线上预约挂号服务停止。据悉,北京市目前有多种形式可以预约挂号:北京114预约挂号平台已完成升级,提供270家医院预约挂号,基本覆盖北京市重点三级医院;从4月23日起,北京近200家公立医院开通支付宝挂号预约服务;此外,2023年3月,北京多家医院相继开拓线上挂号渠道,通过微信上线或升级预约挂号服务平台。
评审动态
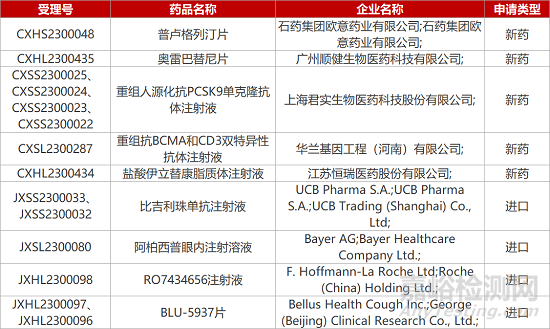
1. CDE新药受理情况(04月26日)
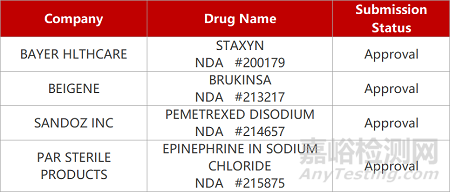
2. FDA新药获批情况(北美04月24日)