Cardiac Dimensions宣布用于治疗功能性二尖瓣反流(FMR)和心衰的产品Carillon获得MDR的认证。

Cardiac Dimensions此次重新向CE注册Carillon,是为了满足欧盟新的医疗器械法规---MDR。在欧盟老法规(MDD)时,Carillon分别于2009年和2011年获得CE批准用于治疗功能性二尖瓣反流(FMR)和心衰两种疾病。Carillon已经在欧洲和澳大利亚上市十多年,在美国依旧属于研究性产品。
MDR相比于MDD注册难度指数级增加,根据统计截止去年12月底只有不到10%的产品(之前获得MDD认证)获得MDR认证。国产高风险的医疗器械获得MDR产品更少,在结构心脏病领域启明医疗的VenusP-Valve是第一款获得MDR认证,同时在欧洲市场获得广泛认可。
高管评价
“我为我们的团队感到骄傲,他们投入了大量时间和资源,确保我们的设备和系统达到欧盟制定的新的高标准,领先于我们行业的许多人。Carillon的卓越安全性,加上支持Carillon的大量高质量临床证据,是获得MDR认证的关键因素。这一里程碑向我们的医生合作伙伴和患者发出信号,他们可以对Carillon的安全性和卓越制造充满信心。”
----Rick Wypych Cardiac Dimensions CEO
CARILLON
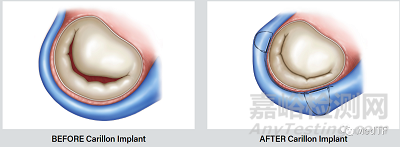
CARILLON是唯一一种间接的、非接触式二尖瓣修复方案,旨在产生瓣环成形术效果,同时启动左心室重塑并提高患者的长期生存率。CARILLON能够治疗功能性二尖瓣反流(FMR)和心衰。
CARILLON包括植入物和输送系统。植入物是一个类“桥状”器械,通过一个带状物将近端锚和远端锚连接在一起。植入物采用类似冠状窦型状,植入植入物后能够减少二尖瓣环扩张,进而减少功能性二尖瓣反流(FMR)。植入物通过输送系统将植入物输送到病灶处。

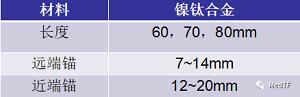
1、植入物
植入物尺寸及材质
2、输送系统
输送系统包括鞘管和操作手柄;
CARILLON 有以下使用优点:
a.手术时间短,整个植入手术只需1小时;
b.能够治疗病情较轻(MR 2+级)患者
c.保留未来的治疗选择,例如 CRT
d.无需额外的抗凝治疗;
e.无需全身麻醉;
f.房间隔缺损(ASD)未发生。
CARILLON 临床研究
在今年TCT 2022上,公布来自上市后临床数据,本项研究涉及101名患者。
有效性
96%的患者在12个月时达到了2+或更低的MR等级,而100%的患者在5年时达到了MR等级。超过69%的患者在一年内NYHA等级为II+或更低,这一比例在五年内提高到79%。
安全性
一年内未发生器械相关的重大不良事件。两年后,死亡率和心力衰竭住院率也明显优于标准医疗管理和其他商业器械治疗的公布数据。之前发表的Carillon装置6年生存数据显示,与医疗管理相比,存活率良好。
Cardiac Dimensions
CardiacDimensions是开发创新性微创治疗模式以解决心力衰竭和相关心血管疾病的领导者。该公司的最初技术平台Carillon Mitral Contour System旨在利用新颖的经皮穿刺方式解决功能性二尖瓣反流(FMR)和心衰问题。