您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2023-05-08 13:01
本文适用于定量剪切波超声肝脏测量仪,根据《医疗器械分类目录》,属于07医用诊察和监护器械分类下07超声生理参数测量、分析设备中的02超声人体组织测量设备,分类编码为07-07-02,产品的管理类别为三类。
一、定量剪切波超声肝脏测量仪产品的结构及组成
定量剪切波超声肝脏测量仪一般由主机、硬度检测探头、超声影像探头、脚踏开关组成。该产品应用瞬时弹性成像技术对组织的硬度进行测量。硬度检测探头通过振动发生器发出机械振动,该振动在组织中传播产生低频剪切波,由于低频剪切波在组织中传播的速度与组织的硬度正相关,可利用脉冲回波技术来捕捉剪切波的传播过程,计算剪切波的传播速度,从而得到组织的硬度值。这种方式可以实现无创、快速、定量地检测肝脏组织硬度,评估肝脏纤维化程度。该产品还可通过检测超声波在组织内传播的衰减来评价肝脏脂肪变进程。
由于肝脏组织结构对检测结果影响较大,部分产品在检测硬度之前需通过超声影像探头进行检测位置确认,用影像探头对肝脏部位进行超声影像扫查,避开大血管、囊肿、实体病变,选择肝脏组织均匀、无大的管道结构的部位进行检测,提高检测结果的准确性和一致性。
硬度检测探头一般由超声换能器、振动发生器、启动按键、外壳、探头连接线组成,如图1所示。振动发生器产生的机械振动在组织中形成剪切波,该剪切波通过皮肤、皮下脂肪到达肝脏。在剪切波传播的过程中,超声换能器记录不同时刻的超声回波信号,从而得出肝脏内的剪切波传播速度及衰减。若一个型号的硬度检测探头不能覆盖所有患者,使用者可根据患者皮肤到肝包膜的距离选择不同测量深度的探头,如图2、图3所示。

图1 硬度检测探头结构示意图
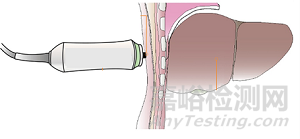
图2 检测示意图
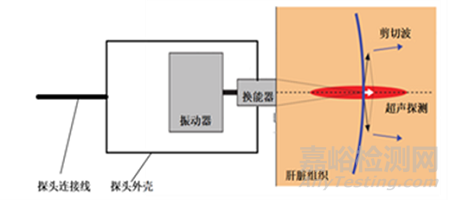
图3 剪切波传播示意图
二、定量剪切波超声肝脏测量仪主要风险
定量剪切波超声肝脏测量仪产品风险点举例见表1,该表所列出的风险点、危害仅为与产品密切相关的部分,并不能代表设备的全部风险。开发人应依据自身的质量管理体系要求,结合产品特点评估相关风险,并建立起科学全面的风险分析与管理制度,进而避免较大程度的风险及危害的发生。
表1定量剪切波超声肝脏测量仪主要风险点
|
主要风险点 |
可能产生的危害 |
|
声输出风险 |
设备故障或失控,导致过大超声能量作用于人体; 产品声输出控制、显示功能失效或故障。 |
|
机械风险 |
设备脚轮锁定不良,移动式设备稳定性差,出现倾倒。 |
|
生物学风险 |
探头与人体接触材料生物相容性差,患者皮肤致敏。 |
|
使用风险 |
清洁消毒不当,造成患者感染皮肤疾病。 |
|
应用于非适用人群或探头与患者不匹配,测量结果不准确。 |
|
|
维护不当或超过维护期限使用,影响测量结果的准确性。 |
|
|
未按照说明书内容对测量结果进行解读,导致诊断错误。 |
|
|
存放环境不当,导致设备受潮或漏电,进而引发患者伤害 |
|
|
非专业用户使用,错误操作导致设备损坏或使用者伤害 |
三、定量剪切波超声肝脏测量仪性能研究实验要求
1、性能指标
需参考YY/T 1749的要求并结合产品特征确定产品技术要求,性能指标至少需包括工作频率、探测深度、硬度测量范围(kPa)、硬度测量准确度、硬度测量重复性、声衰减参数测量范围(dB/m)、声衰减参数测量准确性、声衰减参数测量重复性。以上内容应针对每个探头分别确定。
正常和病变肝脏硬度范围通常在4~24kPa之内,生理结构上肝脏的深度(肝脏上下径)通常≥65mm,肝脏组织的声衰减系数一般为0.4~1.0dB/cm/MHz,3.5MHz对应的声衰减参数为140~350dB/m。以上内容来自于成人的生理参数统计数据,产品性能指标制定可参考以上参数范围。
除以上测量性能外还应明确产品的软件性能和网络性能要求,如软件功能、使用限制、接口、访问控制等。若产品含有脚踏开关,应明确脚踏开关的要求,可参考YY/T 1057。若为内部电源供电产品应明确内部电源单独供电时产品连续使用时间的要求。
安全性应满足GB 9706.1《医用电气设备 第一部分:安全通用要求》/GB 9706.1《医用电气设备 第1部分:基本安全和基本性能的通用要求》、YY 0505《医用电气设备 第1-2部分 安全通用要求并列标准 电磁兼容 要求和试验》/ GB 9706.102《医用电气设备 第1-2部分:基本安全和基本性能的通用要求 并列标准:电磁兼容 要求和试验》、GB 9706.9-2008 《医用电气设备 第2-37部分:超声诊断和监护设备安全专用要求》/ GB 9706.237《医用电气设备 第2-37部分:超声诊断和监护设备的基本安全和基本性能专用要求》的要求。
2、化学和物理性能研究
开发人需要开展产品性能研究,并明确产品技术要求及产品各性能指标条款来源和制定依据。开发人根据产品应用模式、使用方式、产品配置等,进行相应的测试验证。
应明确探头与人体接触部分的化学材料表征。
应针对硬度测量和声衰减测量功能开展研究和确认。应确认整个测量范围内测量结果的准确性和重复性。可采用体模对测量结果的准确性、重复性进行评价。需明确试验体模的技术参数,如杨氏系数(kPa)、超声纵波传播速度(m/s)和衰减系数(dB/cm/MHz)。
3、电气系统安全性研究
应开展电气安全性及电磁兼容性的研究。目前与本产品相关的标准包括:GB 9706.1《医用电气设备 第一部分:安全通用要求》/ GB 9706.1《医用电气设备 第1部分:基本安全和基本性能的通用要求》、YY 0505《医用电气设备 第1-2部分 安全通用要求并列标准 电磁兼容 要求和试验》/ GB 9706.102《医用电气设备 第1-2部分:基本安全和基本性能的通用要求 并列标准:电磁兼容 要求和试验》、GB 9706.9-2008 《医用电气设备 第2-37部分:超声诊断和监护设备安全专用要求》/ GB 9706.237《医用电气设备 第2-37部分:超声诊断和监护设备的基本安全和基本性能专用要求》。
4、声输出安全研究
声输出安全在满足GB 9706.9的基础上,还应规定声能输出的限值,以确保其安全性。应对声能输出限值设置的合理性进行分析,明确设定的依据,并进行设备实际声能输出能够满足限值要求的验证。限值的设定及测试的方法应参考业界通用的准则。硬度测量探头一般采用单阵元换能器,声输出较低,通常MI不超过1,TI不超过1,Ispta.3不超过190mW/cm2。
5、软件研究和网络安全研究
定量剪切波超声肝脏测量仪软件通常为软件组件,开发人可以依据《医疗器械软件注册审查指导原则》中的软件组件要求开展软件研究。软件研究报告需要覆盖全部软件组件和产品功能。考虑该类产品风险程度和不良事件情况,一般应确定为中等或以上的安全性级别。
产品若具有电子数据交换、远程访问与控制、用户访问三种功能当中一种或一种以上的功能,开发人应参照《医疗器械网络安全注册审查指导原则》开展网络安全研究。
6、生物学特性研究
开发人应按照GB/T 16886.1的要求进行生物相容性评价。产品预期与患者接触的部件为探头,与患者完整皮肤进行短期接触。生物学评价内容至少包括细胞毒性、皮肤刺激、迟发型超敏反应。评价对象应为清洁消毒后的成品探头。
7、清洁、消毒研究
探头通常为重复使用,与人体完整皮肤短期接触,使用前需进行清洁、消毒。应明确推荐的清洁和消毒工艺(方法和参数)、工艺的确定依据并进行验证。应当开展产品所推荐消毒工艺耐受性的研究,对其多次消毒后的功能、安全进行验证。若产品经消毒后可能产生残留物质,应进行残留毒性的研究,明确残留物信息及采取的处理方法。
探头仅与完整皮肤短时接触,低水平消毒一般可以保证使用的安全性。
8、稳定性研究
开发人可以依据《有源医疗器械使用期限注册技术审查指导原则》开展产品使用期限的研究。开发人应考虑在正常条件和不利条件下对产品进行分析。应分别对主机、探头和脚踏开关的使用期限进行研究。
推荐采取疲劳试验的方式评价主机和探头寿命。若采用以关键部件寿命来评估主机寿命,则应明确关键部件的选择依据。影响探头寿命的因素一般为激发振动和消毒,应开展探头的总激发振动次数和可耐受消毒次数研究,根据临床实际使用频次换算成探头的使用寿命。
老化后的主机与探头需进行性能测试,测试项目至少包括工作频率、测量深度范围、硬度测量范围、硬度测量准确性、硬度测量重复性误差、声衰减参数测量范围、声衰减参数测量准确性、声衰减参数测量重复性等。
若检验报告已证明产品符合YY/T 1057的要求,检验报告结论可代替脚踏开关的寿命研究。
若采用可充电内部电源供电方式工作,还应开展电池使用寿命和充放电次数的相关验证。
应对产品的使用稳定性和运输稳定性进行研究,使用稳定性研究需包括额定工作高低温试验、湿热试验。运输稳定性研究需包括湿度存储、高低温储存、振动、碰撞、运输试验,可参考GB/T 14710进行试验。

来源:嘉峪检测网


