昨儿晚上看到European Society of Cardiology新公布的MONITOR-HF的研究结果,如下图2,想起这么些年也确实没有好好写一写大A厂的CardioMEMS HF系统,今天就来新增一期吧。
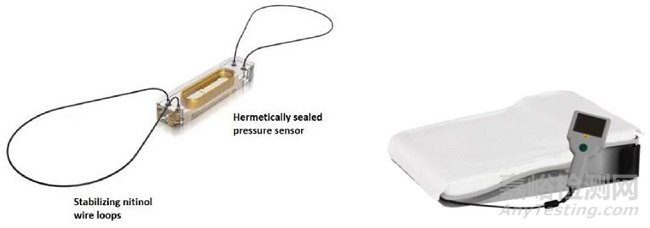
图1 CardioMEMS HF系统(肺动脉压在心力衰竭失代偿期数天至数周前开始升高,是充血的标志,因此心衰患者监测追踪肺动脉压可及早进行干预,从而改善充血症状并降低住院的需要)
图2 MONITOR-HF研究结果,已发表在了Lancet杂志上
如上图1,这个永久肺动脉PA植入物早在2014年5月即获得FDA批准,当时它甚至还不属于圣某厂(不过早在2010年圣某厂已经很有远见地以6,000万美金购买了其19%的股份,并已拥有了购买选择权;最终同样在2014年以3.75亿美金收购了剩余的81%)。作为第一个植入式肺动脉压力测量器械,CardioMEMS HF系统的目标人群一直是心力衰竭患者,植入后能够在多个场景下(医生办公室、诊所、医院或患者家中)收集数据,其收集的数据包括:1)肺动脉PA压力波形;2)PA收缩压、舒张压和平均压;3)心率,这些血流动力学数据被传输到安全数据库,以作为心衰患者监测的一部分,指导治疗。其主要专利如下:
图3 CardioMEMS公司的部分专利
图4 CardioMEMS公司的CTO,Jason Kroh博士。在2001年加入CardioMEMS之前,Kroh博士是Cybersonics的首席电气工程师,主要开发用于NASA喷气推进实验室(Jet Propulsion Laboratory)的超声波/声波钻孔取芯器的驱动技术,该技术现已拓展至碎石和溶栓等大家很熟悉的医疗应用。在离开CardioMENS后,他先后担任了Vero Biotech和Sarvint Technologies的副总裁,最后担任了Strados Labs的CTO(降维打击...)(2016年成立的Strados Labs,现已成功开发了使用声学肺音/呼吸音技术的呼吸、活动追踪平台,旗下的RESP呼吸健康智能传感器平台已于去年获得FDA II类 510(k)批准)
岔开一句,上图4提到的呼吸音,大家都懂的,这个不好开发啊。但是,如果机器算法、人工智能真的可实现准确、成功地鉴别诊断,那么其应用范围要远远大于心衰患者。目前Strados Labs的RESP技术仍然处在早期监测咳嗽、喘息、爆裂声和其他突发事件的阶段,暂时替代不了听诊(和心电监测相比,不知准确性如何)。
图5 Strados Labs的RESP
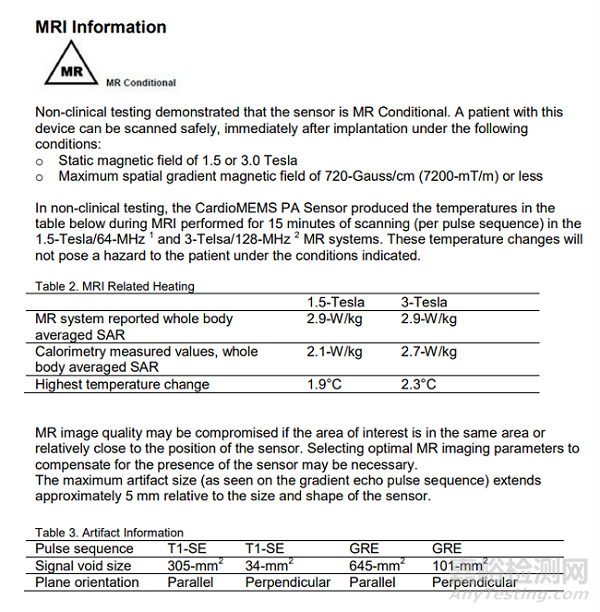
不好意思岔远了,我们再说回肺动脉。顺便,CardioMEMS是可以在部分磁共振条件下正常使用的,如下图6,也不会影响起搏器和/或除颤器的工作。它也无需更换电池或器械,植入后工作时长可覆盖整个患者寿命。
图6 CardioMEMS HF系统的磁共振使用信息,来源IFU
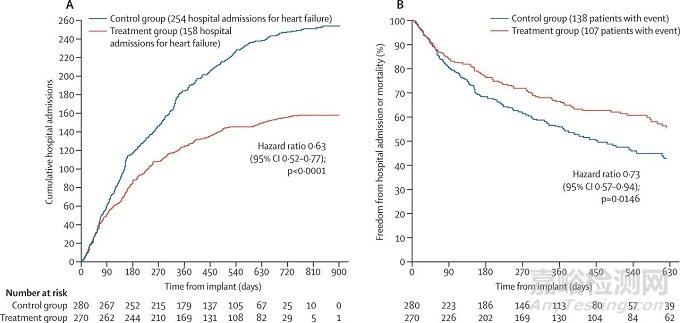
CardioMEMS最有名的是2011年的Champion研究,这个美国本土的单盲、随机对照研究,在64个中心招募了550名NYHA III级的心力衰竭患者,其中治疗组270名患者在6个月时,与心衰相关的累积住院率显著降低了28%,如下图7。在整个随访期间,治疗组的肺动脉压平均降幅更大,因心衰入院的患者更少,住院时间更短,出院后存活的天数更多,生活质量也更高。(文中提到,当时由心衰专家、电生理专家和介入心脏病学专家进行植入,该研究中未出现任何器械相关的肺动脉栓塞,也没有植入器械需要移除)
图7 Champion研究,在整个随机单盲随访期间的心衰相关累计住院数(A),以及整个随访期间无首次心衰相关的住院或死亡率(B)
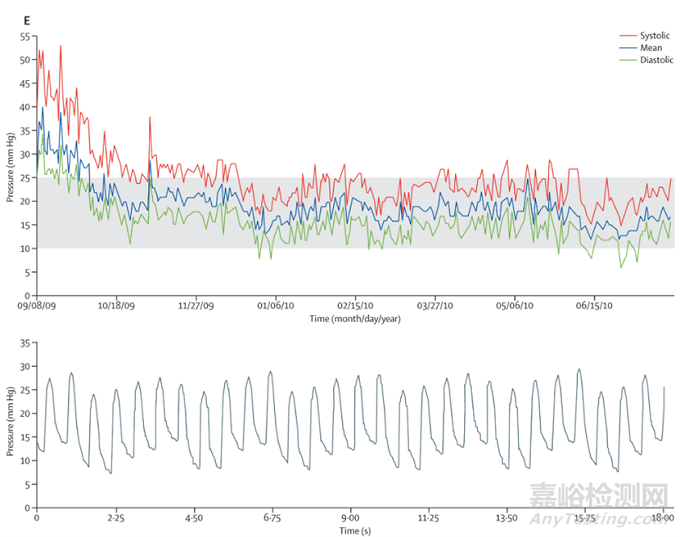
图8 CardioMEMS传输的信息包括压力趋势和单个肺动脉压力波形
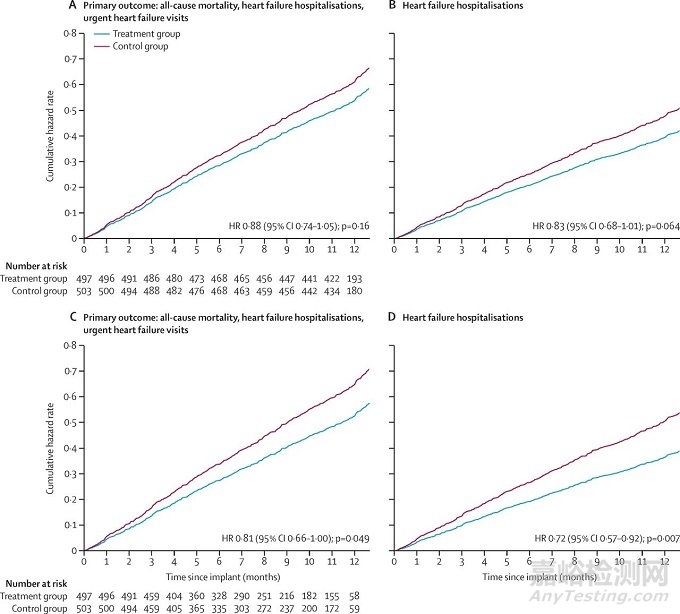
于是,在被收购后,大A厂赞助了另一个美国和加拿大的GUIDE-HF研究,仍然是一个单盲、多中心、随机对照的研究,纳入的则为NYHA II~IV级的心衰患者(或利钠肽升高但并无心衰病史的患者)(意图也很明显~)。但在118个中心入选的1,022例患者中,有22例植入不成功(就没提怎么不成功),剩下1,000例进行随机分组。研究者们最终发现,血流动力学指导下的管理并未降低心力衰竭事件的累积发生率(p=0.096)。虽然COVID-19大流行前的分析表明,CardioMEMS可能有益,并可能使得心衰住院率降低。(在讨论部分,研究者们提到新冠大流行期间对照组主要终点事件显著减少的原因,包括了患者依从性提高、医疗保健提供者行为改变、COVID-19导致的疾病进展变化,等等)
图9 GUIDE-HF研究,主要复合终点以及心衰住院的累积风险率曲线,其中(C)和(D)为COVID-19大流行前的数据分析
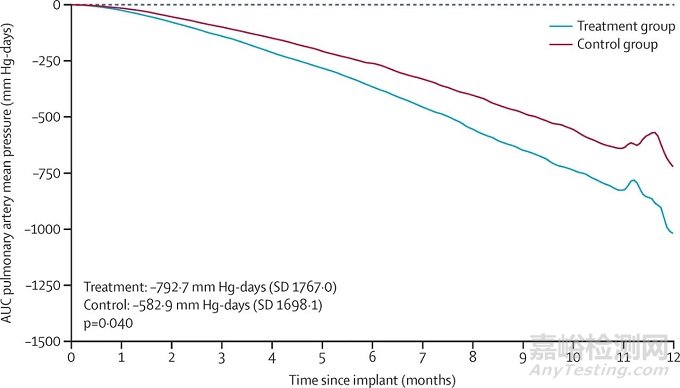
图10 GUIDE-HF研究,两组平均肺动脉压降低情况
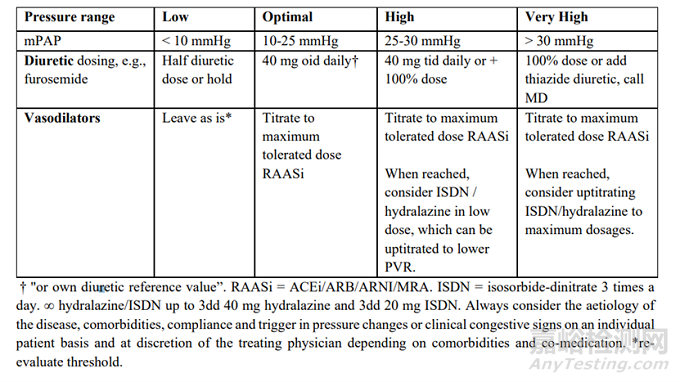
本次新发表的MONITOR-HF研究仍针对的是NYHA III级的患者(与Champion一致),不过是在荷兰25家中心进行的入组,且并未设盲。结果显示治疗组患者的生活质量显著提升,如上图2。MONITOR-HF中,有4名患者(2.3%)出现器械相关的不良事件,其中2名是侵入性治疗措施引起的咳血,另2名为心律失常,分别为心房扑动和房室传导阻滞。在随访期间,有2名患者(1.2%)出现信号丢失,均为器械移位所致。
图11 心衰患者不同肺动脉压下的治疗指导
那么,今天就写到这吧。最后稍微地展示一下CardioMEMS的同类产品,首先即大家可能更熟悉的Endotronix公司的Cordella,如下图12,可以说设计理念和CardioMEMS基本一致,无需多言。另一个则是Biotronik 2012年即发表的COMPASS(Implantable pressure monitoring system),见下图13。但是COMPASS仍然需要一个发生器,这就意味着其手术风险相对CardioMEMS和Cordella仍较高;好处是可读取与分析的数据更多,COMPASS可同时监测左、右心室压,主动脉压和肺动脉压,还能监测心音。这就带来了另一个问题,COMPASS现在去哪了~
图12 Endotronix公司的Cordella肺动脉压力传感器
图13 Biotronik公司的COMPASS压力监测系统
引用文献:
1. A. Urbaszek, J. Kirchner, A. van Ooyen, O.Skerl. Hemodynamic monitoring with an implantable pressure monitor is improved by additional detection of heart sounds. Biomed Tech 2012;57(Suppl.1).
2. JoAnn Lindenfeld, Michael R. Zile, Akshay S. Desai, et al. Haemodynamic-guided management of heart failure (GUIDE-HF): a randomized controlled trial. Lancet 2021;398:991-1001.
3. Jasper J. Brugts, Sumant P. Radhoe, Pascal R.D.Clephas, et al. Remote haemodynamic monitoring of pulmonary artery pressures in patients with chronic heart failure (MONITOR-HF):a randomized clinical trial. Lancet. Published Online May 20, 2023. https://doi.org/10.1016/S0140-6736(23)00923-6.
4. William T. Abraham, Philip B. Adamson, Robert C. Bourge, et al. Wireless pulmonary artery haemodynamic monitoring in chronic heart failure: a randomized controlled trial. Lancet 2011;377:658-66.