背景介绍:
FDA关于透皮贴剂的描述:经皮给药系统是将活性成分(药物)递送穿过皮肤并进入全身循环(Transdermal delivery systems),而局部递送系统(topical delivery systems)是将活性成分递送至局部组织[1]。《中华人民共和国药典》2020 年版关于贴剂描述如下:贴剂系指原料药物与适宜的材料制成的供贴敷在皮肤上的,可产生全身性或局部作用的一种薄片状柔性制剂。贴剂可用于完整皮肤表面,也可用于有疾患或不完整的皮肤表面。其中用于完整皮肤表面能将药物输送透过皮肤进入血液循环系统起全身作用的贴剂成为透皮贴剂[2]。一般用于局部作用的贴剂较多为阵痛类,如包括活血止痛膏或者氟比洛芬、洛索洛芬钠巴布膏或凝胶贴膏等。市面上还有很多止痛的贴剂,药物成分中可能还有中成药、止痛药等。现代的透皮贴剂应用更加广泛,可用于治疗多种病症和疾病,包括用于绝经引起的中度至重度血管舒缩症状、阿尔茨海默病、注意力缺陷多动障碍、重度抑郁症、慢性疼痛的控制、恶心和呕吐的预防、预防心绞痛等[3]。
近年来,外用贴剂因去除了肝脏的首过清除效应,避免了药物化学与生物效应对于胃肠道的刺激,降低或避免副作用的发生,而且由于药物的靶向性较好,药物的使用剂量也大为减少,病人使用也较方便,而越来越受到人们的关注。根据数据研究显示,未来10年内,透皮给药制剂将保持2位数的年复合增长率,远超医药工业的平均增长率。目前市场体量最大的是美国(大约26亿美元)和日本(大约26亿美元),其次是德国(约3.7亿美元)。透皮给药技术领先的也是美国,日本和欧洲,中国市场相对空白。本文就透皮贴剂的特点,国内外获批药物以及处方和工艺研究等方面的进展进行概述,以期为我国开展贴剂类研究提供参考。
1、人体皮肤的组成结构
人体皮肤结构如图1所示[4],皮肤已经演变成一种极其有效的屏障,它既防止了体内水分的过度流失,也防止了外来生物的进入。
透皮给药具有持续的和可受控释放药物的能力。这种良好的使用方法可以提高患者的依从性。然而,由于皮肤的屏障阻碍了药物分子的传递,经皮给药在临床上的应用上同样受到了限制。皮肤的屏障主要为角质层的细胞间脂质双层。皮肤的外层角质层形成了几乎所有化合物扩散的速率控制屏障,约厚(10-20mm),表面层是高度疏水的。它是由死的、扁平的、富含角蛋白的细胞,即角膜细胞组成的。这些致密的细胞被细胞间脂质的复杂混合物包围。它们包括神经酰胺、游离脂肪酸、胆固醇和胆固醇硫酸盐。它们最重要的特征是它们被构造成有序的双层阵列。分子穿过角质层的主要扩散途径是细胞间的,扩散剂需遵循一条曲折的路线,必须依次并重复地穿过许多亲水性和亲脂性结构域[5]。因此,透皮给药的候选药物具有三个共同特点:相对低剂量的有效性、分子质量小于400 Da和亲脂性。从透皮贴剂递送的药物通常在数小时的延迟时间内达到治疗性血浆水平。
通常来讲,评估局部给药的可行性更加困难,因为治疗效果所需的皮肤水平通常是未知的。对于经皮给药,一般有一个充分记录和可确定的终点,即有效治疗所需的血浆水平。
2、透皮给药系统的概述和组成
经皮递送系统(TDS)设计用于将活性成分(药物)递送穿过皮肤并进入全身循环,而局部递送系统设计为将活性成分递送至局部组织。透皮贴剂一般由背衬层、药物层、促渗层、压敏胶和保护层等数层组成,TDS可大致分为骨架型和液体或凝胶储库型递送系统。
骨架型TDS含有一种或多种活性成分,其溶解或部分悬浮在各种成分的混合物中,包括粘合剂、促渗透剂、柔软剂和防腐剂,通常使用溶剂、水凝胶或热熔法制造。骨架型TDS的示例如图2所示,但骨架型TDS可能还包括额外的层和/或更复杂的设计。
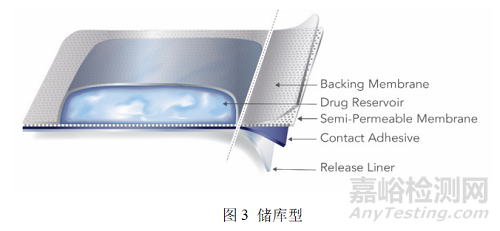
储库型TDS类似地包含各种液体或半固体形式的组分,储库型TDS利用热密封区域将活性物质凝胶保留在背衬膜和微孔膜之间。储库类型TDS的示例如图3所示。由于储库TDS固有的故障模式和安全风险,FDA建议TDS制造商和申请人将制剂开发工作重点放在骨架型TDS上[1]。
3、国内外批准的药物
目前国内已经获批上市的透皮贴剂类药物的适应症主要集中在精神神经和抗炎镇痛等领域,下表1和表2罗列了部分国内外申报及获批的透皮贴剂类品种[6]。
目前国内批准的局部起效的贴剂类药物主要集中在局部镇痛等领域,包括:氟比洛芬凝胶贴膏,洛索洛芬钠贴剂,酮洛芬贴剂,吲哚美辛巴布膏等。
4、处方和工艺研究
透皮贴剂中原辅料的选择对其质量有直接的影响。所以在原辅料的选择上,应对其生产工艺和质量特性做较为深入的探究,有助于最制剂的质量和稳定性有更好的控制。
4.1 处方组成
通常透皮给药的候选药物具有三个共同特点:相对低剂量的有效性、分子质量小于400 Da和亲脂性。基于这些特点,可以选择油/水分配系数大、脂溶性好,熔点低,与此同时,要求药物在水和油中的溶解度最好在1mg/mL以上,作为合适的药物。确定活性成分之后,还要考察活性分子和辅料之间的相互作用,是否对药物的透皮过程有影响。常规的透皮制剂处方中除了原料药,还包括10余种辅料,包括黏合剂(又叫压敏胶,是透皮贴剂的关键辅料),以及交联剂、保湿剂、增粘剂、赋形剂、促渗剂、表面活性剂和抑菌剂等组成[7]。根据不同类型的透皮贴剂,选择合适的辅料添加,还要考虑到最终药物制剂的粘附性,药物渗透性,以及对皮肤的刺激性等影响。开展合适的辅料间相互作用试验以及体外渗透性等试验,是制剂处方开发过程中不可缺少的步骤。FDA建议,为更好的把控在整个产品生命周期中所购进原辅料的质量均一性,应对原辅料的关键质量属性予以识别、评估和适当控制[8]。
4.2 工艺研究
透皮贴剂的制备工艺主要是将原料药和交联剂等固体或液体物料溶于适当的溶剂中,再与其他的辅料,如压敏胶、促渗剂等混合均匀后涂布于保护层,干燥后固化成型,复合层压,裁切和包装,最后密封保存。其中药物应先溶解后再加入,对于难溶性物质可分散在成膜体系中,加入增溶剂或制备为脂质体等。
在批量放大过程中,尤其要注意处方工艺与生产线等均有可能随着批量变化而发生调整,这些微调整极有可能对体外释放以及药物在皮肤的渗透和粘附性产生较大影响,所以建议在对放大生产应进行全面的评估。
5、临床试验要求
透皮贴剂类药物的临床研究方法,根据其吸收特征,包括体内药代动力学方法、药效学方法、临床终点方法、皮肤PK研究方法、体外终点研究方法以及豁免情形。在全球范围内,美国、欧盟、日本和加拿大均专门针对局部用药发布了研究指南,在颁布的每一个指南中,均详细的描述了基于药物特点,作用部位、给药剂型等具体的临床研究方法。
目前国内的大部分透皮贴剂类,可以全身入血的药物,主要集中在仿制药类型,可以参考《以药动学参数为终点评价指标的化学药物仿制药人体生物等效性研究技术指导原则》,通过生物等效性试验,并结合贴剂的自身特点,同步开展粘附性,皮肤刺激性以及药物残留等研究,申请在国内获批上市。
对于局部给药局部起效的透皮贴剂类药物,可以参考《局部给药局部起效药物临床试验技术指导原则》,根据创新药和仿制药的不同类型,需要结合药物的处方组成、剂型、给药装置、非临床药代动力学、药效动力学及毒性等特征进行综合考虑,开展不同的临床试验来满足上市需求。其中,临床终点生物等效性研究是目前评价局部用药的生物等效性的最为常用,也是FDA比较认可的研究方法。该方法是根据在患者中证明安全性和有效性等效,确定两种制剂生物等效。
6、展望
透皮给药系统安全可控,并结合自身的优势和特点,成为了医药行业广大科研人员的研究热点,同时也为患者提供了一种新的治疗选择。透皮给药作为一种特殊复杂的给药途径,从传统的中药橡皮膏开始到运用现代制剂工艺的多种贴剂剂型,给患者的疾病治疗与健康管理提供了很好的平台技术。通过这一平台技术,结合中药,化学药物,生物药,向人们提供了慢性疾病管理宽广的运用前景。相信随着医药水平的不断提高,贴剂使用材料的进展与突破,人们认识程度的加深和开发力度的加强,透皮贴剂为疾病治疗带来突破性的进展。