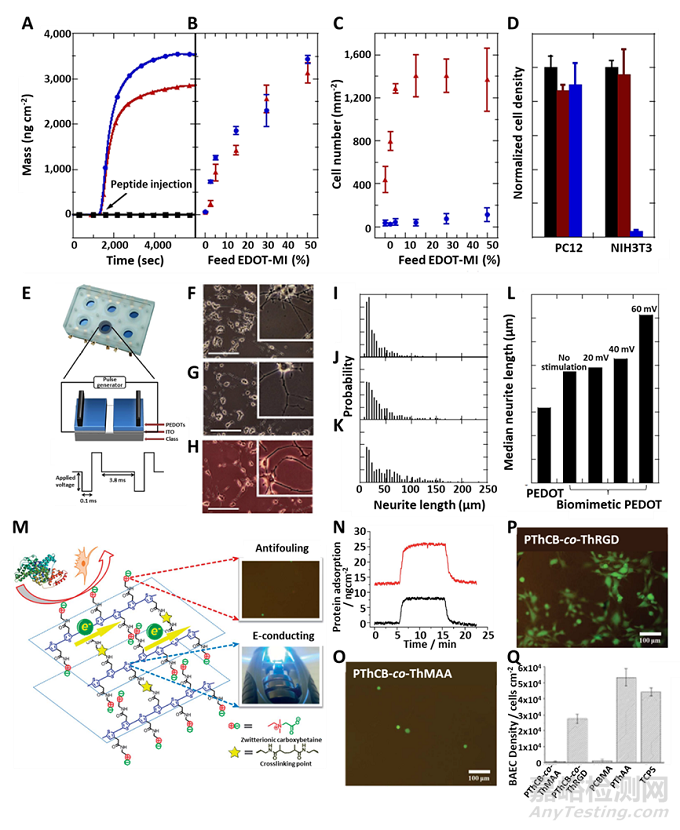
近期,上海大学朱波教授和东华大学何勇教授在科爱创办的期刊Bioactive Materials上联合发表综述文章:用于生物电子亲密电耦合且抗炎症反应的功能化导电高分子的最新进展。本文从导电高分子在生物电子器件领域的重要优势:具有优异的混合离子-电子导电性,可调谐的金属界面势垒,组织匹配的柔软性以及可化学改性出发,详细总结了化学改性的导电高分子在制造长期生物电子植入物,解决慢性免疫反应方面的研究进展,并指出化学改性的导电高分子与神经元的相互作用弱以及在长期电通信稳定性差的问题。进而,重点介绍了两性离子导电高分子在生物电子植入器件中的应用进展,并对其在选择性神经偶联和可再植入功能方面的进展进行了综述。最后,对两性离子导电高分子在体内生物电子器件中的应用前景进行了展望。
研究内容简介
生物电子植入器件已广泛应用于神经假体、脑机接口和其他生物集成设备来进行检测和记录生物信号。然而目前商业植入电极,由金属或硅制成,这些材料的刚性性质,使得电极和组织之间的机械性能不匹配,导致异物反应甚至器件故障。且这些电极材料的表面可能通过非特异性相互作用吸附蛋白质,触发异物反应。此外,这类材料表现为化学惰性,难以与生物分子之间形成稳定的相互作用。
导电高分子(CPs)具有优于无机材料和金属材料的优点:1.CPs的弹性模量远低于无机材料和金属材料,从而最大限度地减少了机械失配,减少了设备-组织界面处的应力集中。2.将CPs涂覆在电极上,通过显著降低整体设备阻抗,显著改善了体外和体内组织记录部位的电偶联。且CP电极由于其巨大的体积电容,为生物安全刺激也提供了高电荷存储和注入能力。3.生物分子改性的CPs能够增强与神经元界面的相互作用并减少炎症反应。然而,生物分子的表面修饰通常不能解决非特异性蛋白质吸附问题。这将增加界面阻抗,甚至引发免疫反应。
最近,两性离子CPs在减少非特异性细胞/蛋白质相互作用方面表现突出,并能在低阻抗下实现与细胞/组织有效电通信。两性离子CPs除了具有CPs的混合离子-电子电导率外,其两性离子成分还增强的离子电导率和金属-导电高分子的电偶联,进一步促进电极与细胞/组织之间的电荷转移。两性离子CPs与其他亲水性CPs相比,在防污、水稳定性、低炎症和电化学性能方面也具有优势,并已广泛应用于体内和体外生物电子器件中。此外,两性离子CPs可以通过耦合的细胞识别分子为细胞提供附着点。鉴于这些优势,两性离子CPs有望解决上述导电高分子的局限性。
图1. 本综述的思路
一、生物电子器件用CPs
CPs由于具有柔软性、优异的电化学特性和可表面生物功能修饰被认为是下一代人工耳蜗植入物、神经探针、仿生眼和脑机接口的替代材料。
1.1 CPs的生物相容性和柔性
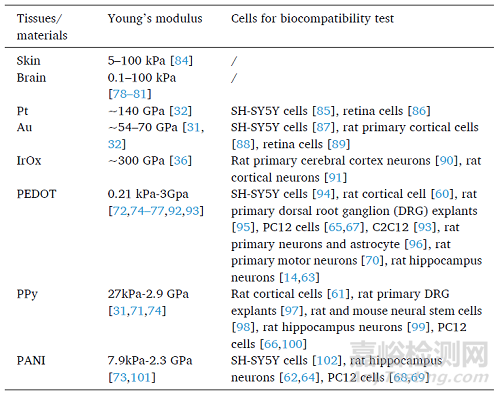
电子材料的生物相容性是生物电子植入物在复杂生物条件下发挥作用的关键因素之一。CPs已被证实与神经细胞系兼容,如皮质细胞、海马神经元、PC12细胞和运动神经元等。此外,由于CPs的弹性模量比较小,用作可植入电极的涂层可以作为软组织和硬质金属之间的缓冲层,显著降低神经植入物的界面机械应力,显著提高可植入装置的性能和寿命。
表1 总结了导电材料的杨氏模量和生物相容性
1.2 CPs的电学性能
1.2.1 CPs的混合离子-电子电导率
CPs同时传导离子和电子载流子,从而使得CPs具有较高的离子电导率和电容。生物电子器件的电荷传输主要涉及四个过程:1.CP/电解质界面的掺杂离子传输,2.CP内部通过掺杂离子(阴离子)来平衡电子载流子(空穴),3.电子载流子跳跃,4.金属电极与CP之间的电荷转移。在电荷输运过程中,离子与电子传导的相互作用对导电高分子器件的运行起着至关重要的作用。因此,在电子和离子电导率之间进行权衡通常是优化电子器件性能所必需的。本综述仅简要介绍了CPs的离子-电子相互作用和耦合输运性质,以帮助读者理解CP的导电性。
1.2.2 CPs的低阻抗性能
为了使神经电极具有高信噪比和高空间分辨率,需要小尺寸和低阻抗的电极。在神经电极上沉积CPs可实现小尺寸微电极具有大的电极电容和低的阻抗。许多研究证实,与IrOx、铂、金和ITO等传统电极材料相比,CPs在1 kHz时的电化学阻抗要低得多。当CPs作为神经电极时,它们的低阻抗抑制了电噪声,减少了信号损失,产生更明显的神经网络反应。CPs阻抗的大幅降低主要归功于其独特的混合离子-电子导电性,这有助于电极衬底和电解质之间的电耦合,促进离子或电子载流子的界面交换。
1.2.3金属-导电高分子的界面作用
CPs与金属的界面对CPs电极至关重要,因为它决定了CPs与金属的接触是欧姆接触还是整流接触。金属和半导体层之间良好的欧姆接触对于通过界面注入高密度电流和制造高性能半导体器件至关重要。CP和金属的功函数的差异在它们之间建立了热力学平衡和界面势垒(肖特基势垒)。p型CPs可以帮助实现与高功函数金属的欧姆接触。并且通过改变CPs的化学结构来降低界面势垒。此外,增加p型CPs的掺杂水平可以进一步有利于CPs与金属之间形成良好的欧姆接触。此外,金属和CPs在遇到水分子时会改变它们的功函数。因此,仍然需要进一步地研究水对CP/金属界面的影响。
1.3 生物功能化CPs
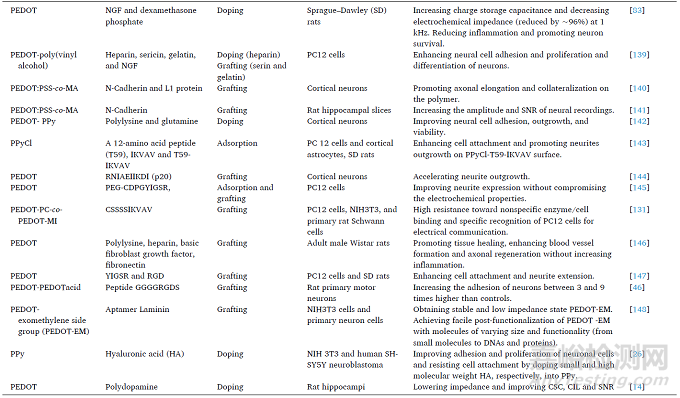
在生物系统中工作时,电极的性能经常随着时间的推移而下降,其主要与植入物诱导的炎症反应有关。异物反应可能造成神经胶质瘢痕形成,导致神经探针周围形成致密的细胞鞘,并将电极与附近的神经元隔离开来。在这种情况下,从电极到神经细胞/组织的电荷转移将受到阻碍,导致记录电信号的强度减弱和质量降低。在目标神经元和电极之间建立选择性相互作用可以抑制组织反应,从而可以提高记录质量和慢性电极性能。将生物分子与CPs结合在一起,可以保证电极与神经元之间的紧密电偶联,促进神经元的增殖和分化,提高神经记录的质量。目前,神经营养因子、细胞粘附生物分子(聚赖氨酸、钙粘蛋白、YIGSR和IKVAV多肽)以及其他一些亲水性生物分子,如透明质酸、硫酸软骨素和硫酸葡聚糖等已广泛应用于CPs神经电极。
表2 总结了生物功能化CPs的相关研究成果
虽然生物功能化方法可以有效地增强CPs与神经元的相互作用,但在生物功能化CPs植入器件植入后仍然诱导炎症反应。因此,常采用抗炎药掺杂到CPs中来减轻早期植入器件的炎症反应。
1.4生物功能化导电聚合物的挑战
生物功能化CPs作为植入式材料仍有几个关键性问题尚未解决。
首先,制备生物分子功能化CPs的方法存在局限性。物理吸附和分子包埋的方法无法控制生物分子的数量。化学偶联的方法会使得CPs的导电性受到损害,生物分子的活性也可能会在化学反应中受损。
其次,虽然生物分子修饰方法可以提高CPs电极的生物相容性,但可能会影响CPs的机械、电化学、稳定性和生物学特性。
此外,生物分子功能化的CPs不能阻止长期植入的胶质瘢痕的形成。
二、生物电子器件用两性离子CPs
2.1两性离子CPs
防污CPs具有抵抗非特异性蛋白质/细胞相互作用和抑制免疫反应的潜力。这些防污CPs的共同结构特征是它们接枝亲水性基团或聚合物。根据化学结构的不同,开发了三种主要的生物电子防污CPs。第一种是低聚乙二醇(OEG)或聚乙二醇(PEG)功能化CPs,它们是最早报道的防污CPs。第二种是两性离子功能化的CPs,它们由两性离子基团或具有相同数量的相反电荷基团的聚合物链接枝。两性离子基团和两性离子聚合物通常具有很强的亲水性和中性电荷,这有助于CPs阻止蛋白质/细胞通过非特异性相互作用(包括疏水-疏水,静电,偶极-偶极或范德华相互作用)接近其表面。第三种是亲水生物分子修饰的CPs,如亲水肽和植酸也被用于功能化具有防污性能的CPs。
PEG或OEG功能化的CPs易受氧化降解,而且具有免疫原性,不适用于长期植入器件。研究表明两性离子聚合物在化学上更稳定,防污性能更优越。其中磷酸胆碱(PC)、磺胺甜菜碱(SB)和羧基甜菜碱(CB)是最常用的用于CPs功能化的两性离子。本综述我们重点研究了两性离子CPs的合成、性质及其生物电子应用。
2.2两性离子导电聚合物的防污性能
2.2.1两性离子的水合作用
防污界面的水合作用对细胞/蛋白质的抗性至关重要。两性离子修饰界面上形成的水化层来源于离子相互作用。这使得水化层比在PEG/OEG修饰的界面上形成的水化层更加致密和稳定。靠近两性离子表面的水分子的迁移率降低,偶极子取向分布更宽,停留时间更长。因此,两性离子聚合物强烈排斥蛋白质的非特异性吸附。
2.2.2 pH、间隔长度、组成、化学结构效应
三种常用两性离子CPs都有相同的带正电的单位,即铵基,但带负电的结构单元不同。它们带负电单元的不同会导致不同的表面电荷,从而在相同的酸环境下产生不同的防污性能。此外,由于两性离子结构的不同,其阴阳离子的电荷密度也不同,从而会影响两性离子的自缔合性,影响其结构的稳定性。两性离子中两个带相反电荷基团之间的距离也会影响两性离子聚合物的防污性能。聚合物组成对CPs抵抗蛋白质/细胞粘附性能也会产生比较大的影响。
2.3 两性离子导电聚合物的低阻抗
2.3.1离子电导率增强
对于生物电子植入物,电极的低阻抗是确保其与细胞/组织有效电偶联的关键。高阻抗通常会导致神经记录中的噪声增加和信号丢失。此外,植入器件需要具备高CSC和CIC从而防止组织/细胞在高电位下被电化学副反应损伤。研究表明,两性离子功能化的CPs,其阻抗与未功能化的导电高分子相同或者甚至更低。其可能的原因是两性离子增强了离子电导率。此外,两性离子修饰的CPs电极,其CSC和CIC值高于OEG功能化的CPs电极。这应该是由于与非离子低聚物(乙二醇)相比,两性离子促进了离子的解离和运输。
图1. 两性离子增强离子电导率
2.3.2金属与两性离子CPs的界面
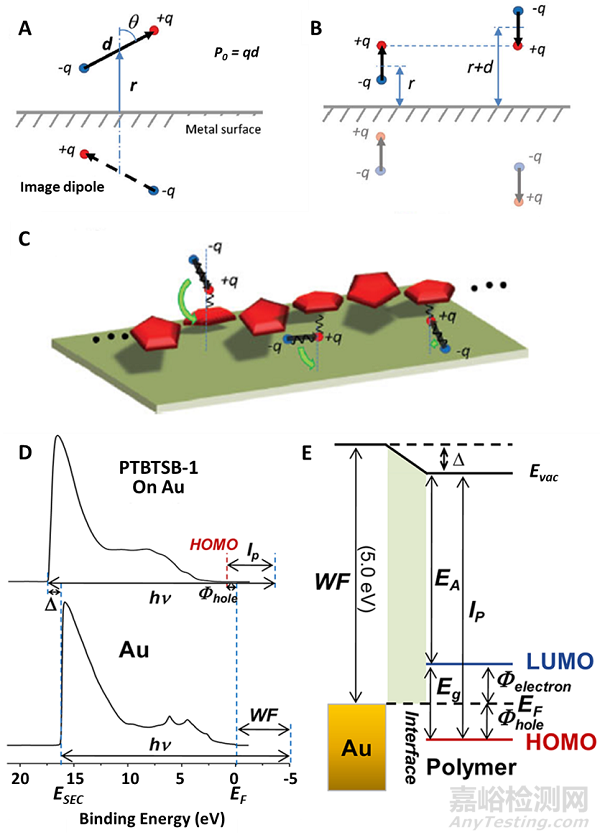
两性离子CPs涂层电极由多层结构组成,其中两性离子聚合物直接与金属接触,并作为金属和水性缓冲液之间的界面层。两性离子不能迁移,在金属附近表现出很强的偶极子。当在金属表面涂覆一层两性离子共轭聚合物时,由于界面偶极子的存在,两性离子悬垂的基团会显著改变金属电极的功函数。
图2. 两性离子CPs改变金属电极的功函数
2.3.3两性离子结构及间隔长度
对于两性离子CPs来说,两性离子结构以及主链与两性离子之间的间隔对两性离子CPs的电化学性能起着至关重要的作用。研究发现,PC功能化的PEDOT与SB、CB修饰的PEDOT相比具有最低的阻抗和最高的电容。此外,增加两性离子与主链间的间隔,并不会影响两性离子CPs抵抗蛋白的粘附能力。然而,随着间隔的增加,CPs的界面阻抗显著降低。
2.4两性离子CPs的生物电子学应用
赋予植入器件防污性能是减少植入物诱导炎症的有效方法。许多研究证实两性离子聚合物涂层可以显著提高种植入器件的抗炎症、抗感染和抗增生性能。
两性离子CPs制备的电极具有低阻抗、大电荷存储容量和高电荷注入能力,植入后能很好地保持良好的灵敏度和反应率,并在植入后电极可以抑制疤痕组织形成。这些结果为两性离子CPs在生物电子植入物中的应用提供了广阔的前景。抗炎症和低阻抗的独特结合使两性离子导电聚合物有望成为长期的生物电子植入物。
图3. PEDOT-PC/碳纤维微电极植入后保持高检测灵敏度
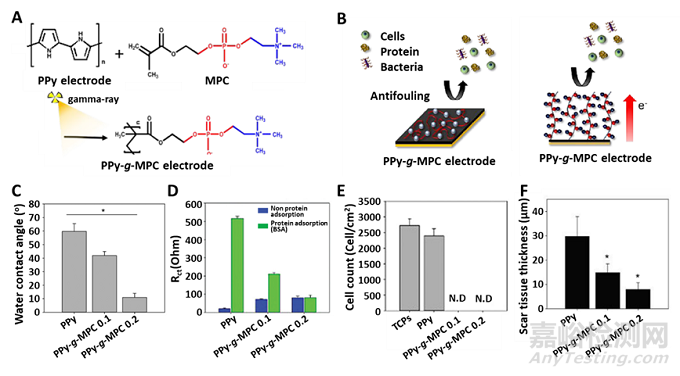
图4. 2-甲基丙烯酰氧乙基磷酸胆碱(MPC)修饰的PPy电极实现抗非特异性黏附及抑制疤痕组织
此外,通过在两性离子CPs上构建神经细胞/组织耦合位点,能够实现电极与生物分子或神经细胞/组织相互作用,同时保持两性离子电极的防污特性。两性离子CPs与神经特异性肽结合能够实现与神经元稳定而密切的相互作用。
图5. IKVAV多肽与两性离子CPs结合实现与神经细胞的特异性粘附
目前,临床实验中,植入器件停止功能或治疗完成后,往往面临着重新植入或移除的问题。然而,器件的再植入比最初的植入更复杂,因为第二次手术可能会导致组织损伤,并削弱再植入后的身体功能。研究者通过模拟自然界整合素-细胞外基质的动态相互作用,开发了一种动态两性离子EDOT共聚物,可实现可控地控制细胞的粘附和释放。
图6.一种动态控制细胞粘附和释放的两性离子聚合物
三、结果和展望
未来的电子植入电子器件应该具有抑制炎症反应,高信噪比,并能与神经元紧密电偶联。生物功能化CPs已被广泛用于修改神经元-电极相互作用或调节表面免疫反应。两性离子CPs具有优异的电化学性能,且能显著抑制疤痕组织的形成,保持器件灵敏度。
然而,为了开发一种可长期应用的生物电子植入器件,几个关键问题仍有待解决。首先,两性离子CP电极在脑内的长期植入需要进一步探索。其次,了解两性离子如何调节混合离子-电子传输以及CP-金属和CP-水界面的电荷传输,对组织电偶联植入器件至关重要。第三,开发化学方法来制备可溶性两性离子CPs将使制造电极植入器件具有成本效益。此外,将生物功能化的CPs与两性离子CPs结合,有望与植入器件的目标神经细胞/组织形成紧密的选择性电偶联。进一步在体内验证和优化这种方法将使生物电子植入器件在大脑中长期稳定地发挥作用。两性离子CPs与生物分子的结合将赋予生物电子植入物抑制炎症的特性,并同时促进与神经细胞/组织在低阻抗下的紧密电偶联,显著推进神经细胞/组织的长期监测、刺激和记录。
原文信息
Sihao Qian,‡ Hsing-An Lin,‡ Qichao Pan, Shuhua Zhang, Yunhua Zhang, Zhi Geng, Qing Wu, Yong He,* Bo Zhu*.
Chemically revised conducting polymers with inflammation resistance for intimate bioelectronic electrocoupling.
Bioactive Materials, 26 (2023) 24-51.