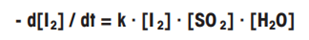对药品的质量控制非常重要,测定其中水分含量也是一个重要的环节。水分的多少会影响药品的贮存期限,药品中的水分增加,水解和氧化等化学反应就会加速,水分的研究是稳定性研究中很重要的部分,药品中水分含量的异常会影响药品的质量和功效,尤其是对于抗生素类药品。监控生产过程:不同生产步骤中药品的水分含量有不同要求,通过测定可以监督生产是否规范。因此,药品中水分测定对于药品质量控制、稳定性、药效、生产过程和研发过程都非常重要。
本文从实验的多个方面对卡尔费休水分测定方法进行了总结和概括。
1、卡尔费休化学反应概述
水分测定基于R.W.Bunsen[1]描述的反应:
卡尔费休发现了此反应可以在含有过量二氧化硫的无水环境中测定水分含量。实验证明甲醇是合适的溶剂。为了让反应平衡向右边进行,必须中和反应过程中产生的酸(HI和H2SO4)。卡尔费休用吡啶实现这

根据上述反应式可见,甲醇不仅作为溶剂,并且直接参与反应。在醇溶液中,碘和水按1:1反应。在无醇溶液中,碘和水按1:2反应:
J.C.Verhoff和E.Barenrecht[3]对卡尔费休反应进一步研究表明:
•吡啶并没有直接参与反应,即:吡啶仅作为缓冲剂,并且可以被其他碱代替。
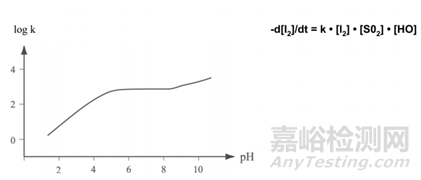
•卡尔费休反应速率k取决于介质的pH值。
pH和反应速率的这种关系的一种解释是:它并非由于在水的影响下被碘氧化的二氧化硫本身,而是由于二氧化硫和甲醇反应形成的甲基亚硫酸根离子。二氧化硫和甲醇的反应如下:
溶液的pH值越高,就有更多的质子被捕捉而形成更多的甲基亚硫酸根离子,卡尔费休反应的速度就越快。当pH介于5.5至8之间时,所有的二氧化硫均可反应形成甲基亚硫酸盐,此时反应速率最大。当pH于8.5时,由于碘和氢氧根或甲基化离子之间的反应,反应速率会增大,但这将导致终点消失,并消耗更多的碘。
在这些理论的基础上E.Scholz[4]采用咪唑作为碱的无吡啶卡尔费休试剂。这种试剂不仅代替了有毒有刺激性气味的含吡啶试剂,而且使反应更快、更精确,因为咪唑较吡啶的pH缓冲能力更强。E.Scholz研究的结果按卡尔费休反应最终产生了以下反应式:
这样就有了通用的化学平衡式:
E.Scholz的化学分析还揭示了乙醇、异丙醇、甲氧基乙醇等[5]够提高试剂滴定度稳定性的醇类物质也可以代替甲醇。
2、容量法和库仑法
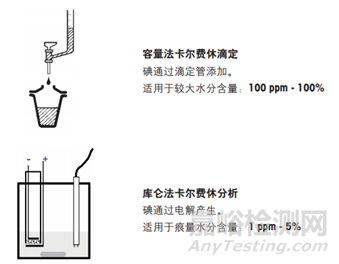
容量法:含碘的溶液通过活塞驱动的滴定管添加;库仑法:碘由杯中的电解电极产生。根据水分的预估量选择不同的测定方法。
2.1 容量法试剂汇总
2.1.1 单组分卡尔费休试剂
滴定剂含有碘、二氧化硫、咪唑,溶于醇溶液。溶剂是甲醇,也可以使用适合于样品的混合甲醇溶剂。
试剂大约可以存储两年。试剂若保存在密封瓶中,滴定度大约以每年0.5mg/mL的速度下降。
2.1.2 双组分卡尔费休试剂
滴定剂含有碘和甲醇。溶剂含有二氧化硫、咪唑和甲醇。
双组分试剂能使滴定速度快至原先的二至三倍。双组份试剂的滴定剂和溶剂在存储时均极为稳定。如果滴定剂瓶密封性好,其滴定度也是比较稳定的,
2.1.3 含吡啶试剂
除确保快速精确进行卡尔费休滴定的无吡啶试剂外,含吡啶的试剂因其价格低廉及生产工艺简单而仍然广泛应用。
2.1.4 醛酮专用试剂
醛(RCHO)和酮(RCOR)与通常的含甲醇试剂反应生成缩醛和缩酮,反应中产生的水同时被滴定,从而导致水分含量升高甚至终点消失,因此有了不含甲醇的单组分试剂解决这个问题,醛酮专用试剂的滴定时间比常规卡尔费休试剂稍长。注意可能需要在滴定方法中调整终点值以适应这些试剂。此专用试剂还适合胺等与甲醇反应的物质。
2.1.5 含乙醇的卡尔费休试剂
由于乙醇比甲醇毒性低,1998年上市了含乙醇的双组分卡尔费休试剂。因为酮在乙醇中形成缩酮的速度远比在甲醇中形成的速度慢,这些试剂也可用于酮的滴定。
2.2 库仑法滴定用的试剂和溶剂
为测得全部含水量,样品必须完全溶解在阳极液中,如果样品不完全溶解,即会形成乳浊液,这样部分含水量就无法测得,因此测得的结果低于样品的实际含水量,此种情况下阳极液必须马上更换。
阳极液分很多种,用于溶解不同类型的样品。另外,阳极液中还可以加入多种辅助溶剂。
2.2.1溶于甲醇或乙醇的样品
烃(至C10)、卤代烃(至C10)、醇、醚、酯、硝基化合物、乙酰胺等。
2.2.2微溶于甲醇或乙醇的样品
醚油、食用油、膏药、烃(C10至C20)等。
可以在阳极液中加入辛醇或己醇,增加样品的溶解性,但最多不能超过总体积的30%,以免电导率太低。
2.2.3不溶于甲醇或乙醇的样品
石油、变压器油、硅油、烃(高于C20)等。
必须在阳极液中加入氯仿,以增加样品的溶解性,但最多不能超过总体积的30%,以免电导率太低。
2.2.4 醛酮类样品
酮和醛与甲醇反应,形成缩醛或缩酮,并产生水。这类样品必须使用无甲醇的专用试剂。
测定酮类样品时需注意:
Ø从常规试剂更换成醛酮类试剂时,整个滴定杯必须彻底清洗,因为即便是微量甲醇也会导致严重的干扰。
Ø如果需要经常测试酮类样品,建议再购买一个滴定杯专用于酮类测试。
Ø如果已经滴定了许多酮类样品,漂移值会因为缓慢的副反应而逐渐增大。在待机较长时间后,阳极液有可能会在几天后消耗殆尽,即便没有任何样品测定。
Ø选择相对较小的样品量,样品量越大,副反应的作用就越发明显,即样品的漂移逐渐变大以致终点很难测定。
Ø酮专用试剂还适用其他样品。特别需要注意的是,能与酮反应的醇不能在该试剂中滴定。测定醛类样品时需要注意:
Ø短链醛(如乙酰胺)在阳极氧化并产生水,库仑法不能用,但可以用容量法测定。
Ø芳香醛(如苯甲醛)也可以用库仑法测定。需要注意的是,二硫化物与芳香醛的加成反应非常强烈,因此需要等二硫化物反向分解的反应发生后才终止滴定(以确保漂移值降至初始值)。
12.4.5 对于酸和碱(pH值)
如果滴定曲线噪音大或终点迟迟不能出现,则说明pH值出现偏移。这时需要测定阳极液的pH值。
用缓冲溶液校正过的pH电极测定pH值,从滴定杯中取出1份阳极液,由于电极会带入许多水分,测量过程不能直接在滴定杯中进行。
pH试纸也可以大概了解阳极液的pH值。
尔费休滴定酸性或碱性样品,阳极液的pH值必须控制在5.5〜7。
对于酸性样品,如乙酸、甲酸等:使用咪唑后阳极液的pH值会很高。一般在阳极池中加入大约80 mL阳极液和20 mL HYDRANAL @ buffer。
对于碱性样品,如铵盐:碱性样品必须用水杨酸或苯甲酸中和,一般在阳极池中加入大约90 mL阳极液和5 g水杨酸或苯甲酸。
2.3 容量法的滴定剂
建议每天标定滴定剂的浓度。在一些国家,白天的温度变化比较大,并且实验室没有空调系统,最好2~4小时标定一次滴定剂的浓度。
2.4 库伦法的滴定剂
库仑法滴定测得的水分含量是通过计算用于电解产生碘所消耗的电量(库仑,C)。产生1摩尔化学物质需要的单个电子的数量:96485C。96485C/moL就是法拉第常数。因此反应中1moL水需要2*96485C。水的摩尔质量是18.015g/moL,可以得到:1mg水消耗10.712C电子。
对于电化学优化的卡尔费休滴定池,电流转化产生碘的效率几乎为100%。由于电流和时间都能量化和精确测量,故无需标定库仑法卡尔费休试剂,因此这是一种绝对的方法。因而库仑法卡尔费休分析是一种水分含量测定的参考方法。不过还是建议定期用标准水样品检查库仑仪的状态。
3、卡尔费休反应的影响因素
3.1 速率由PH决定
由于卡尔费休反应的最大速率在5.5到8的pH范围之间,在实际操作过程中应避免pH值小于4和大于8。滴定酸性或碱性样品时,应加入缓冲试剂调节pH值(用咪唑作为碱性缓冲试剂,用水杨酸作为酸性缓冲试剂)。
3.2 样品溶剂
Eberius[6]研究发现溶剂里的甲醇含量大于等于20%时碘和水按1:1的比例反应,因此甲醇的量始终不得少于要求的最低量。如果必须使用不含甲醇的滴定剂(滴定醛和酮),可以选用其他的伯醇,例如乙二醇
|
醇溶液
|
H2O:I2=1:1
|
如:甲醇
|
|
无醇溶液
|
H2O:I2=2:1
|
如:二甲基甲酰胺
|
3.3 水分含量
H2O:I2的摩尔比还受样品含水量的影响。J.C.Verhoff 和E.Barendrecht[7]发现:当水分含量大于1mol/L时滴定度将提高。然而实际操作中并不多见,因为溶剂的含水量微乎其微。
4、方法学验证
4.1 精度和检测限
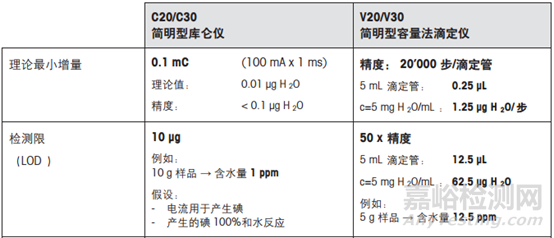
下表显示了基于仪器技术规范可以达到的理论值。
4.2 准确性
准确性不但取决于仪器的技术规范,而且取决于上节提到的所有因素:取样(如需,包括样品存储)、样品预处理;预计水含量和选择适合的仪器;选择最佳样品量;卡尔费休试剂的情况,如新鲜试剂、预滴定、低漂移值;滴定杯和管路的密封性;测量电极的情况;库仑法:电解电极的情况;滴定方法的参数设置等等。
为了测得非常接近样品真实值的结果,必须通过滴定标准水或已知含水量的样品来验证测量。准确度最关键的因素是最佳含水量和样品量,以及优化控制条件。
4.3 重复性
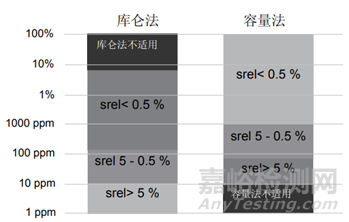
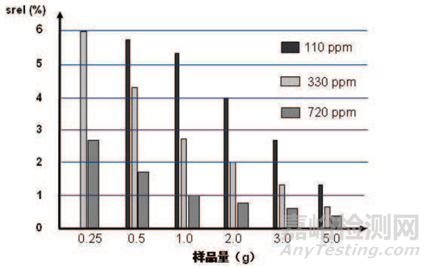
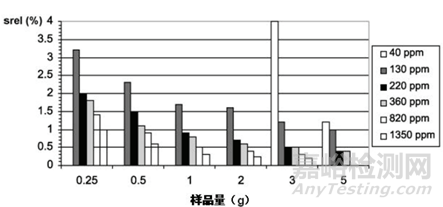
相同样品连续测量得到的结果的接近程度可用相对标准偏差(srel)来表示,以%计。在最佳样品量和优化控制的测试条件下,重复测量可以得到以下结果。图中显示了不同含水量的srel,通常样品系列的重复性会随着含水量的减小而增大。注意含水量小于10 ppm时,建议不要采用容量法滴定。
下图分别是容量法和库伦法不同含水量样品的srel与样品量的函数关系。
上述举例中,相对标准偏差随着样品量的减小而增大,为得到重复性高的结果必须优化样品量。特别对于低含水量的样品,增大样品量是个不错的优化方向。
5、注意事项
5.1 碘的添加或产生速度
碘的添加或产生必须控制,理想的状况是碘的添加或产生越快越好并且在到达终点时刚好停止,然后才可以按所需精度测量滴定剂的消耗或产生碘的量,转换成水的含量。
5.2 卡尔费休反应的速度
卡尔费休反应速度取决于:水的浓度、二氧化硫的浓度、碘的浓度
对于容量法卡尔费休滴定,使用的单组分滴定剂中,加入的二氧化硫仅比碘滴定溶液略微过量。而使用的双组分试剂中,溶剂中的二氧化硫大量过量。这样双组分试剂比单组分试剂的反应速度快2倍,因此卡尔费休滴定使用双组分试剂比使用单组分试剂的反应速度明显更快。
对于库仑法卡尔费休分析,阳极液中二氧化硫大量过量,随着测试样品数目的增加,二氧化硫浓度逐渐下降,因此使用过很长时间的阳极液,其反应速度必然很慢。
5.3 搅拌和样品溶液的混匀速度
混合均匀是卡尔费休滴定快速、准确的必要条件。混合受搅拌速度、滴定剂加入点(容量法)滴定杯形状(容量法)的影响。
当看见明显的漩涡时即达到最佳搅拌速度。如果速度太慢,滴定速度也会很慢并且不稳定或者出现过滴定。如果溶液中产生气泡,则搅拌速度太快了,气泡会干扰测量值。
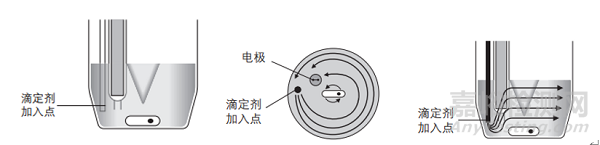
滴定剂加入点滴定剂应该在湍流最大的地方加入可以获得最佳的混合效果。另外加入点应该远离电极以便有充分的反应时间。否则电极直接测量到加入的碘分子,将导致滴定速度变慢、滴定时间更长。
锥形的滴定杯和短的搅拌棒可以在滴定剂加入点处形成湍流而使滴定剂充分分散。这将加快反应速度,使滴定时间缩短。
如果搅拌棒过长,不会形成湍流,而分散效果也会减弱。碘不会分散到溶液的上层,而在底部聚集被电极直接测量到。
5.4 工作环境
空气湿度是导致卡尔费休滴定出现误差的最主要因素。湿气可以进入样品、滴定剂和滴定台。大多数的空调系统仅仅可以冷却空气,但不能吸收更多的湿气,所以,空调系统应该配有水分冷凝器。卡尔费休滴定仪的安装位置不能距空调太近!
5.5 滴定系统
滴定系统必须尽可能的密封,防止空气中的水分进入。首次安装滴定台时,滴定杯的玻璃表面和内置部件均会附着水分,滴定杯内部的空气也会有水分。
然而,有时预定至无水状态后漂移值仍然很高,原因是玻璃表面和内部空气中的水分缓慢地扩散到阳极液(溶剂)内,可能要持续1〜3小时。可以通过缓慢地摇晃滴定杯,带动内部液体形成漩涡来吸收附着在玻璃表面上的水分,将总的水分快速滴定。但注意摇晃不要太用力,防止溶剂溅出。
干燥剂可以吸收水分防止水分进入滴定杯,但干燥剂的干燥能力是有限的,这取决于空气的湿度,一般可以持续2~4周(通过硅胶颜色变化指示)。
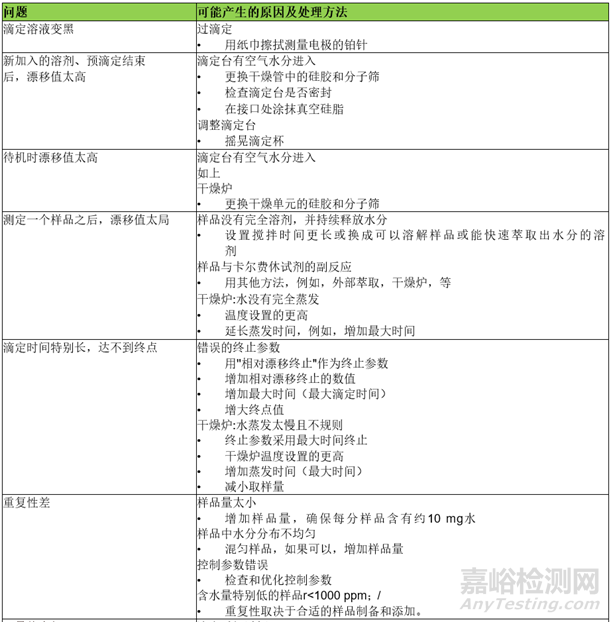
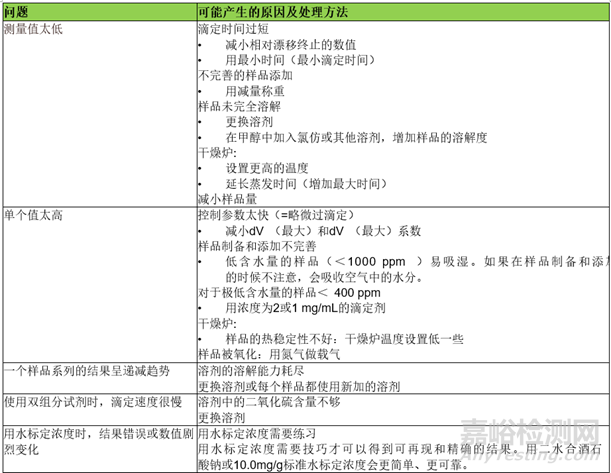
6、故障处理
6.1 库仑法
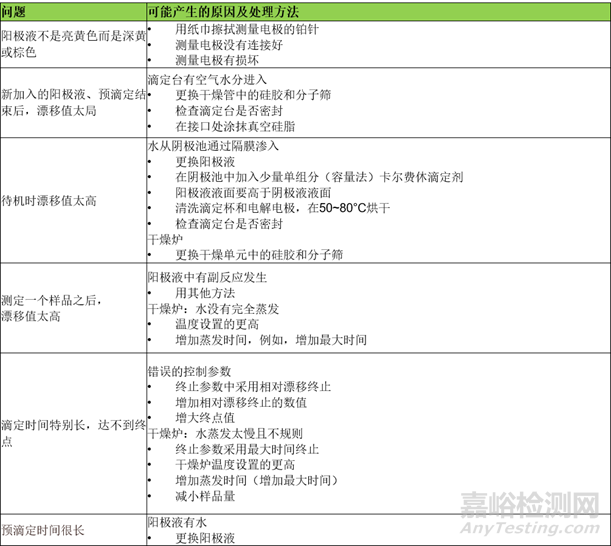

6.2 容量法
7、参考文献
[1]BUNSEN,R.W.,LiebigsAnn.Chem.86,265(1853).
[2]SMITH,.M.;.M.BRYANT;.MITCHELLjr.z''AnalyticalProceduresEmployingKarlFischerReagentI.
[3]VERHOFF,J.C.;E.BARENDRECHT,MechanismandreactionrateoftheKarlFischertitrationreaction.PartI.Potentiometricmeasurements",
[4]SCHOLZ.E.z"KarlFischerReagentienohnePyridin\FreseniusZ.Anal.Chem.303z203207(1980).
[5]GRUNKE,S.;WUNSCH,G.z.KineticsandstoichiometryintheKarlFischersolution",FreseniusJ.Anal.Chem368,139147(2000).
[6]EBERIUS,E.zZ/WasserbestimmungmitKarlFischerLosung\1.Auflage,erlagChemieWeinheim(1954)/(inGerman).
[7]VERHOFF,J.C.;E.BARENDRECHT,''MechanismandreactionrateoftheKarlFischertitrationreaction.PartI.Potentiometricmeasurements"