今日头条
璧辰BRAF抑制剂获胶质瘤孤儿药资格。FDA授予璧辰医药自主研发的小分子BRAF抑制剂ABM-1310孤儿药资格,用于治疗BRAF V600突变的脑胶质母细胞瘤 (GBM)。ABM-1310具有高选择性和高血脑屏障通透性,已在中美两国针对BRAF V600突变晚期实体肿瘤(包括GBM和其他脑胶质瘤等原发性脑肿瘤)的Ⅰ期临床中显示出良好的抗癌疗效,且安全性、耐受性良好。详细数据已在2023ASCO年会上公开。
国内药讯
1.辉瑞PDE-4抑制剂新适应症中国获批。辉瑞非甾体类抗炎药克立硼罗乳膏(商品名:舒坦明 )获国家药监局批准新适应症,推测用于3个月及以上儿童和成人特应性皮炎患者。克立硼罗是Anacor公司(已被辉瑞收购)开发的一款小分子非激素磷酸二酯酶4(PDE-4)抑制剂,该产品已在2020年7月获批中国上市,用于治疗2岁及以上的轻重度特应性皮炎患者。
2.绿叶罗替高汀缓释微球报帕金森NDA。绿叶制药注射用罗替高汀缓释微球(LY03003)的上市申请获CDE受理并获CDE拟纳入优先审评,用于帕金森病的治疗。LY03003是一款可产生持续性多巴胺能刺激(CDS)的周制剂,在人体内的稳定释放能够减轻帕金森患者药物治疗易出现的“开关”效应,显著改善晚期帕金森病患者易出现的运动并发症,有望推迟运动并发症的产生。目前,该产品也在美国和日本同步开发。
3.诺华VEGF单抗中国报眼科NDA。诺华新一代VEGF单抗brolucizumab(布西珠单抗,RTH258)的上市申请获CDE受理。此前该产品已在中国糖尿病性黄斑水肿(DME)患者中完成一项Ⅲ期试验。Brolucizumab可通过抑制VEGF信号通路,进而抑制新生血管病变的增长,清除视网膜水肿并改善患者的视力。该产品已在海外获批用于治疗湿性年龄相关性黄斑变性(AMD)和糖尿病黄斑水肿(DME)。
4.箕星引进两款老花眼创新药获批Ⅲ期临床。箕星药业从LENZ Therapeutics引进的盐酸醋克利定滴眼液(LNZ100)和醋克利定溴莫尼定滴眼液(LNZ101)在中国治疗老视的Ⅲ期临床申请获CDE批准。该项研究旨在评估LNZ100和LNZ101用于改善中国老视人群近视力的疗效与安全性。去年10月,这两款滴眼液已在治疗老花眼的Ⅱ期临床达到主要终点,使用眼药水1小时后,两组患者的缓解率分别达到71%(p<0.0001)和56%(p<0.0001),显著高于对照组(6%)。
5.齐鲁PD-1/CTLA-4双抗启动肝癌II/III期研究。齐鲁制药PD-1/CTLA-4双抗QL1706登记启动一项II/III期临床(CTR20232313),拟评估QL1706联合用药对比信迪利单抗联合贝伐珠单抗一线治疗晚期肝细胞癌患者的有效性。QL1706可同时抑制PD-1和CTLA-4,并且CTLA-4抗体成分在体内具有更短的清除半衰期,因此该产品既有同时阻断PD-1和CTLA-4的协同作用机制,又降低了CTLA-4抗体产生的毒性。目前,齐鲁制药正在中美同步QL1706的临床开发,适应症包括广泛期小细胞肺癌、结直肠癌等。
6.索元基因疗法获批胶质瘤Ⅱ期临床。索元生物基因疗法DB107获FDA批准开展Ⅱ期临床,拟评估在全新生物标志物DGM7指导下,DB107治疗高级别神经胶质瘤(HGG)的有效性。DB107是一种基于RRV基因治疗平台开发的创新疗法,其包括带有胞嘧啶脱氨酶(CD)的重组逆转录病毒载体(RRV)与5-氟尿嘧啶(5-FU)的前药5-氟胞嘧啶(5-FC)。此前,该产品曾获得FDA及EMA的孤儿药资格,以及FDA授予的突破性疗法认定。
国际药讯
1.第一三共mRNA新冠疫苗在日本获批上市。第一三共针对新冠原始毒株(SARS-CoV-2)的单价疫苗DAICHIRONA®(DS-5670)获日本监管部门批准上市,用于加强接种预防新冠感染。DS-5670是第一三共采用其新型核酸传递技术开发的一款mRNA疫苗,这款疫苗可在2-8°C冷链下分发和和储存。据悉,第一三共还将计划继续推进含有XBB.1的单价疫苗的开发,争取今年年底之前提供含有XBB.1.5的单价疫苗。
2.创新Grb2靶向mRNA疗法Ⅱ期临床积极。Bio-Path公司靶向Grb2 mRNA的反义寡脱氧核苷酸疗法prexigebersen,联合一线疗法(decitabine和venetoclax)治疗急性髓系白血病(AML)的Ⅱ期试验获积极中期数据。在初治患者中,prexigebersen联合治疗的完全缓解率达到86%(n=14),显著高于一线疗法的完全缓解率(62%);在经治患者中,联合治疗较一线疗法显著提高患者的完全缓解率(57%vs21%)。Prexigebersen总体耐受性良好。
3.Vertex第二款糖尿病干细胞疗法上临床。Vertex公司第二款干细胞衍生的全分化胰岛细胞疗法VX-264,在治疗1型糖尿病(T1D)的Ⅰ/Ⅱ期临床首例患者给药。今年6月,该公司已在2023ADA年会上公布其首款胰岛细胞疗法VX-880的早期积极结果,接受VX-880治疗的所有6例患者均显示内源性胰岛素分泌,糖化血红蛋白(HbA1c)检测显示血糖控制改善;其中2例随访超过1年的患者不再依赖外源胰岛素治疗。
4.抗Aβ疫苗Ⅱa期研究见刊柳叶刀子刊。United Neuroscience(UNS)公司开发的抗Aβ疫苗UB-311在治疗轻度阿尔茨海默病(AD)的Ⅱa期临床(V203-AD)积极数据发表于《柳叶刀》子刊eBioMedicine上。结果显示,UB-311具有良好安全性和耐受性;UB-311对淀粉样蛋白-β产生积极的抗体应答,总体应答率达到97%,在研究结束时抗体应答率维持在93%。去年5月,FDA已经授予UB-311用于治疗AD的快速通道指定。
5.CRISPR基因编辑疗法获HIV快速通道资格。Excision公司拟用于功能性治愈慢性1型人类免疫缺陷病毒(HIV-1)感染的CRISPR基因编辑疗法EBT-101获FDA授予快速通道认定。EBT-101利用腺相关病毒 (AAV) 来装载CRISPR-Cas9和两种向导RNA(gRNA),同时靶向HIV基因组内的三个不同位点,通过多次切割切除大部分HIV基因组,最大限度地减少潜在的病毒逃逸。EBT-101目前正在Ⅰ/Ⅱ期临床中评估治疗HIV-1的潜力。
6.辉瑞2023H1总收入310亿美元。辉瑞发布2023年上半年业绩报告,上半年总收入310亿美元(-42%),其中第二季度收入为127亿美元(-54%)。业绩下降主要原因是新冠口服药Paxlovid和新冠疫苗Comirnaty的患者需求下降。Q2收入TOP7分别为抗凝血药物Eliquis(13.8%)、新冠mRNA疫苗Comirnaty(11.7%)、肺炎疫苗Prevnar(10.9%)、乳腺癌药物Ibrance(9.8%)、3款罕见心肌病药物Vyndaqel/Vyndamax/Vynmac(6.1%)、类风湿药Xeljanz(3.7%)、前列腺癌药物Xtandi(2.4%)。
医药热点
1.成都印发改善就医试点方案。7月21日,成都市卫健委、医保局印发《改善就医感受提升患者门诊体验工作试点方案(试行)》,以成都大学附属医院、金牛区-成都大学附属医院、网格化城市医联体成员单位为试点,在七个方面进一步优化门诊服务流程。在延长挂号有效期方面,实行“一次就诊只挂一次号”,延长挂号有效期至主要疾病诊疗行为完成,原则上不超过3天,医疗机构不得重复挂号、重复收费。对于当日不能完成的检查检验项目,免费为患者提供复诊预约服务,解读报告和明确治疗方案无需再次挂号。
2.广州医科大附一院介入医学中心揭牌。近日,广州医科大学附属第一医院介入医学中心正式成立,旨在为各个学科介入技术的发展提供了一个良好的公共平台,有助于实现多学科介入技术交叉融合、协同发展。该中心主任由广州呼吸健康研究院副院长李时悦教授、介入科主任熊斌教授担任,并聘任中国科学院院士、中国医师协会介入医师分会会长、东南大学附属中大医院院长滕皋军教授担任中心首席顾问,中国科学院北京纳米能源与系统研究所研究员李舟为特聘教授。
3.南昌再建一家三甲医院。7月26日,南昌大学第二附属医院与新建区人民政府正式签订合作共建“南昌大学第二附属医院新建医院”协议。这是一家三级甲等医院,位于望悦湖片区敏学路北侧,计划总投资13亿元,占地100.9亩,设计床位765张。目前,项目已经进入有序建设施工中,预计2026年建成。
评审动态
1. CDE新药受理情况(08月02日)
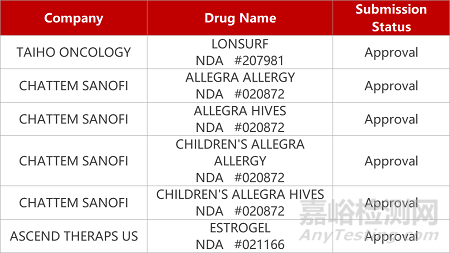
2. FDA新药获批情况(北美08月02日)