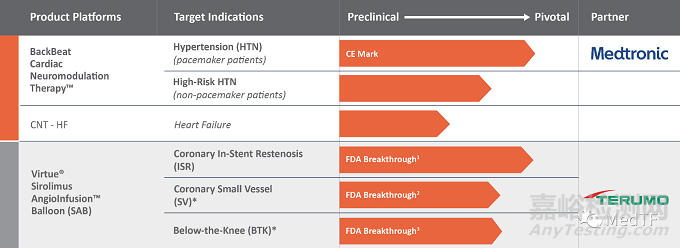
Orchestra BioMed宣布FDA批准其产品Virtue SAB开展IDE研究(Virtute ISR-US),来评估Virtute SAB治疗冠状动脉支架内再狭窄(ISR)患者的有效性和安全性。

FDA之所以能够批准Virtute SAB进行IDE研究,是得到了在欧洲开展的SABRE临床研究结果支持,SABRE是一项针对冠状动脉ISR患者的欧洲多中心、前瞻性、独立核心实验室裁决的临床试验。
Virtute ISR-US是一项随机、前瞻性、双盲、多中心、对照研究,对照组采用普通球囊(POBA)治疗单层冠状动脉ISR。Virtute ISR-US主要疗效和安全性终点是12个月时的靶病变失败(TLF)。该研究将以2:1的比例将300名参与者随机分为Virtute SAB或POBA。与该研究的随机组平行,Orchestra BioMed计划招募一个非随机组,由100名患有双层冠状动脉ISR的参与者组成,接受Virtute SAB治疗。
PI评价
“Virtue SAB的差异化设计,以及SABRE试点研究令人鼓舞的三年临床结果,使其成为冠状动脉疾病适应症的一个潜在的令人信服的治疗选择。这项研究的 IDE 批准代表着朝着生成重要数据以确立 Virtue SAB 的安全性和有效性以及向冠状动脉 ISR 患者推进这种基于西罗莫司的独特疗法的关键一步。”
----Dean J Kereiakes The Christ Hospital Heart & Vascular Institute, Cincinnati
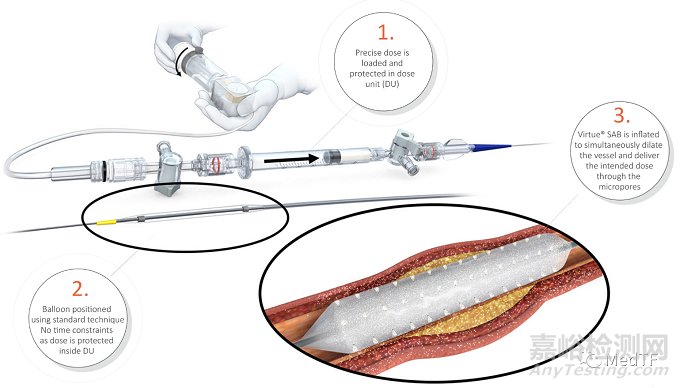
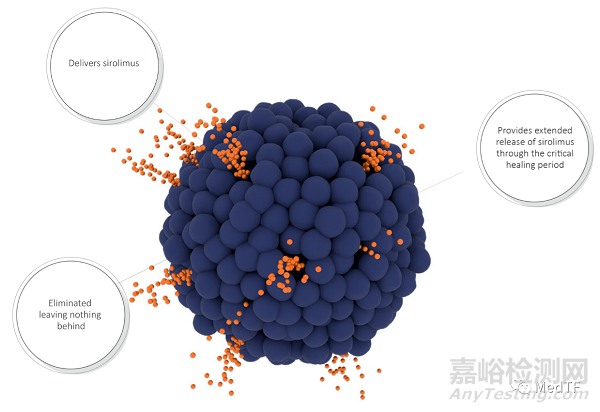
目前的用于治疗冠状动脉支架内再狭窄(ISR)的载药球囊基本上是紫杉醇涂层球囊,Orchestra BioMed认为这些紫杉醇涂层球囊没能完全解决患者临床需求,部分患者经过治疗后并不理想,例如治疗后药物释放存在突释、大药物涂层颗粒脱落造成血管堵塞等等。而Virtue SAB采用灌装方式,能够将西罗莫司注入到血管壁中,让西罗莫司缓慢释放,尤其是在在关键愈合期间延长西罗莫司治疗水平的局部释放,彻底改变药物输送,同时不留下任何痕迹,减少异物残留造成风险。
Virtue SAB这种原创技术也获得泰尔茂投资,泰尔茂为此支付3000万美元的预付款。同时泰尔茂还将负责 Virtue SAB 在全球冠状动脉和外周血管适应症市场中的设备制造、商业销售、营销和分销。
Orchestra BioMed除了Virtue SAB之外,还有一个起搏器产品线,这款产品线中的治疗高血压起搏器获得美敦力投资。
Virtue SAB
Virtue SAB 是一种血管灌注球囊,用于治疗某些形式的动脉疾病,旨在在球囊血管成形术期间将西罗莫司的专有缓释西罗莫司制剂输送到血管壁,而无需球囊表面的任何涂层或需要在动脉中留下支架或其他永久性植入物。
Virtue SAB采用独特的SirolimusEFR技术,该技术能够在大约 30 天的关键愈合期内,延长西罗莫司治疗水平的局部释放。
Virtue SAB临床
Virtue SAB 在 50 名患者的前瞻性、多中心 SABRE 试验中证明了对冠状动脉支架内再狭窄 (ISR) 患者的安全性和有效性。


Orchestra BioMed
Orchestra BioMed是一家美国生物医学创新公司,成立于2017年。公司致力于推动创新医疗产品的商业全球化。该公司有两款值得关注的产品,第一个是美德西罗莫司血管灌注球囊,这是一种新型的预防球囊血管成形术中血管再狭窄的医疗产品,该款产品已获得了美国FDA“突破性设备”称号;第二个产品是BackBeat心脏神经调节疗法,这是一款处于临床试验阶段的可植入式心脏刺激治疗设备,该药物已在临床研究II期研究中证明治疗高血压的功效和安全性,可显著持续降低血压水平,目前公司已着手开展临床III期的临床试验。