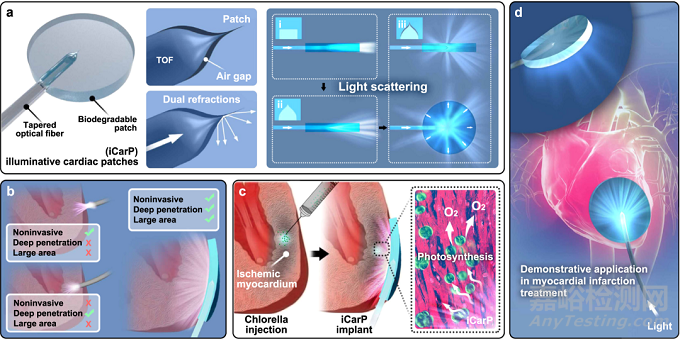
日前,浙江大学周民研究员团队研发了一款能够实现远程控制心脏活动的装置,名为iCarP(illuminative cardiac patch)。这是一种柔性导光贴片,可以植入并集成到心脏表面,在无线光控制下实现对心脏活动的调节,具有潜在的临床应用前景。
该研究成果以“A biodegradable, flexible photonic patch for in vivo phototherapy”为题,被收录于国际顶级期刊《Nature Communications》。
柔性导光贴片“iCarP”
iCarP的诞生是一次科技创新的巨大飞跃。据了解,该贴片采用柔性光子学结构,使其能够与心脏表面完美贴合。关键在于,研究人员成功引入了一种光敏蛋白质,这种蛋白质能够对特定波长的光做出高度敏感的反应。借助这种机制,科学家们能够通过照射特定光波来操控心脏的脉动和跳动。
然而,外部光源的光照并不能有效地触发这些光敏荧光颗粒产生活性氧分子。由于iCarP材料内部的光敏荧光颗粒受到了复杂的生物环境影响,光能的传递和激发效率也可能受到限制,导致外部光源难以有效地激活iCarP内部的活性氧产生。
光散射光子器件的设计、功能和演示应用,对内脏和组织的深度照明
为了解决这一问题,研究团队精心设计了光敏荧光颗粒,确保其能够被体内的光源激发产生活性氧分子,从而实现精确的光敏治疗效果。此外,他们还优化了材料的结构和成分,以提高光能传递和转化效率,确保光敏荧光颗粒能够充分受到激发。
在体外实验中,研究人员使用iCarP材料刺激心脏细胞,并通过荧光成像监测细胞的响应。结果显示,iCarP材料能够实现精确的光敏激活和监测。在进一步的动物试验中,研究人员将iCarP设备植入动物心脏表面,然后远程照射特定波长的光。结果显示,这种无线光刺激能够准确地操控心脏的跳动频率和强度,这一突破性技术为心脏疾病治疗领域带来了新的希望。
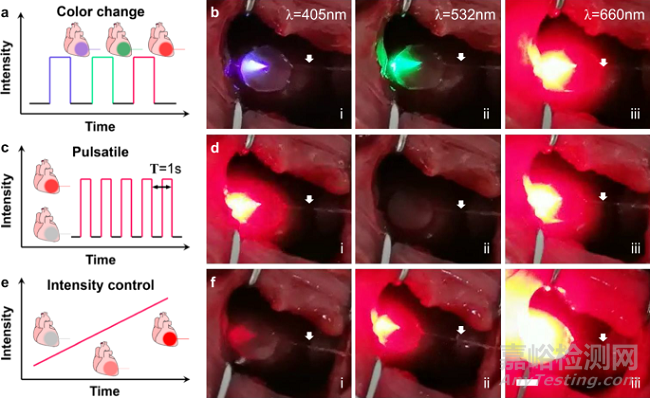
iCarP在动物实验中的照明演示
而此次器件的制备要从藻类说起。藻类是一种能够进行光合作用的微生物,它们可以利用光能来合成有机物质。研究团队受到藻类光合作用的启发,设计出了能够在光照下释放氧气并实现光敏调控的iCarP。
具体来说,科学家们在iCarP中引入了一种类似于藻类光合作用的机制——通过光敏蛋白质和可降解聚合物的组合,实现了在光照下产生氧气并调控细胞的功能。这种设计灵感的借鉴使得iCarP能够在体内模拟藻类的光合作用过程,从而实现对心脏细胞的精准控制。
与目前市售的医用光纤相比,iCarP 兼具大光照面积和大光照深度的优势。同时,对于不同波长光,其具备一定的普适性,并能实现多种模式的照明。这也意味着它能用于包含光动力治疗、光热治疗、以及光遗传治疗在内的光疗手段之中,并有望在某些疾病治疗上替代现有的导光设备。