预充针逐渐成为复杂的生物制品的选择,选择使用预充针比使用小瓶包装节省了产品的体积用量,降低了生产成本。有多种预充针来满足不同的要求,这些要求使得在选择预充针材质时面临着挑战。Baxter生物制药解决方案研究总监对预充针的选择给出了一些看法和建议。
预充针(PFS)市场增长继续保持强劲的态势,最近一份报告显示预计到2019年PFS的全球销售额可达49.8亿美元(39亿英镑)。PFS产品销售增长的推动因素包括药企研发管线中注射用生物制剂的增加和生物制剂的全球化。
预充针对于高成本、复杂的生物制品(如单克隆抗体和融合蛋白)的开发者有着特别的吸引力。与瓶装制剂相比,预充针需要最小的过量灌装体积以确保患者注射准确的剂量,每批节省的装量就可以抵消PFS组件的成本。
法规对生物制品的要求推动了预充针的创新。虽然I型玻璃仍然是注射器常用的材料,但塑料注射器也越来越受欢迎,包括环烯烃聚合物(COP)、环烯烃共聚物(COC)、聚丙烯(PP)和聚碳酸酯(PC)。在日本,50%的注射器是塑料的。聚合物注射器无菌、随时可用、具有玻璃外观(图1),并且耐磨损。
除了West Pharmaceutical Services Crystal Zenith公司的COP注射器外,大多数注射器针筒需要添加硅油使活塞在使用过程中平稳滑动。一般需要硅胶的聚合物材质的注射器有BD公司的Sterifill™(使用较少的硅胶)或Schott公司的TopPac SD®(使用交联硅胶)。
可以依据针筒形状与结构、硅胶水平和钨含量选择不同的预充针,使得选择预充针变得复杂。
对于生物制品而言,理想的注射器针筒应该降低硅油的用量,因为硅油能引起多种蛋白质的聚集。研究表明蛋白质的聚集水平与硅油含量成正比。
在大多数玻璃注射器针筒生产时,使用钨探针在注射器尖端形成流体通道,可能会残留氧化钨蒸汽和钨颗粒。已经确定可溶性钨残留是引起临床批次的α重组人肾红细胞生成素和α螺旋蛋白高水平异常聚集的根本原因。
注射器生产商已经专门为生物制品设计了PFS系统,这些产品钨残留量较低,如BD公司的用于生物技术的Hypak™玻璃注射器和Sterifill™ COP注射器。Schott syriQ®的玻璃固定针注射器和West Pharma Crystal Zenith COP固定针注射器均不含钨。
随着可以选择注射器针筒结构、硅树脂含量和钨含量,PFS系统的选择变得复杂。使用较新的PFS系统会增加成本,因此需要在最终确定处方之前通过实验评估PFS对产品质量存在的潜在影响,并平衡质量和成本。
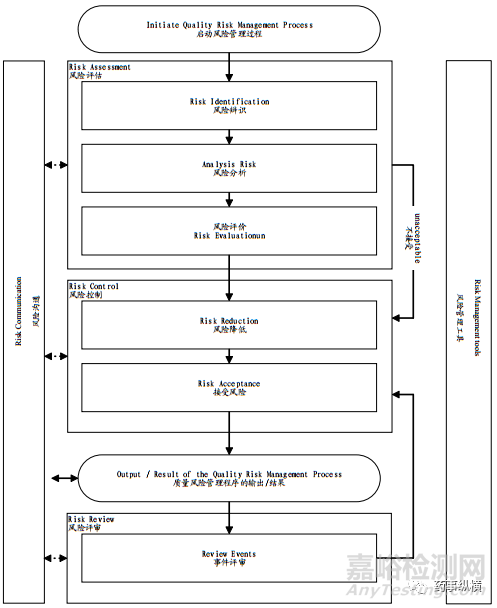
ICH Q9质量风险管理(图2)中风险管理流程可用于评估药物处方和PFS的相容性。第一步-风险识别,可以扩展到公司管线中的大多数肽类、蛋白质和mAb产品。建议对不相容的风险进行评估,包括1)玻璃分层,2)对钨的敏感性和3)硅油引起的聚集;第二步-风险分析,可以通过文献调研完成。
近年来,已有玻璃分层或玻璃颗粒从容器内表面剥落导致产品召回的案例。玻璃分层不是即刻显现的,通常会在稳定性样品中发生,特别是高温条件下放置的样品。已知的处方风险因素包括pH≥8.0的药品;醋酸盐、柠檬酸盐和磷酸盐缓冲溶液的存在;EDTA等螯合剂的存在;有机酸的钠盐的存在以及高浓度的碱性盐。终端灭菌也存在风险,但不适用于生物制品。
玻璃的化学成分和生产工艺-特别是形成和退火也会影响玻璃分层。加热速率、最高温度、退火时间和温度等因素都会引起玻璃耐用性的变化。
PFS的生产过程不同于小瓶注射剂,在生产期间降低了注射器针筒的接触面积。在一项比较使用小瓶和PFS的处方研究中,得出的结论是大多数测试条件下PFS优于小瓶,并且对于其他测试条件具有相同的性能。柠檬酸盐或磷酸盐缓冲液的存在可能导致释放元素杂质。PFS没有召回或分层报告,表明使用PFS不存在重大风险。
已有多篇文献报道了钨诱导蛋白质聚集。用钨沉淀mAb的研究表明在pH5.0的条件下钨诱导其快速凝聚,但在pH>6.0条件下处方中蛋白质聚集的风险较低,因为较高pH条件会抑制钨聚阴离子的形成。在pH7.0的重组人肾红细胞生成素缓冲溶液中加入钨针提取物,在25℃条件下储存6个月后检测到少量的聚集体。pH 4.0的α螺旋蛋白质制剂对钨诱导的聚集敏感性研究,确定了使用真空塞子增加了溶液中钨的残留量。真空塞子除去了漏斗区域和产品之间的气体,将溶液暴露于注射器中富含钨的区域,从而导致了蛋白质的聚集。
在溶液中加入硅油以及通过比较硅化注射器中的溶液与非硅化注射器进行硅油-蛋白质相互作用的研究。全面研究处方因素的影响,关于硅油引起蛋白质聚集的机制研究尚未完成,但可以帮助研发人员确定一些风险因素。
硅油引起的聚集最有可能发生在蛋白质的饱和溶液中。在针对多种抗SEB mAb研究中,仅在pH接近pI和振摇后才观察到蛋白质聚集。在IgG1模型的研究中,含0.01%的吐温20的溶液在搅拌过程中能够抑制硅油诱导的蛋白质聚集。该研究的作者推测表面活性剂与蛋白质分子竞争吸附油-水、空气-水和油-空气-水的相界面。同样的研究表明蔗糖能够部分抑制硅油诱导的蛋白质聚集。
另一种理论是蔗糖增加了硅胶液滴的形成速度,可能降低了油水界面面积,但需要进一步研究来了解蔗糖是否有对硅油-蛋白质相互作用产生影响。
PFS选择的风险分析汇总在表1中。在分析处方因素后,该工艺转向风险评估。在具有多种玻璃分层风险因素的处方中,进行实验对风险评估需要延长稳定性研究的时间。在这种情况下可能会面临风险,建议考虑使用共聚物注射器。
蛋白质对钨的敏感性可以通过简单的掺加研究来评估。硅油诱导的蛋白质聚集风险评估可以通过硅油-水乳液掺加到处方中并使样品聚集来进行研究。Badkar描述了详细的试验研究。所引用的许多文献都依赖之前发表的流动成像技术。流动成像技术既可以对颗粒进行计数,也可以对颗粒形态的进行评估。功能强大的软件允许根据粒子的形状对粒子进行分类。硅油滴具有特征性的球形外观,具有光中心和朝向球体外部的增加的对比度(图3),这允许流动成像软件系统识别较小的硅油颗粒。流动成像技术还可以识别与硅油滴结合的蛋白质聚集体。
使用溶液掺加研究进行风险评估之后,可以通过选择注射器特性(如超低硅树脂、交联硅树脂或无硅树脂产品)来降低风险。在进行最终选择之前,建议使用手动注射器进行小型加速稳定性研究。样品应在标准和加速条件下储存。
对于生物制品,至少应使用流动成像技术和产品稳定性指示测试方法来评估亚可见聚集体的形成并评估产品稳定性。此外,加速稳定性研究是确保注射器功能(特别是最大滑动力)不被产品改变并且满足患者的需要。
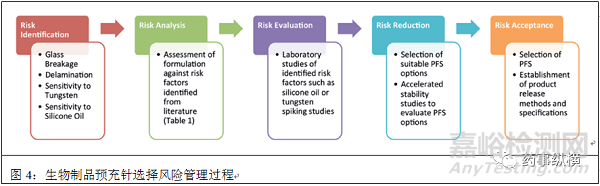
强烈建议评估多批PFS。在内部未发表的研究中,使用流动成像技术发现不同批次的PFS中与硅油相关颗粒数量存在显著差异。应在选择容器密封盖时启动对可提取物/可浸出物的研究。风险管理流程(图4)最后选择了PFS。通常定期对产品进行不同批次的检测和供应商进行持续监控,以便通知和评估任何注射器生产变化对于产品质量的重要性。
生物制品的复杂要求推动了预充针技术的创新,这为产品开发团队提供了广泛的选择。虽然新的注射器选择可能会增加产品的成本,但评估特定处方不稳定性和组件的风险应该平衡质量、安全性、成本。ICH Q9质量风险管理提供的框架可用于创建PFS容器选择的有效流程。