终末期肾病是慢性肾病的最后阶段,肾功能已经衰退到肾脏不能再自行运转的地步。在肾功能完全正常的情况下,血液中的废物和多余的液体会被过滤,然后随尿液排出体外。对于 ESRD 患者来说,肾脏失去了过滤能力,体内积聚的液体、电解质和废物就会达到危险的水平。美国约有 80 万 ESRD 患者,其中 71% 依靠透析来控制病情,其余 29% 则接受了功能性肾移植。
近日,致力于使肾脏护理更方便的医疗技术公司Quanta透析技术公司 (Quanta Dialysis Technologies®)宣布,该公司已向美国食品药品管理局 (FDA) 提交了一份 510(k) 上市前通知,申请扩大Quanta™透析系统的适应症,这是一款结构紧凑、易于使用的血液透析设备。Quanta透析系统目前适用于慢性肾病和急性肾病治疗。新提交的申请旨在将使用范围扩大到自我护理、居家血液透析。
新提交的 FDA 510(k) 申请旨在将Quanta透析系统的适应症扩展至自我护理、居家血液透析。美国食品及药物管理局的批准将增加终末期肾病患者可选择的家庭血液透析设备的数量。
根据美国肾脏数据系统(U.S. Renal Data System)的数据,美国有超过 49 万人使用血液透析治疗终末期肾病(ESRD)。家庭血液透析(HHD)取代了每周三次往返透析诊所接受治疗的方式,占血液透析总人数的 2%。研究表明,与传统的中心透析相比,家庭血液透析有很多好处,如提高生活质量、改善健康状况和获得医疗服务。鉴于家庭透析的好处,医疗保险和医疗补助服务中心(CMS)制定了一项计划,鼓励医疗保险受益人更多地使用家庭透析和肾移植。
Quanta公司首席执行官 Alejandro Galindo 表示:"Quanta透析系统获得 FDA 批准用于家庭透析,这是Quanta公司的一个重要里程碑,我们的目标是让每一位患者在任何情况下都能更方便地进行透析。"Quanta透析系统已经为英国患者提供了血液透析所带来的自由和灵活性。随着这项510(k)认证的通过,美国患者将对他们的治疗有更多的控制权,并可以选择接受治疗的地点、时间和方式。
Quanta透析系统将成为美国第三种适用于终末期肾病 (ESRD) 患者血液透析的设备。预计美国食品药品管理局将于 2024 年批准扩大适应症。
Quanta提交的 510(k) 申请得到了 Home Run™ 研究临床数据的支持,该研究是一项前瞻性、多中心、开放标签试验,旨在评估Quanta透析系统用于 HHD 的疗效和安全性。该研究的全部结果将于今年11月在宾夕法尼亚州费城举行的美国肾脏病学会(ASN)肾脏周上进行海报展示。
关于Quanta家用透析
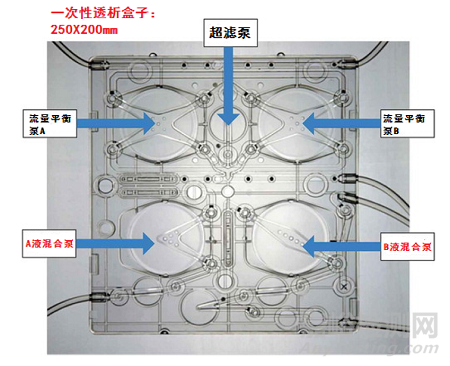
设备亮点在于设计了一次性透析盒子,全部液体均不接触透析机内部,使用后无需消毒。也是目前唯一一款将推拉式血液透析集成到小型透析设备以提高清除率的商品。
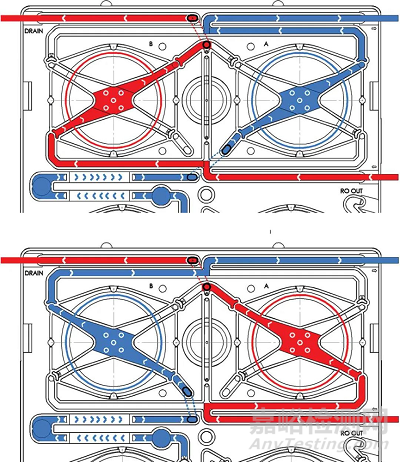
流量平衡系统原理实际是容量平衡,和平衡腔基本一样,但是设计很巧妙。每个平衡周期有22ml液体进出透析器,交换速度非常高。
关于Quanta透析技术公司
Quanta透析技术公司(Quanta Dialysis Technologies)致力于通过广达透析系统让每一位患者在任何环境下都能获得透析服务。Quanta透析系统是一种便携式设备,其性能可与大型传统透析机媲美,是一种模块化的强大解决方案,具有在多种环境下提供透析护理所需的临床多功能性。Quanta透析系统的用户界面简单易用、直观易懂,适合各类用户操作,可直接为患者提供透析服务。Quanta透析系统已在英国上市,供家庭和医院使用。在美国,它通过了 FDA 认证 (K222067),可用于慢性病和急症护理,治疗类型包括间歇性血液透析 (IHD)、持续低效透析 (SLED)、延长间歇性肾脏替代疗法 (PIRRT)、慢速持续超滤 (SCUF) 和持续静脉血液透析 (CVVHD)。Quanta透析系统已在英国上市,可供家庭和医院使用;在美国,可用于慢性和急性护理环境,但不适合家庭或夜间使用。