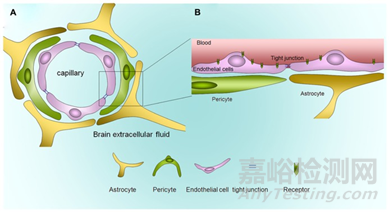
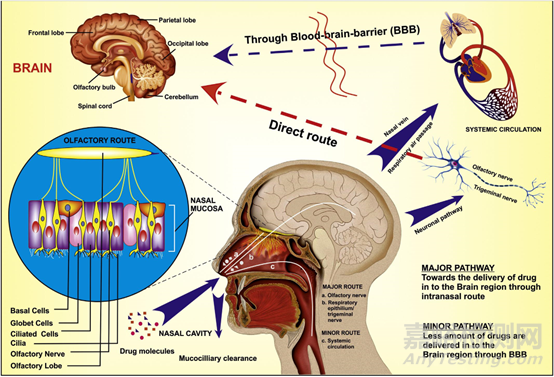
98%小分子和近100%大分子药物由于血脑屏障(blood-brain barrier, BBB)的存在而被限制进入中枢神经系统(central nervous system, CNS)发挥作用。BBB结构如下图所示,BBB阻止有害物质由血液进入脑组织保护我们的同时,也阻止了药物分子被摄取吸收,为神经和精神领域工作者提出了挑战。
图1:血脑屏障的解剖结构
针对BBB的存在,进行CNS给药最直接粗暴的方法便是进行脑室手术给药(脑室内或脑实质内注射),但是该方法价格昂贵,对操作人员素质要求较高,患者也面临较高的风险。
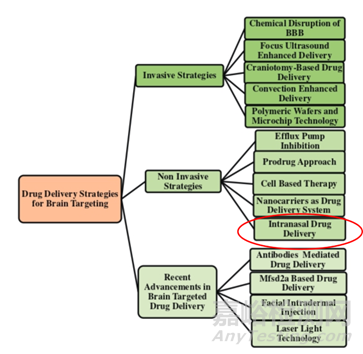
图2:脑部药物递送策略
况且目前许多人还存在能吃药不打针,能打针不输液的思想,不到疾病发展到万不得已,没人会进行手术治疗,更不用说脑部手术了。鼻腔内给药已经成为侵入性给药方法的一种替代,它可以通过嗅觉和三叉神经途径绕开BBB的障碍而直接靶向CNS。
鼻腔给药药物靶向脑的重要途径之一,它是由阿尔茨海默氏病研究中心的william ll frey博士于1989年首次提出,并获得专利。那么,单单拿出来鼻腔给药这个技术,具有什么优势呢?
首先,我们的鼻腔具有丰富的血管丛,药物可以直接入血而避免消化道破坏和首过效应,改善药物的生物利用度和动力学(针对CNS疾病,药物直接入血还是会存在BBB障碍);其次是鼻腔靠近脑部,可以迅速提高脑部以及脊髓的药物浓度,利于靶向治疗和降低副作用;而且鼻腔用药量少且给药方便,患者依从性好。
那么,鼻腔给药后药物是如何通过鼻-脑通路的呢?
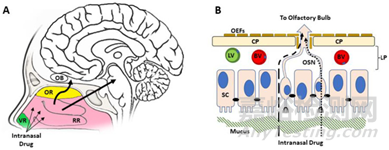
鼻腔给药后,药物穿过嗅区(olfactory region, OR)沿嗅神经(左箭头)移动至嗅球(olfactory bulb, OB),或沿侧呼吸区(respiratory regions, RR)和三叉神经(右箭头)移动至脑桥(图A)。与嗅觉途径相比,三叉神经通路对鼻-脑药物转运的贡献比较小。药物也可能通过淋巴管(lymphatics, LV)或脉管系统(vasculature, BV)被全身吸收(图B)。
其中,药物的细胞内转运包括神经元对药物的内化、沿轴突的转运以及在 CNS 内另一端的胞吐作用。细胞外途径中,上皮细胞之间存在许多紧密连接,但通道的短暂开放允许分子运动进入固有层;嗅觉神经元进行新旧替换时的缺口也会允许药物进入固有层。细胞外途径药物运输效率高于细胞内运输,是鼻腔给药优化的重点方向。
图3:鼻腔、鼻上皮和通往中枢神经系统的运输途径的解剖学和组织学
目前鼻腔给药的剂型有滴鼻剂(nasal drop)、气雾剂(aerosol)、喷雾剂(spraying agent)、粉剂(dusts)、凝胶剂(gel)、微球(microspheres, 1-1,000μm)、脂质体(liposomes, 20nm-20μm)以及乳剂(emulsion)。
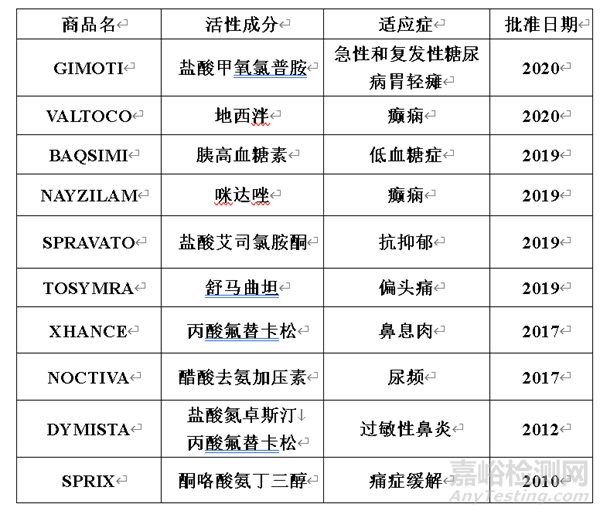
下表为部分 FDA 已批准上市的鼻腔药物信息,以喷剂为主,部分为粉剂提供(BAQSIMI、SPRAVATO、XHANCE等)。相比于液体制剂,粉剂由于稳定性高而更适用于蛋白质、多肽类的药物分子。这些制剂适应症广泛,不单单针对CNS类疾病。
表1:2010年以来 FDA 批准上市的鼻腔药物
如上所述,鼻腔给药在一定程度上具有其他给药途径不可比拟的优势,且可针对包括CNS在内的诸多疾病的治疗,那么鼻腔给药看似简单,采用滴鼻方法或喷雾类器械联合使用便可,实则鼻腔也存在给药障碍。下面我们看下针对CNS疾病,鼻腔给药带来哪些挑战与对应可能的应对策略。
首先,我们先看下鼻腔自身生理环境对药物吸收的影响。
鼻腔粘膜面积约200cm2,上皮细胞与毛细血管紧密连接,丰富的血管和淋巴管有利于药物的入血吸收但避免不了BBB的障碍。羟甲唑啉被用作过敏和感冒的减充血剂,作为血管收缩剂,其被证明可以减少鼻子内的血流量。事实上,包括温湿度、疾病(鼻炎等)和心里压力在内的多种因素均会对鼻内血流量产生影响,这为鼻腔给药带来了不小挑战。
图4:药物从鼻腔给药后靶向CNS通路和障碍
鼻腔有粘液(含有大量水、离子和蛋白)和纤毛的存在,粘液纤毛清除机制限制了疏水和带电分子的的扩散,这为药物的设计带来的挑战,因此给药前鼻腔的清理可能是一个好策略。纤毛鼻腔前部比后部要少,为了避免其清除,可将药物尽量施用在鼻腔前部。鼻腔也存在有药物代谢酶,尽管其相比于消化道酶活性低,但是在异物清除中的作用也不可忽视。
其次,我们来看下药物本身对其吸收的影响。
鼻腔给药的药物一般是小分子(表1常见药物分子量分布于300-500Da),不带电、亲脂性的小分子容易通过粘液。当然,药物的分子量只是限制吸收因素之一,研究表明胰岛素甚至是干细胞都能通过鼻腔给药而达到脑部转运的目的。制剂辅料的添加往往会对粘液结构产生影响,因从需要注意配方问题。粉剂会存在溶解后吸收的过程,因此溶解度大或增溶剂的添加有利于药物吸收。喷雾的药液粒径在5-10μm范围容易沉积在鼻腔后良好吸收。
刚才说到辅料问题,常见的辅料添加应该考虑什么问题呢?
一般而言,辅料不仅对粘液产生影响,反过来,小体积的药物会被粘液理化环境所影响,因此需要添加缓冲剂(eg. TOSYMRA:柠檬酸盐、磷酸盐);生物黏附剂(卡波姆)的添加可以减弱粘液纤毛清除;吸收促进剂如表面活性剂(eg. GIMOTI:苯扎氯氨,SPRIX:依地酸二钠)的添加可以增加鼻粘膜的通透性;酶抑制剂(eg. SPRIX:依地酸二钠)的添加可以减弱代谢酶活性;为了得到一个出色喷雾效果与均一性,DYMISTA添加了纤维素和羧甲基纤维素钠。当然,常见的抗氧化剂、防腐剂(eg. GIMOTI苯扎氯氨;DYMISTA:聚山梨酯80)等也是最常见的药物辅料。辅料的添加可能存在多种作用,如苯扎氯氨兼有防腐和促进吸收的作用,依地酸二钠兼有酶抑制和促进吸收的作用。
克服这些问题的制剂方法的共同主题包括减少从鼻腔环境的清除、改善药物本身性质、合理添加辅料来达到包括增加渗透性在内的目的。
实际给药过程中发现诸如头部姿势、给药方式(剂型以及器械)、体积在内的多种因素会影响药物在鼻腔的沉积以及进入CNS的途径。临床前以及临床实验建议采用仰卧位的姿势给药(小鼠:~5μL,大鼠:~50μL),2020年FDA批准治疗癫痫地西泮(商品名:VALTOCO)喷雾的产品说明见下图。尽管动物与人的鼻腔载药体积、嗅觉占比表面积等存在差异,但是相似的药物转运吸收途径也为临床试验提供了一定依据。
图5:地西泮(100μL/支)喷雾的产品使用说明
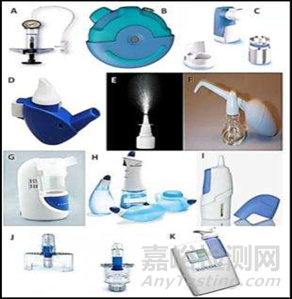
不同的给药装置也是影响因素之一,目前有包括喷雾器、干粉吸入粉、滴注鼻导管等在内的多种鼻腔给药装置。
图6:鼻腔给药装置
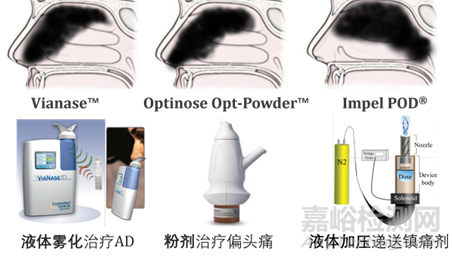
虽然目前存在有多种给药装置,但它们共同的目标是将更多的药物施加在鼻腔的嗅觉区域。
图7:不同鼻腔给药装置给药后的剂量分布
神经系统疾病在老龄化快速的发展下必然成为未来世界上的一大负担,单拿老年痴呆而言,我国老年痴呆患者实际人数已远远超过1000万,有着巨大的临床需求。BBB限制了系统给药疗法对CNS疾病的治疗,对相关CNS疾病药物开发人员的工作提出了重大的挑战。
图8:每10万人中阿尔茨海默病和其他痴呆症的年龄标准化患病率
鼻腔给药已经有几十年的长足发展,其中脑部靶向已经在啮齿动物和人类实验中得到了有力证据的支持。包括纳米制剂在内的新兴的制药技术与鼻腔给药方法结合来突破BBB障碍,对CNS疾病的治疗具有广阔的应用前景。
综上,鼻腔给药来突破BBB进行CNS给药将成为绝佳给药的候选方案之一。
路虽远,行则至。
参考文献
1. Xu G, Mahajan S, Roy I, Yong KT. Theranostic quantum dots for crossing blood-brain barrier in vitro and providing therapy of HIV-associated encephalopathy. Front Pharmacol. 2013 Nov 15;4:140. doi: 10.3389/fphar.2013.00140. PMID: 24298256; PMCID: PMC3828669.
2. Crowe TP, Hsu WH. Evaluation of Recent Intranasal Drug Delivery Systems to the Central Nervous System. Pharmaceutics. 2022 Mar 12;14(3):629. doi: 10.3390/pharmaceutics14030629. PMID: 35336004; PMCID: PMC8950509.
3. Hong SS, Oh KT, Choi HG, Lim SJ. Liposomal Formulations for Nose-to-Brain Delivery: Recent Advances and Future Perspectives. Pharmaceutics. 2019 Oct 17;11(10):540. doi: 10.3390/pharmaceutics11100540. PMID: 31627301; PMCID: PMC6835450.
4. Agrawal M, Saraf S, Saraf S, Antimisiaris SG, Chougule MB, Shoyele SA, Alexander A. Nose-to-brain drug delivery: An update on clinical challenges and progress towards approval of anti-Alzheimer drugs. J Control Release. 2018 Jul 10;281:139-177. doi: 10.1016/j.jconrel.2018.05.011. Epub 2018 May 24. PMID: 29772289.
5. Khan AR, Liu M, Khan MW, Zhai G. Progress in brain targeting drug delivery system by nasal route. J Control Release. 2017 Dec 28;268:364-389. doi: 10.1016/j.jconrel.2017.09.001. Epub 2017 Sep 6. PMID: 28887135