当一个药物分子不能与其镜像重合时,该药物就称为手性药物。这里我们所说的手性药物主要是指以单一的立体异构体开发的药物,不包括外消旋体药物 。由于手性药物与其对映异构体在非手性环境下的理化性质均相同,所以在研究手性药物时,应注意从立体化学的角度考虑问题。本期我们接着化合物结构研究系列来说下仿制药中手性药物的研究内容和注意事项。
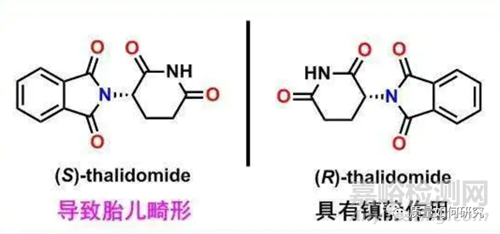
举一个经常被大家引用的例子来说,沙利度胺(Thalidomide)由于其手性异构体没有经过严格的安全性评价,从而使得它从“天使”变为了“魔鬼”,造成了迄今为止最大的药物安全事件。当然,后面通过老药新用和二次开发,又让它重新获得FDA的批准用于治疗麻风病人和骨髓瘤的治疗。
对于仿制药中手性药物的研究,我们主要从以下五个方面来分析,具体如下:
1、制备工艺
对于研发单位来说,药物的制备工艺是整个药物研究的基础 。若工艺不稳定、 不可控,则药品质量的稳定、可控就成了无源之水。因此,在手性药物的制备工艺中应注意以下问题 :
所用的合成路线应有依据 (文献或理论 ), 注意反应条件及关键中间体的分离与纯化方法的选择,以及合成工艺中消旋化的可能性。
需采用具有立体选择性的方法控制手性原料、手性试剂及引入手性中心后的重要中间体的光学纯度,并提供详细检测方法及图谱。
对于含两个以上手性中心的药物,因最终产品中可能存在的光学异构体杂质数目多,质控难度大,此时对最终产品光学纯度控制可采用加强合成过程中工艺条件的控制,对各手性中间体及原料的光学纯度严格控制来实现。
2、结构确证
结构确证的作用在于回答“产品对不对的问题”。所有的质量研究都是基于对的化合物结构基础之上的。因此对手性药物的特殊要求主要有以下几点 :
应确证产品的立体构型。可根据手性中心的多少、文献数据是否充足、对照品的有无来选择合适的确证方法,必要时可采用单晶X-射线衍射进行确证。
比旋度通常是必需的检测项目之一。
已知的起始原料的构型和化学合成方法的立体选择性也可作为依据之一。
3、质量研究
由于非对映异构体与普通的非光学杂质一样, 可以通过非手性的分析方法进行分离控制 ,所以,手性药物的质量研究应重点考察对映异构体的分析方法是否合理即可 。但需注意的地方是:
单用比旋度控制手性药物的光学纯度不够完善,尤其是在药物本身比旋度数值小以及有多个手性中心存在的情况下,用比旋度控制药物光学纯度是有很大误差的。因此,还应采用手性色谱法 (手性HPLC及毛细管电泳等)或手性衍生法进行控制,并且所用方法应提供详细方法学研究资料,尤其要注意分离度是否符合要求 (建议提供相应的消旋化合物的分离图谱作为佐证)。
对于含有多个手性中心的化合物,由于其非对映异构体可通过普通色谱方法进行定性或定量测定,故可作为一般杂质处理,以简化研究工作。
4、质量标准
对于原料药来说,比旋度作为药典收载的常规理化常数,具有仪器简单、数据直观的点,在一定程度上能反映产品的纯度。因此,该项目一般都应列人原料药质量标准之中。但须注意其范围不应过大,否则起不到控制产品光学纯度的目的。采用立体专属性的含量测定或有关物质检查方法,能更加精确地控制手性药物的纯度。因此,为严格控制产品质量,一般应将两者结合起来。即
首先,应制定合理的比旋度范围。
其次,如含量测定采用非立体专属性方法,应在 “有关物质”项中增加对映异构体的检查,限度应根据实测情况及稳定性考察的结果确定。
另外,对于含有多个手性中心的药物 ,如果根据所用的合成路线及质量研究的结果,对映异构体不可能存在,则可不定入对映异构体检查项,但应对其他可能产生的非对映异构体进行控制。
而对于制剂来说,手性药物制剂的标准中是否定入立体专属性的鉴别项或对映异构体的检查项应从两个方面来考虑:一是该手性药物在制剂的制备及放置过程中有无外消旋化,二是该手性药物是否同时也有其外消旋体或对映异构体上市销售。
如果该手性药物在制剂的制备及放置过程中有外消旋化发生,则制剂的标准中一定要制订对映异构体的检查项。
如无外消旋化发生,但同时有该手性药物的外消旋体或对映异构上市销售,则制剂的标准中不必制订对映异构体的检查项,但应该定入立体专属性的鉴别项,以与该手性药物的外消旋体或对映异构体相区别。
如无外消旋化发生,并且也没有该手性药物的外消旋体或对映异构体上市销售,则制剂的标准中既不必制订对映异构体的检查项,也不必定立体专属性的鉴别项,但企业可自行选择。
5、稳定性研究
手性药物因各自结构的不同,由于各种因素(如高温、高湿、酸、碱、强光等)的影响,在放置过程中有可能发生外消旋化,因此在稳定性研究时,应采用立体专属性的分析方法对此进行考察,以给处方及工艺的确定、成品的储存、标准的制定提供依据。
对于原料药来说,稳定性的要求是应采用质量标准中的方法考察其有无消旋化的倾向。具体要求如下:
影响因素试验应考察本品立体构型的稳定性。
如影响因素试验证明本品立体构型稳定,则加速试验及长期留样试验只需在试验开始及结束时监测立体构型的变化;
如影响因素试验证明本品立体构型不稳定,则加速试验及长期留样试验时,应多在几个时间点监测立体构型变化情况。
对于制剂来说要求是一样的,即采用立体专属性的分析方法考察本品有无消旋化的倾向。