2023年11月19-20日,由国家药品监督管理局高级研修学院主办的2023年贴剂与贴膏剂研发技术与申报策略培训班在长沙召开。可见,近年来,随着仿制药一致性评价逐渐接近尾声,入局普通仿制药的药企逐渐变少。高端复杂剂型反而受到了越来越多的关注,如透皮给药剂型。目前透皮制剂主要包括贴剂、软膏剂、凝胶剂、乳膏剂、洗剂、凝胶贴膏剂等剂型。
透皮制剂是一类用于皮肤从而发挥局部或全身治疗作用的制剂。对于透皮制剂的质量研究来说,体外释放试验(IVRT)和体外渗透试验(IVPT)是比较关键的体外研究项目。这两项研究对制剂开发过程中的处方工艺筛选以及模拟外用药物在生理条件下的透皮过程,起到了重要的指导和参考意义。而体外释放一般由剂型、原料、辅料、工艺等多种因素决定。一般在开发透皮制剂产品时,虽然证明Q1、Q2与RLD的相同可以减少BE的风险,但辅料及其关键材料属性会影响微结构特征(即Q3表征的主要内容)。故本文主要讨论辅料对体外释放的影响。
通常,透皮制剂的辅料组成包括粘合剂、溶剂、增溶剂、乳化剂、渗透促进剂、防腐剂、pH调节剂、抗氧化剂、螯合剂和增粘剂等。辅料对体外药物释放的影响主要有:1.所用辅料的来源/型号;2.所用辅料的功能性质;3.所用辅料数量。
一、 不同来源辅料的影响
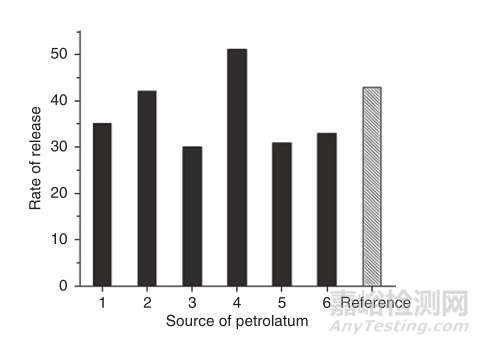
本案例研究不同来源/型号的辅料对药物释放速率产生的影响。2012年,Baynes等人发表文献指出,某制药公司在开发类固醇激素品种时,处方中使用了特殊型号的白凡士林,导致临床试验与参比制剂的生物不等效。通过调查后发现,凡士林的生产来源和型号均不同。故采用了六家不同的凡士林生产商生产的凡士林,进行制备样品研究,使用IVRT方法与市售参比制剂进行药物释放比较。结果表明,不同来源的凡士林确实产生了不同的类固醇释放速率(图1)。主要原因是凡士林是一种长链烷烃的混合物,不同厂家生产的凡士林的碳氢化合物的链长分布比不同,会导致其释放不同。与参比制剂相比,含6号凡士林的制剂释放速率较低,可能为临床失败的主要原因。
含2号凡士林的制剂与参比制剂相比具有相似的特征,在体外皮肤经皮吸收试验中证实了等效性,并在临床研究中证明了生物等效性,该案例研究清楚地表明了,虽然Q1和Q2一致,但是不同来源的辅料也会导致释放速率的不同
▲图1-不同来源/型号的凡士林对局部类固醇释放速率的影响
二、 不同功能辅料的影响
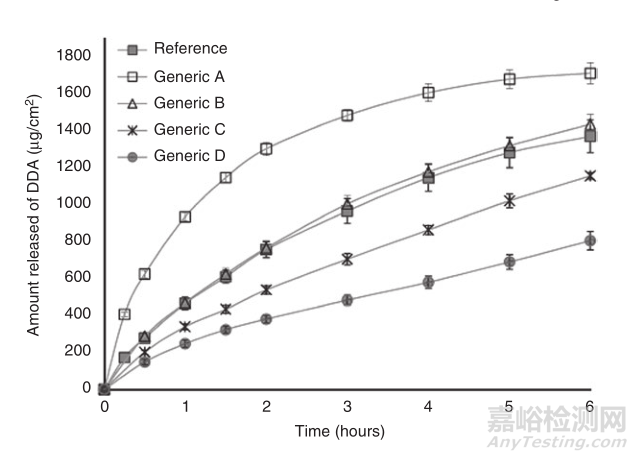
2013年,Goebel等人研究了乳胶剂中双氯芬酸二乙胺的体外释放。使用垂直式扩散池法,透过膜采用醋酸纤维素膜,将巴西制药市场上的四种批准的仿制药与参比制剂进行了比较。主要研究不同处方制剂的质量特征,在辅料和制备工艺方法方面可能存在微小差异。参比制剂和四种仿制药的处方组成见表1。从图2及表2可以看出:1)只有成分与参比制剂相似的处方(仿制药B)具有与参比制相似的释放曲线/速率,二者90%置信度极限值为94.99%-111.93%,在75%—133%之间,因此二者判断为相似。2)与参比制剂相比,添加了助乳化剂鲸蜡硬脂醇的制剂(仿制药C)释放缓慢,原因可能是鲸蜡硬脂醇作为增粘剂导致了药物释放速率慢。从表2也可以看出,相比于参比制剂,90%置信度极限值为66.82%-77.74%,低于标准值75%—133%。3)不含任何润肤剂的制剂(仿制药D)中的药物释放最低,90%置信度极限值也反应了仿制药D比参比制剂低。4)与参比制剂相比,仿制药A具有更快的释放速率,这可能是因为缺少异丙醇作为溶剂以及聚丙烯酰胺作为粘合剂,粘合的效果不理想,进而导致释放快。90%置信度极限值也表明仿制药A最快。
▲表1-不同厂家双氯芬乙二胺乳胶制剂的处方对比*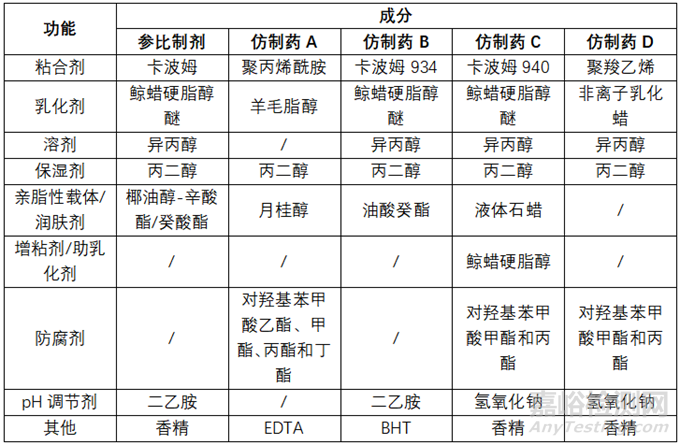
*实际所有处方中含有水和双氯芬酸二乙胺,但没有列在表中。
▲表2-参比制剂和4种市售仿制药制剂之间差异的统计检验
(使用聚醚砜收集收据)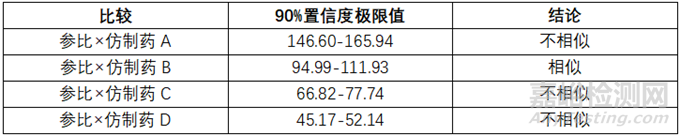
相似性要求:数值范围为75%—133%。(FDA 1997)
▲图2-参比制剂和四种市售仿制药的双氯芬酸二乙胺累积释放量
三、 辅料用量的影响
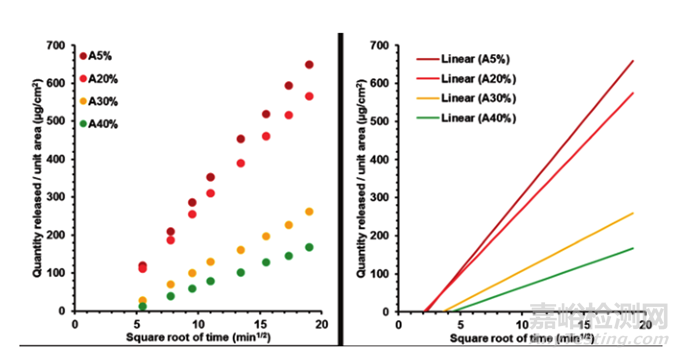
2017年,Radulescu和Miron研究了丙二醇浓度对阿昔洛韦乳膏体外释放的影响。发现当丙二醇的浓度从5%增加到40%时,观察到阿昔洛韦的药物释放减少(图3)。这可能是因为随着丙二醇用量的增加,乳膏的黏度降低,药物浓度降低,药物浓度梯度减少,进而导致释放减少;也可能是因为阿昔洛韦在丙二醇中溶解度比在水中低,进而导致药品中有效浓度低,进而导致释放度降低。
▲图3-丙二醇浓度(5%、20%、30%和40%)对阿昔洛韦药物释放的影响。
四、 辅料对体外释放方法选择的影响
辅料的类型也会影响药物体外释放试验方法的选择,如凡士林制备的软膏。2015年,Vonguru等人研究表明,在开发凡士林基软膏合适的IVRT方法时具有一定的挑战,原因是药物的亲/疏水性会直接影响药物在介质中的溶解度。但是通过选择非典型的IVRT方法,可以克服这些挑战。对于含有疏水性药物的凡士林基软膏,未选择常规的水性或水/醇介质,而是选择四氢呋喃、辛醇和二甲亚砜等溶剂作为扩散池介质。而对于含有亲水性药物的凡士林软膏,使用浸泡池系统,比常规垂直扩散池具有显著和更高的药物释放。
对于透皮制剂的研究,应更加注重辅料种类、用量、来源等对制剂的影响,当辅料为高分子类化合物时,辅料内在质量不同更容易导致制剂释放不同。因此在选择物料来源时,应做好充分的对比,否则很难做到与原研等效。此外,除了关注自研Q1、Q2与参比相同外,还应关注Q3的相似性(Q3包含微观结构、IVRT和体外透皮实验),做到宏观和微观的结合,将透皮制剂做到尽善尽美。
参考文献:
1.Baynes, J.Riviere, T.Franz, N.Monteiro-Riviere, P.Lehman, M.Peyrou, P.L.Toutain, Challenges obtaining a biowaiver for topical veterinary dosage forms.J.Vet. Pharmacol. Ther. 35(Suppl 1), 103–114 (2012)
2. Goebel, M.E.O.Sato, D.F.Souza, S.Murakami, I.F.Andreazza, In vitro release of diclofenac diethylamine from gels: Evaluation of generic semisolid drug products in Brazil.Braz.J.Pharm.Sci.49(2), 211–220 (2013)
3. Radulescu, D.S.Miron, Physicochemical characterization of acyclovir topical semisolid dosage forms towards TCS validation. 3rd FDA/PQRI Conference on Advancing Product Quality, 22-24 Mar2017
4. Vonguru, R.Gilman, R.Klein, D.M.Mattocks, K.D.Thakker, Developing in vitro release testing (IVRT) methods for petrolatum based semi-solid dosage forms. Abstract submission, AAPS (2015)
5. Nigel Langley·Bozena Michniak-Kohn David W. Osborne Editors.The Role of Microstructure in Topical Drug Product Development(2019)