今年的4.11是第28个世界帕金森病日。这一天是帕金森病的发现者——英国内科医生詹姆斯·帕金森博士的生日。
帕金森基金会数据显示,截至2020年全球有超过1000万名帕金森病患者,预计到2030年,这一数字将增长到1200万名。
随着帕金森病进展,药物治疗会逐渐失效,除了采用外科毁损疗法(即微电极进行靶点精准定位后,使用射频针加热毁损病变细胞,能够暂时缓解PD患者肢体震颤、关节僵硬等症状)外,脑起搏器已经是运动障碍类疾病的标准治疗手段。
“脑起搏器”植入术,是脑深部电刺激术(Deep Brain Stimulation,DBS)的俗称。
DBS,是运用脉冲发生器刺激其大脑深部的某些神经核,纠正异常的大脑电环路,以达到治疗或改善效果。作为利用电能对大脑神经活动产生影响的干预方式,是现阶段最被广泛接受的重要治疗方法。相关研究也在探索利用DBS治疗其他脑部疾病,如严重抑郁症和阿兹海默病。
1998年,脑深部电刺激疗法(DBS)进入中国;
1999年, DBS在中国注册用于治疗帕金森病和特发性震颤;
2016年,中国批准DBS用于治疗肌张力障碍和难治性癫痫。
截止发稿日,获批的脑深部刺激器及相关配件如下表:
1、脑起搏器发展历史
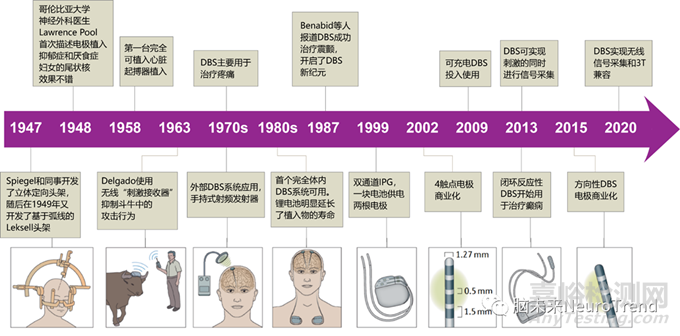
大脑皮质下植入电极进行慢性电刺激疗法最早由哥伦比亚大学的神经外科医生提出。在DBS刚诞生的最初20年几乎没取得多少进展,直到电池大小、电池寿命技术方面的进步才为DBS的发展取得了突破。
1970年代,DBS作为干预运动障碍类疾病的手段开始被广泛地接受和使用。现代DBS设备出现于1987年。
脑起搏器发展历程
按照设备产品分类可以将DBS分为单通道和双通道两种。近年来,多个企业进入DBS领域,DBS技术不断革新突破,如分段式电极、方向电极、可充电电池、更长的电池寿命、更灵活的刺激参数和基于无线信号传输的远程控制等。
最新的DBS技术发展包括可以输出电流的方向电极/分段电极,更灵活的编程控制能力,磁共振影像兼容和脑电信号采集能力。
2、脑起搏器关键部件
DBS设备改造自心脏起搏器,其中包含颅内电极、连接导线和电脉冲发生器三个主要部件。在DBS诞生的40年时间里,随着工程学、影像学的进步加深了人们更好地理解DBS与患者的互动关系。
电极和电池设计上的突破、脉冲发生器刺激模式的可调节、闭环/按需求刺激和脑活动检测技术都是提升DBS的疗效以及拓宽DBS使用的方面。
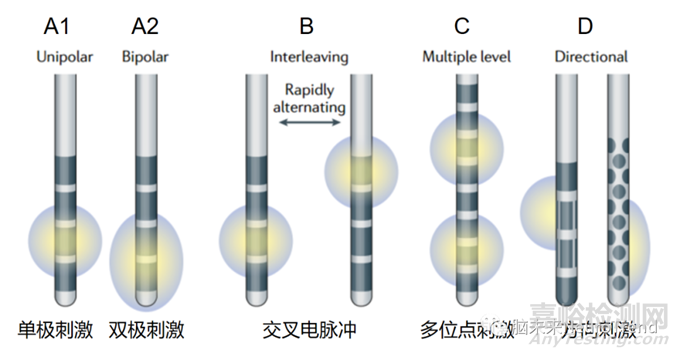
脑起搏器电极类型
作为直接植入在大脑组织内的部件,生物相容性是电极很重要的部分。长期植入的情况下,胶质细胞会包裹住电极,蛋白质吸收和离子环境都会影响电极的正常使用,引起局部炎症。
现阶段DBS电极的生产多还是依靠于人力手工制造,未来运用更现代的电子设备生产技术有可能可以提高电极设计的灵活度,缩小体积,使用不同材料来达到提升长期的表现和安全性。
3、脑起搏器全球市场
据Global Market Insights数据,2021年神经技术器械市场规模超过109亿美元,预计未来十年将以14.5%的复合年增长率上升,其中神经刺激在2021年约占69%的市场份额,并将持续上升。
DBS疗法的临床应用已有三十余年,2000年初进入中国以来,国内DBS市场基本被美敦力、波士顿科学和雅培这神经调节的三大外资巨头所独占,直到景昱医疗、品驰医疗等医疗技术公司致力于攻坚克难,研发出国产化的脑起搏器,才逐渐打破原有的垄断格局。
目前,随着医疗技术的发展,数字化脑起搏器治疗已成为各大器公司的主流创新方向,个性化治疗、远程治疗各类脑部疾病正在走向现实。
4、脑起搏器海外公司代表
(一) 美敦力
美敦力公司的Percept系列中最新一代脑起搏器---可充电Percept RC,分别于2023年11月获得CE认证和2024年1月获得FDA批准。
Percept系列是全球唯一一个具有传感功能的脑深部刺激器(DBS),允许医生对帕金森病、原发性震颤、肌张力障碍以及癫痫等运动障碍患者进行个性化治疗。
Percept RC
Percept RC是第一款搭载BrainSense技术的脑起搏器,同时也是最小、最薄、可充电的双通道神经刺激器。Percept RC主要由神经刺激器,BrainSense 技术和SenSight定向导线组成。
Percept PC相比于美敦力上一代脑起搏器 Activa PC小20%、薄20%,重量仅为61g,并设计更符合人体工程学,使患者舒适度大幅提高。
Percept PC尽管体积小巧,但是其电池使用寿命长达15年,且具有稳定快速的充电性能。与其它可充电脑起搏器相比,美敦力独有的专利电池技术的电池褪色程度更低,可提供更可靠、更持久的电池。Percept PC充电速度非常快,1小时内就能充满90%电量。
Percept RC相比于传统的脑起搏器,最大技术优势在于其搭载BrainSense 技术。BrainSense 技术可以使用植入的脑起搏器导线捕获大脑信号(LFP)并被记录。根据研究发现LFP的β功率与帕金森病的运动不能、运动减退和肌肉强直等症状相关。因此当BrainSense 技术将捕获LFP信号后,Percept RC可以在设定范围内自动调整,并输出刺激。从而实现个性化治疗。
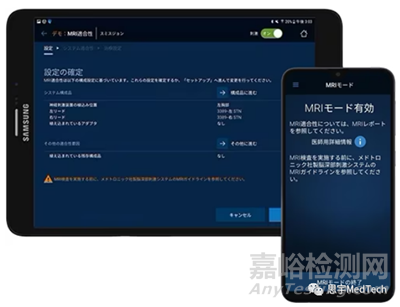
Percept RC是唯一一款兼容1.5T和3T MRI的脑起搏器,患者在一定条件下,可以不关闭脑起搏器治疗进行3T和1.5T的MRI扫描。
(二)波士顿科学
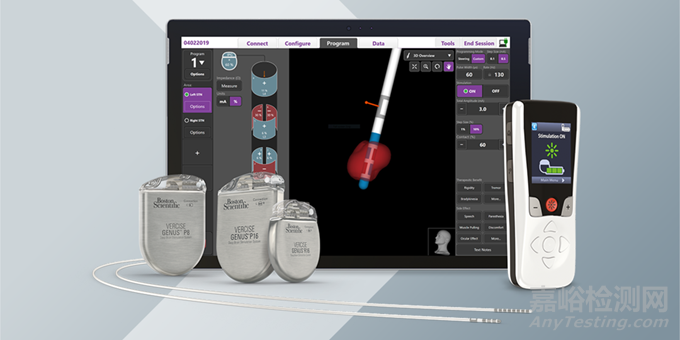
Vercise Genus是波士顿科学最新一代的 DBS 产品,其搭配的Cartesia方向性电极可以实现定向刺激,从而解决传统DBS环形电极缺陷。通过方向性电极的刺激方向调整,精准刺激目标神经核团,避免患者出现语言障碍、视觉障碍等不良反应。
Vercise Genus是属于第四代DBS产品,Vercise Genus系统在多个方面进行了创新,如独家的MICC控制模式、独家的端头方向性电极、领先的可视化程控等方面。Vercise Genus系统和传统DBS一样,主要由电极导线、脉冲发生器组成。
Vercise Genus
2023年7月12日,该公司宣布,其开发的新型脑深部刺激系统软件Vercise Neural Navigator 5已经获得美国FDA的批准。该软件可与Vercise Genus脑深部刺激系统配合使用,为帕金森病或原发性震颤患者提供有效的治疗方案。
(三)雅培
2024年1月25日,雅培宣布公司旗下的Liberta RC™脑起搏器(DBS)获得了FDA的批准,目前是世界上最小的具有远程编程功能的可充电DBS。
Liberta RC™ DBS IPG
关于这款设备,它的优点主要体现在体积、电池、充电器、控制、虚拟诊所五个方面:
体积:Liberta RC™的植入式脉冲发生器的体积为13.79cc,大小与智能手表的表盘相当,比美国目前可用的其他常用植入式可充电DBS约要小上31%。
电池:在标准设置下使用时,Liberta RC™需要使用充电器每37天充电一次(相当于每年10次)。如果用户喜欢每周充电,那么每周充电30分钟即可。充电要求是 FDA 批准的 DBS 系统中最低的。
充电器:充电器是无线的,要贴在脉冲发生器附近,但是充的时候用户可以活动。充电器的电量足以充满设备两次。
控制便利:可以使用专门的控制器或iOS设备控制Liberta RC™,比如说发送通知、调整设置和充电模式等等。
虚拟诊所:Liberta RC™系统是唯一兼容雅培专有的NeuroSphere™虚拟诊所的可充电DBS系统。这个虚拟诊所是美国首创的互联护理技术,于2021年3月在美国推出,允许用户在足不出户的情况下就能和医生沟通,确保DBS设备设置正确、功能正常,还能让用户根据医生的指导远程接受新的治疗设置。
5、脑起搏器国产企业突围崛起
高昂的费用曾经是影响我国患者接受脑起搏器的一大因素。但近年来,随着部分城市DBS逐渐纳入医保,价格进一步下降,百姓的医疗负担下降,DBS使用数量呈增长趋势。以上海为例,自纳入上海医保,选脑起搏器治疗的患者同期增加50%,为更多遭受帕金森、肌张力障碍等运动功能障碍的患者带来福音。
在国家政策红利支持及庞大的市场潜力吸引之下,我国脑起搏器领域发展前景可观,一些国产企业也突出重围,蓄势待发。
(一)景昱医疗(SceneRay)
作为国内第一代生物医学工程专业毕业生,景昱医疗创始人宁益华在2009年组建了技术团队,获得了苏州工业园区创业投资引导基金1100万元的投资后,成立景昱医疗公司。
2022年4月景昱医疗的双靶点脑深部电刺激(DBS)技术治疗药物成瘾适应症获得FDA突破性医疗器械资质,这是中国企业首次在神经及精神疾病领域获得突破性医疗器械资质。
景昱医疗可充电DBS
此外,景昱和空军军医大学合作研发的戒毒脑起搏器系统,降低吸毒成瘾后的高复吸率;与华为建立合作,运用华为AI系统,实现医生与患者间的异地互动、远程诊疗。
2022年2月,景昱医疗宣布完成3亿元人民币D+轮融资,由红杉中国和高瓴创投共同领投。
2023年12月19日,证监会官网显示,景昱医疗上市辅导备案登记获证监局受理,辅导机构为华泰联合证券,派出机构为江苏证监局。
(二)品驰医疗Beijing Pins
品驰医疗创立于2008年,通过与清华大学、北京天坛医院、协和医院等众多临床医院合作,建立了“产-学-研-医”协同创新的模式。其系列脑起搏器自2000年起由清华大学李路明教授团队牵头开始研发,2009年开展第一例临床试验,2014年获得全系列DBS产品注册证,2016年取得了CE认证。
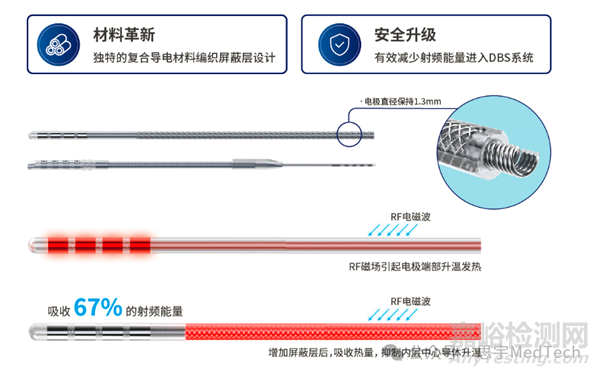
品驰®3.0T磁共振兼容脑起搏器(G106/G106R型),由品驰医疗和清华大学共同研制开发,具有完全自主知识产权,通过通过抗干扰设计解决植入患者体内的DBS电极导线在磁共振扫描期间产生热量,而引起周围组织热损伤的世界级医疗安全问题。
品驰®3.0T磁共振兼容脑起搏器(G106/G106R型)于2019年2月入选国家创新医疗器械特别审查程序,于2022年1月获得国家药品监督管理局颁发的三类医疗器械注册证,入选国家“十三五”科技创新成就展,入选“中国2022年度重要医学进展”。
品驰®3.0T磁共振兼容蓝牙可感知脑起搏器(G106RS型)于2023年3月获得三类医疗器械注册证获批上市,为首个国产磁共振兼容蓝牙可感知脑起搏器,填补国内空白。
品驰医疗3.0T磁共振兼容脑起搏器
2023年7月4日,新一代“蓝牙可感知、可充电、可远程程控的3.0T磁共振兼容脑起搏器(106RS型)”在中国科大附一院(安徽省立医院)完成上市后首例临床应用,标志着我国在神经调控领域取得了又一进步。