您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-04-25 12:30
背景
治疗性单克隆抗体(mAb)在治疗肿瘤药物中起到非常关键的作用,目前已经批准上市的单克隆抗体药物大约200种,其中治疗肿瘤相关疾病的大约90种。单克隆抗体作为免疫治疗癌症的方法已在各种癌症类型的治疗中得到验证,并取得良好的效果,多款以PD-1等免疫检查点作为靶点上市的抗体药物成为了mAb治疗癌症的代表[1]。
在这些药物的研发过程中,受体占有率(Receptor Occupancy,RO)可以反映抗体等蛋白类药物与细胞表面靶点的相对结合程度,受体占有率生物分析是抗体等大分子药物临床开发中重要的药效学(PD)指标之一[2]。RO生物分析有助于建立生物治疗剂的最小生物效应水平,并建立最佳的给药方案[3],也可以帮助更好理解药代动力学-药效学(PK-PD)的关系[4]。此外,RO分析生成的数据可用于评估安全性,例如,长期最大RO可能是过量给药的标志,与靶点长期结合,可能导致严重的副作用甚至毒性[5-6]。近年来,包括PD-1/PD-L1,Tim-3,LAG-3,4-1BB,CD3和CD47等众多靶点的单抗药物在临床的研究中,RO的生物分析都起到了非常重要的作用。
什么是受体占有率
RO,即受体占有率(Receptor Occupancy),是检测蛋白类药物对特定细胞亚群表面的特异靶点占据的程度(图1)。蛋白类药物主要包括单克隆抗体、配体、ADC和融合蛋白等;细胞亚群一般为外周血细胞,如红细胞、血小板、白细胞亚群(T细胞/B细胞/NK/单核/粒细胞等);药物靶点主要涉及PD-1/PD-L1、Tim3、4-1BB、CCR4、CD3和CD20等。
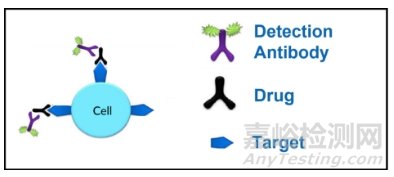
图1 :RO检测示意图,图片引自文献[7]
生物分析在药物临床研究中的意义
首先,剂量选择方面,RO生物分析可辅助早期剂量设定,随着药物浓度的增加,可以检测出RO饱和时所需的药物浓度;也可以帮助评估生物制剂的最小生物效应水平[3],在剂量爬坡实验中,可以帮助评估最佳给药剂量,其次,药理监测方面:RO生物分析可监测治疗药物与靶点的持续结合,评估给药间隔、频次等;例如,随着时间推移,RO在饱和后,又会逐渐的降低,药效也可能会降低,此时,再次给药,RO将再次达到饱和;同时,RO生物分析也可以作为生物标志物评估PK/PD的关系[4];然后,安全评估方面RO生物分析可评估靶点可能存在的安全风险,如CD47单抗的靶点位于肿瘤细胞,但红细胞也表达该靶点,红细胞上RO增加将会导致的红细胞裂解,进而引起贫血,这种情况下,红细胞的RO生物分析就显得十分重要;最后,RO生物分析可以评估长期饱和RO所导致毒副作用以及靶点非特异结合所产生的毒性[5-6]。
受体占有率的生物分析策略
平台的选择:流式细胞平台是临床前和临床试验中生物标志物分析和药物开发强有力的工具,因为它能够在单细胞水平上检测多种异质细胞群以及其表达的靶点,故可以检测靶点在感兴趣的细胞群体上与药物的结合,评估靶点与药物结合的程度。
策略选择:RO生物分析的基本策略包括两大类:直接法和间接法,这是RO分析两种最基本的形式,在实际应用中两种方式会有多种变化形式。直接法:临床给药后,需同时测出占据靶点位点的数量(图2-B)和药物饱和时位点的数量,其中饱和位点的检测需要在样本中加入过量药物,这样可以使所有的靶点均被占据。基本计算公式如下:RO的计算是受体占有率%=结合受体量/总受体量×100%;直接法中,检测试剂(检测抗体)的筛选非常重要。检测试剂的选择可以有多种,根据不同的药物,选择通用型抗人IgG的抗体,抗IgG亚型抗体或抗药抗体。
间接法:使用和药物非竞争性的抗体测出靶点的总量(图2-C),使用和药物竞争的抗体测出游离位点(图2-A)也就是没有被药物占据的靶点的量,两者相减后,除以靶点总量即可得出受体占有率。基本公式如下:受体占有率%=100%-游离受体/总受体×100%。间接法的检测试剂的选择同样重要,其中筛选到合适的竞争性抗体是关键。此外也可以采用荧光标记药物进行间接法受体占有率测定。
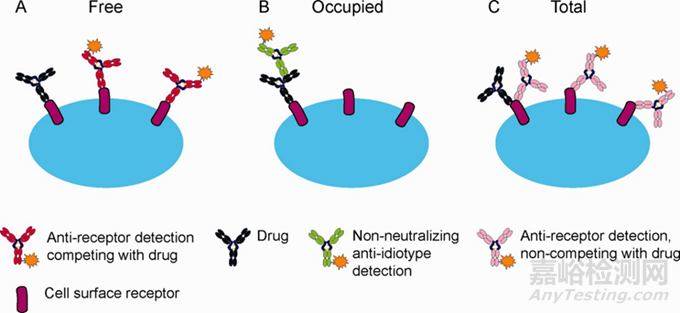
图2:受体占有率分析的基本策略(图2引自文献[8])
数据表现形式:(1)阳性百分比;(2)平均荧光强度或者等量可溶性荧光分子量(molecules of equivalent soluble fluorochrome ,MESF)。
RO分析的基本策略的设计考量点
首先需要考虑的就是药物背景及临床方案,抗体的IgG亚型会影响试剂的选择,而抗体的结构是单抗还是双抗或者多功能抗体也会影响基本策略的选择和结果计算及分析;临床方案中是否联合用药,联合用药是否感染干扰目标受体的检测;还要考虑药物是否会产生明显的免疫原性,ADA或者Nab也会影响受体的检测 ;如果临床考察RO的目的除了药效还有安全性的考虑,则RO生物分析可能还要涉及安全性相关的细胞群(比如:红细胞)。与此同时,了解靶点(受体)在哪些细胞群表达以及在细胞群的表达丰度会帮助科学筛选目标细胞群和准确的计算RO。最后,样本的类型(外周血\PBMC\肿瘤等)、储存条件和处理方法等也需要考虑进去。
受体占位生物分析挑战
由于药物结构复杂和靶点多样化以及表达差异等原因,RO生物分析方法的建立具有相当的挑战,本文主要讨论在临床样本进行RO分析时主要有以下几个挑战:(1)样品稳定性:临床采集全血样本或者组织样本均涉及新鲜活细胞,从研究场所采集运输到检测实验室,通常需要相当的时间,如果样品稳定性控制不好,从样品采集到分析的时间即可能会影响实际RO水平。针对不同的靶点可以使用不同类型抗凝剂或市售的稳定试剂,可以优化和延长样品稳定性。如果稳定期太短,可能要在采集后进行固定和染色。(2)临床样本量不足:由于单次检测RO通常至少需要100μl左右全血,再加上复管和对照管,可能需要更多体积的全血,而临床采集的全血样本通常有多个检测目的,此时可以考虑使用多重检测的方式,同时检测免疫表型和相关靶点RO,这样可以节约全血的体积,同时也对人员和仪器都有更高的要求。(3)靶点在靶细胞上表达量低:例如Tim3,在靶细胞上表达很低,对方法验证的完成造成了挑战,此时需要跟据不同的靶点选择不同的刺激剂,来增加靶点的表达。选择可替代的表达靶点较高的细胞群也是可以选择的方案。(4)生物变异性:在RO分析策略设计之前,要充分考虑到检测靶点的测量范围,用于方法验证的样品的分析物的检测值应该覆盖预期的样本中分析物的检测范围。(5)免疫原性:样本中含有ADA可能会影响RO的检测。(6)关键检测试剂:筛选完全竞争或者特异性良好的抗体也是方法开发和验证中重要的环节。
结语
开发和验证准确及稳定的受体占有率生物分析方法在药效动力学等方面起到非常重要的作用,然而,由于抗体药物本身结构复杂且靶点多样化,在开发和验证其生物分析方法中充满了挑战。流式细胞平台(FACS)具有强大的检测异质细胞群和与靶点与细胞结合的能力,通常RO分析会选择该平台。对于药物结构和特点以及靶点的生物学背景的深刻理解是方法成功开发的前提,基本策略的选择、关键试剂筛选和稳定性验证等方面均是方法开发的基本环节。目前药明康德测试事业部临床生物分析团队已经开发并验证了多种符合GLP法规要求的RO生物分析方法,药物蛋白的种类包含单抗、双抗和多功能抗体,所涉及的靶点包括PD-1、PD-L1、Tim-3、LAG-3、4-1BB、CD3和CD85d等。在FACS平台积累了丰富的RO生物分析经验,可以帮客户解决抗体等大分子药物再临床生物分析中遇到的各种挑战,加速药物研发和上市的进度。
参考文献:
[1] Sharpe AH, Pauken KE. The diverse functions of the PD1 inhibitory pathway. Nat Rev Immunol. 2018; 18: 153–67.
[2]Green CL, Stewart JJ, Hogerkorp CM, Lackey A, Jones N, Liang M, et al. Recommendations for the development and validation of flow cytometry-based receptor occupancy assays. Cytometry B Clin Cytom. 2016; 90: 141–9.
[3] Spitz S, Zhang Y, Fischer S, et al. 2020 White Paper on Recent Issues in Bioanalysis: BAV Guidance, CLSI H62, Biotherapeutics Stability, Parallelism Testing, CyTOF and Regulatory Feedback (Part 2A - Recommendations on Biotherapeutics Stability, PK LBA Regulated Bioanalysis, Biomarkers Assays, Cytometry Validation & Innovation Part 2B - Regulatory Agencies' Inputs on Bioanalysis, Biomarkers, Immunogenicity, Gene & Cell Therapy and Vaccine). Bioanalysis. 2021;13(5):295-361.
[4]Agrawal S, Feng Y, Roy A, Kollia G, Lestini B. Nivolumab dose selection: challenges, opportunities, and lessons learned for cancer immunotherapy. J Immunother Cancer. 2016;4:72. Published 2016 Nov 15.
[5]Vermeire S, O'Byrne S, Keir M, Williams M, Lu TT, Mansfield JC, Lamb CA, Feagan BG, Panes J, Salas A, et al. Etrolizumab as induction therapy for ulcerative colitis: a randomised, controlled, phase 2 trial. Lancet 2014; 384: 309–318.
[6]Hua F, Comer GM, Stockert L, Jin B, Nowak J, Pleasic-Williams S, Wunderlich D, Cheng J, Beebe JS. Anti-IL21 receptor monoclonal antibody (ATR-107): Safety, pharmacokinetics, and pharmacodynamic evaluation in healthy volunteers: a phase I, first-in-human study. J Clin Pharmacol 2014; 54: 14–22.
[7] Stewart JJ, Green CL, Jones N, et al. Role of receptor occupancy assays by flow cytometry in drug development. Cytometry B Clin Cytom. 2016;90(2):110-116.
[8] Liang M, Schwickart M, Schneider AK, et al. Receptor occupancy assessment by flow cytometry as a pharmacodynamic biomarker in biopharmaceutical development. Cytometry B Clin Cytom. 2016;90(2):117-127.

来源: 药明康德测试事业部


